
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Средние коэффициенты активности ионов при различной ионной силе раствора
Таблица 4 Произведение растворимости труднорастворимых в воде соединений (при 25 0С)
Продолжение таблицы 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Формула соединения | ПР | Формула соединения | ПР | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PbC2O4 | 3, 4 · 10–11 | MnS | 1, 1 × 10–15 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PbCrO4 | 1, 8 · 10–14 | MnCO3 | 5, 05 × 10–10 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PbCl2 | 1, 7 · 10–5 | Co(OH)2 | 1, 6 × 10–18 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PbS | 6, 8 · 10–29 | CoS | 3, 1 × 10–23 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SrSO4 | 3, 6 · 10–7 | CoCO3 | 1, 45 × 10–13 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sr(OH)2 | 6, 7 · 10–2 | Ni(OH)2 | 8, 7 × 10–19 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SrCO3 | 9, 42 · 10–10 | NiS | 1, 4 × 10–24 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SrC2O4 | 5, 6 · 10–8 | NiCO3 | 1, 35 × 10–7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SrCrO4 | 3, 6 · 10–5 | ZnS | 7, 4 × 10–27 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ZnCO3 | 9, 98 × 10–11 | Zn(OH)2 | 4, 5 · 10–17 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ZnC2O4 | 2, 0 × 10–8 | Mg(OH)2 | 5, 5 × 10–12 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Таблица 5
Вычисление растворимости электролита ( S ) в моль/л
| Тип электролита | Растворимость, моль/л |
| 1. Бинарный электролит (типа BaSO4, CaCO3 и др.) | 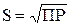
|
| 2. Трехионный электролит (типа CaF2, Ag2CrO4 и др.) | 
|
| 3. Четырехионный электролит (типа Ag3PO4, BiJ3 и др.) | 
|
| 4. Пятиионный электролит (типа Ca3(PO4)2, Bi2 J3 др.) | 
|
Таблица 6
Плотности водных растворов некоторых кислот и щелочей
при 15 0С (в г/см3)
| W, % | Вещество | ||||
| H2SO4 | HNO3 | HCl | KOH | NaOH | |
| 2 | 1, 013 | 1, 011 | 1, 009 | 1, 016 | 1, 023 |
| 4 | 1, 027 | 1, 022 | 1, 019 | 1, 033 | 1, 046 |
| 6 | 1, 040 | 1, 033 | 1, 029 | 1, 048 | 1, 069 |
| 8 | 1, 055 | 1, 044 | 1, 039 | 1, 065 | 1, 092 |
| 10 | 1, 069 | 1, 056 | 1, 049 | 1, 082 | 1, 115 |
| 12 | 1, 083 | 1, 068 | 1, 059 | 1, 100 | 1, 137 |
| 14 | 1, 098 | 1, 080 | 1, 069 | 1, 118 | 1, 159 |
| 16 | 1, 112 | 1, 093 | 1, 079 | 1, 137 | 1, 181 |
| 18 | 1, 127 | 1, 106 | 1, 083 | 1, 156 | 1, 213 |
| 20 | 1, 143 | 1, 119 | 1, 100 | 1, 176 | 1, 225 |
| 22 | 1, 158 | 1, 132 | 1, 110 | 1, 196 | 1, 247 |
| 24 | 1, 174 | 1, 145 | 1, 121 | 1, 217 | 1, 268 |
| 26 | 1, 190 | 1, 158 | 1, 132 | 1, 240 | 1, 289 |
| 28 | 1, 205 | 1, 171 | 1, 142 | 1, 263 | 1, 310 |
| 30 | 1, 224 | 1, 184 | 1, 152 | 1, 286 | 1, 332 |
| 32 | 1, 238 | 1, 198 | 1, 163 | 1, 310 | 1, 352 |
| 34 | 1, 255 | 1, 211 | 1, 173 | 1, 334 | 1, 374 |
| 36 | 1, 273 | 1, 225 | 1, 183 | 1, 358 | 1, 395 |
| 38 | 1, 290 | 1, 238 | 1, 194 | 1, 384 | 1, 416 |
| 40 | 1, 307 | 1, 251 | 1, 411 | 1, 437 | |
| 42 | 1, 324 | 1, 264 | 1, 437 | 1, 458 | |
| 44 | 1, 342 | 1, 277 | 1, 460 | 1, 478 | |
| 46 | 1, 361 | 1, 290 | 1, 485 | 1, 499 | |
| 48 | 1, 380 | 1, 303 | 1, 511 | 1, 519 | |
| 50 | 1, 399 | 1, 316 | 1, 538 | 1, 540 | |
| 52 | 1, 419 | 1, 328 | 1, 564 | 1, 560 | |
| 54 | 1, 439 | 1, 340 | 1, 590 | 1, 580 | |
| 56 | 1, 460 | 1, 351 | 1, 616 | 1, 601 | |
| 58 | 1, 482 | 1, 362 | 1, 622 | ||
|
Продолжение таблицы 6 | |||||
| W, % | Вещество | ||||
| H2SO4 | HNO3 | HCl | KOH | NaOH | |
| 60 | 1, 503 | 1, 3773 | 1, 643 | ||
| 62 | 1, 525 | 1, 384 | |||
| 64 | 1, 547 | 1, 394 | |||
| 66 | 1, 571 | 1, 403 | |||
| 68 | 1, 594 | 1, 412 | |||
| 70 | 1, 617 | 1, 421 | |||
| 72 | 1, 640 | 1, 429 | |||
| 74 | 1, 664 | 1, 437 | |||
| 76 | 1, 687 | 1, 445 | |||
| 78 | 1, 710 | 1, 53 | |||
| 80 | 1, 732 | 1, 460 | |||
| 82 | 1, 755 | 1, 467 | |||
| 84 | 1, 776 | 1, 474 | |||
| 88 | 1, 808 | 1, 486 | |||
| 90 | 1, 819 | 1, 491 | |||
| 92 | 1, 830 | 1, 196 | |||
| 94 | 1, 837 | 1, 500 | |||
| 98 | 1, 841 | 1, 510 | |||
| 100 | 1, 838 | 1, 522 | |||
Таблица 7
Криоскопические (К) и эбуллиоскопические (Е) постоянные
| Растворитель | Температура кристаллизации, 0С | К | Температура кипения, 0С | Е |
| Ацетон | – 94, 6 | 2, 4 | 56, 0 | 1, 48 |
| Анилин | –6 | 5, 87 | 184, 4 | 3, 69 |
| Бензол | 5, 5 | 5, 10 | 80, 2 | 2, 57 |
| Вода | 0 | 1, 86 | 100 | 0, 52 |
| Камфора | 6, 09 | 40, 0 | 204 | 6, 09 |
| Нитробензол | 5, 27 | 6, 90 | 210, 9 | 5, 27 |
| Уксусная кислота | 16, 7 | 3, 90 | 118, 4 | 3, 1 |
| Фенол | 3, 6 | 7, 3 | 182, 1 | 3, 6 |
| Хлороформ | 3, 88 | 4, 9 | 61, 2 | 3, 88 |
| Четыреххлористый углерод | 4, 3 | 2, 98 | 76, 7 | 5, 3 |
Таблица 8
Полуреакции и стандартные окислительные потенциалы восстановления окислителей в водных растворах по отношению к водородному электроду
(при t = 25оС)
| Уравнение реакции | φ ° | |
| АЗОТ HNO2 + e + H+ ↔ NO + H2O 2HNO2 + 6e + 6H+ ↔ N2 + 4H2O NO3- + 2e + 3H+ ↔ HNO2 + H2O NO3- + e + 2H+ ↔ NO2 + H2O NO3- + 3e + 4H+ ↔ NO + 2H2O NO3- + 8e + 10H+ ↔ NH4+ + 3H2O NO3- + 8e + 6H2O ↔ NH3 + 9OH- N2 + 6e + 8H+ ↔ 2NH4+ | +0, 99 +1, 45 +0, 94 +0, 81 +0, 96 +0, 87 -0, 12 +0, 28 | |
| АЛЮМИНИЙ Al3+ + 3e ↔ Al AlO2- + 3e + 2H2O ↔ Al + 4OH- | -1, 67 -2, 35 | |
БАРИЙ
Ba2+ + 2e ↔ Ba
БЕРИЛЛИЙ
Be2+ + 2e ↔ Be
БОР
HBO3 + 3e + 3H+ ↔ B + 3H2O
БРОМ
Br2 + 2e ↔ 2Br –
HBrO + 2e + H+ ↔ Br - + H2O
BrO- + 2e + H2O ↔ Br - + 2OH-
2BrO3- + 10e + 12H+ ↔ Br2 + 6H2O
BrO3- + 6e + 6H+ ↔ Br - + 3H2O
BrO3- + 6e + 3H2O ↔ Br - + 6OH-
ВАНАДИЙ
V2+ + 2e ↔ V
V3+ + e ↔ V2+
VO2+ + e + 2H+ ↔ V3+ + H2O
VO2+ + e + 2H+ ↔ VO2+ + H2O
VO2+ + 2e + 4H+ ↔ V3+ + 2H2O
VO2+ + 3e + 4H+ ↔ V2+ + 2H2O
ВИСМУТ
Bi3+ + 3e ↔ Bi
NaBiO3 + 2e + 6H+ ↔ Bi3+ + Na+ + 3H2O
ВОДОРОД
2H+ + 2e ↔ H2
H2 + 2e ↔ 2H-
2H2O + 2e ↔ H2 + 2OH-
ВОЛЬФРАМ
WO2 + 4e + 4H+ ↔ W + 2H2O
WO3 + 6e + 6H+ ↔ W + 3H2O
WO4 2- + 6e + 4H2O ↔ W + 8OH-
ГЕРМАНИЙ
H2GeO3 + 4e + 4H+ ↔ Ge + 3H2O
ЖЕЛЕЗО
Fe2+ + 2e ↔ Fe
Fe3+ + e ↔ Fe2+
[Fe(CN)6]2- + e ↔ [Fe(CN)6]-
[FeF6]3- + e ↔ Fe2+ + 6F-
Fe(OH)3 + e ↔ Fe(OH)2 + OH-
ЗОЛОТО
Au3+ + e ↔ Au2+
[AuCl4] - + 3e ↔ Au + 4Cl-
Au3+ + 2e ↔ Au+
Au+ + e ↔ Au
[Au(CN)2] - + e ↔ Au + 2CN-
ИОД
I2 + 2e ↔ 2I –
[I3]- + 2e ↔ 3I -
2HIO + 2e + 2H+ ↔ I2 + 2H2O
IO- + 2e + H2O ↔ I - + 2OH-
2IO3- + 10e + 12H+ ↔ I2 + 6H2O
IO3- + 6e + 6H+ ↔ I - + 3H2O
IO3- + 6e + 3H2O ↔ I - + 6OH-
H5IO6 + 2e + H+ ↔ IO3 - + 3H2O
КАЛИЙ
K+ + e ↔ K
КАЛЬЦИЙ
Ca2+ + 2e ↔ Ca
КИСЛОРОД
O2 + 4e + 4H+ ↔ 2H2O
O2 + 4e + 2H2O ↔ 4OH-
O3 + 2e + 2H+ ↔ O2 + H2O
O3 + 2e + 2H2O ↔ O2 + 2OH-
O2 + 2e + 2H2O ↔ H2O2 + 2OH-
H2O2 + 2e + 2H+ ↔ 2 H2O
O2 + 2e + 2H+ ↔ H2O2
КОБАЛЬТ
Co2+ + 2e ↔ Co
Co3+ + e ↔ Co2+
Co(OH)3 + e ↔ Co(OH)2 + OH-
[Co(NH3)6]3+ + e ↔ [Co(NH3)6]2+
[Co(CN)6]3- + e ↔ [Co(CN)6]2-
КРЕМНИЙ
Si + 4e + 4H+ ↔ SiH4
Si + 4e + 4H2O ↔ SiH4 + 4OH-
SiO2 + 4e + 4H+ ↔ Si + 2H2O
SiO32- + 4e + 3H2O ↔ Si + 6OH-
[SiF6]2- + 4e ↔ Si + 6F-
ЛИТИЙ
Li+ + e ↔ Li
МАГНИЙ
Mg2+ + 2e ↔ Mg
МАРГАНЕЦ
Mn2+ + 2e ↔ Mn
MnO2 + 2e + 4H+ ↔ Mn2+ + 2H2O
MnO4- + 5e + 8H+ ↔ Mn 2++ 4H2O
MnO4- + 3e + 4H+ ↔ MnO2 + 2H2O
MnO4- + 2e + 2H2O ↔ MnO2 + 4OH-
MnO4- + 3e + 2H2O ↔ MnO2 + 4OH-
МЕДЬ
Cu2+ + 2e ↔ Cu
Cu2+ + e ↔ Cu+
Cu2+ + e + I- ↔ CuI
Cu2+ + e + 2CN- ↔ [Cu(CN)2]-
МЫШЬЯК
AsO2- + 3e + 2H2O ↔ As + 4OH-
HAsO2 + 3e + 3H+ ↔ As + 2H2O
H3AsO4 + 2e + 2H+ ↔ HAsO2 + 2H2O
AsO43- + 2e + 2H2O ↔ AsO2- + 4OH-
As + 3e + 3H+ ↔ AsH3
НАТРИЙ
Na+ + e ↔ Na
НИКЕЛЬ
Ni2+ + 2e ↔ Ni
Ni(OH)3 + e ↔ Ni(OH)2 + OH-
Ni(OH)3 + e + 3H+ ↔ Ni(OH)2 + OH-
[Ni(CN)4]3- + e ↔ [Ni(CN)6]2-
ОЛОВО
Sn2+ + 2e ↔ Sn
Sn4+ + 2e ↔ Sn2+
Sn4+ + 4e ↔ Sn
HSnO2- + 2e + H2O ↔ Sn + 3OH-
[Sn(OH)6]2- + 2e ↔ HSnO2- + 3OH- + H2O
ОСМИЙ
OsO4 + 8e + 8H+ ↔ Os + 4H2O
ПЛАТИНА
[PtCl4]2- + 2e ↔ Pt + 4Cl-
[PtCl6]2- + 2e ↔ [PtCl4]2- +2Cl-
РТУТЬ
Hg2+ + 2e ↔ Hg
Hg 22+ + 2e ↔ 2Hg
2Hg2+ + 2e ↔ Hg22+
2HgCl2 + 2e ↔ Hg2Cl2 +2Cl-
Hg2Cl2 + 2e ↔ 2Hg +2Cl-
СВИНЕЦ
Pb2+ + 2e ↔ Pb
Pb4+ + 2e ↔ Pb2+
Pb4+ + 4e ↔ Pb
PbO2 + 2e + 4H+ ↔ Pb2+ + 2H2O
СЕРА
S + 2e ↔ S2-
S + 2e + 2H+ ↔ H2S
[S2]2- + 2e + 2H+ ↔ 2S2-
S4O62- + 2e ↔ 2S2O32-
SO32- + 6e + 3H2O ↔ S2- + 6OH-
SO42- + 2e + 4H+ ↔ H2SO3 + H2O
SO42- + 2e + H2O ↔ SO32- + 2OH-
SO42- + 6e + 6H+ ↔ S + 4H2O
S2O82- + 2e ↔ 2SO42-
(SCN)2 + 2e ↔ 2SCN-
SO42- + 8e + 8H+ ↔ S2- + 4H2O
SO42- + 8e + 10H+ ↔ H2S + 4H2O
СЕЛЕН
Se + 2e ↔ Se2-
-0, 36
+0, 03
СЕРЕБРО
Ag+ + e ↔ Ag
Ag2O + 2e + H2O ↔ 2Ag + 2OH-
Ag2S + 2e ↔ 2Ag + S2-
[Ag(CN)2]- + e ↔ Ag + 2CN-
AgCl + e ↔ Ag + Cl-
AgBr + e ↔ Ag + Br-
AgI + e ↔ Ag + I-
СУРЬМА
Sb + 3e + 3H+ ↔ SbH3
SbO- + 3e + 2H+ ↔ Sb + H2O
SbO3- + 2e + H2O ↔ SbO2- + 2OH-
ТАЛЛИЙ
Tl+ + e ↔ Tl
Tl3+ + 2e ↔ Tl+
Tl3+ + 3e ↔ Tl
ТЕЛЛУР
Te + 2e ↔ Te2-
Te + 2e + 2H+ ↔ H2Te
TeO42- + 2e + H2O ↔ TeO32- + 2OH-
ТИТАН
Ti2+ + 2e ↔ Ti
Ti3+ + e ↔ Ti2+
TiO2 + 4e + 4H+ ↔ Ti + 2H2O
[TiF6]2- + 4e ↔ Ti + 6F-
УГЛЕРОД
CH3CHO + 2e + 2H+ ↔ C2H5OH
HCHO + 2e + 2H+ ↔ CH3OH
HCOOH + 2e + 2H+ ↔ HCHO + H2O
CO2 + 2e + 2H+ ↔ HCOOH
CH3COOH + 2e + 2H+ ↔ CH3CHO + H2O
2CO2 + 2e + 2H+ ↔ HOOCCOOH
C6H4O2 + 2e + 2H+ ↔ C6H4(OH)2
ФТОР
F2 + 2e ↔ 2F –
F2 + 2e + 2H+ ↔ 2HF
OF2 + 4e + 2H+ ↔ 2F- + H2O
ХЛОР
Cl2 + 2e ↔ 2Cl –
ClO3- + 6e + 6H+ ↔ Cl- + 3H2O
ClO3- + 6e + 3H2O ↔ Cl - + 6OH-
HOCl + 2e + H+ ↔ Cl - + H2O
ClO- + 2e + H2O ↔ Cl - + 2OH-
ClO2 + 5e + 4H+ ↔ Cl- + 2H2O
ClO4- + 8e + 8H+ ↔ Cl- + 4H2O
ClO4- + 8e + 4H2O ↔ Cl - + 8OH-
2ClO3- + 10e + 12H+ ↔ Cl2 + 6H2O
2HOCl + 2e + 2H+ ↔ Cl2 + 2H2O
ХРОМ
Cr2+ + 2e ↔ Cr
Cr3+ + 3e ↔ Cr
Cr3+ + e ↔ Cr2+
CrO42- + 3e + 4H2O ↔ Cr(OH)3 + 5OH-
Cr2O72- + 6e + 14H+ ↔ 2Cr3+ + 7H2O
ЦЕРИЙ
Ce3+ + 3e ↔ Ce
Ce3+ + e ↔ Ce2+
ЦИНК
Zn2+ + 2e ↔ Zn
[Zn(CN)4]2- + 2e ↔ Zn + 4CN-
ZnO22- + 2e + 2H2O ↔ Zn + 4OH-
ЦИРКОНИЙ
ZrO2 + 4e + 4H + ↔ Zr + 2H2O
Таблица
Латинский алфавит
| Шрифт ПЭВМ | Название | Шрифт ПЭВМ | Название | ||
| прямой | курсив | прямой | курсив | ||
| А а | А а | a | Nn | Nn | эн |
| В b | В b | бе | Оо | Оо | о |
| С с | С с | це | Рр | РР | пэ |
| D d | D d | де | Q q | Q q | ку |
| Е е | Е е | е | R r | R r | эр |
| F f | F f | эф | S s | S s | эс |
| G g | G g | ге | T t | T t | тэ |
| H h | H h | аш | U u | U u | у |
| I i | I i | и | V v | V v | ве |
| J j | J j | йот | W w | W w | дубль-ве |
| K k | K k | ка | X x | X x | икс |
| L I | L l | эль | Y y | Y y | игрек |
| M m | M m | эм | Z z | Z z | зет |
Таблица
Греческий алфавит
| Шрифт ПЭВМ | Название | Произношение | Латинская транскрипция |
| Aa | альфа | а | а |
| Bb | бета | б | b |
| Gg | гамма | г | g |
| Dd | дельта | д | d |
| Ee | эпсилон | э | е |
| Zz | дзэта | дэ | z |
| Hh | эта | э | 
|
| QqJ | тхэта | тх | th |
| Ii | йота | и | i |
| Kk | каппа | к | с |
| Ll | ламбда | л | 1 |
| Mm | мю | м | m |
| Nn | ню | н | n |
| Xx | кси | кс | x |
| Oo | омикрон | о | o |
| Pp | ли | п | p |
| Rr | Ро | р | r |
| SsV | сигма | с | s |
| Tt | тау | т | t |
| Uu | ипсилон | ю | у |
| Ffj | фи | ф | ph |
| Cc | хи | х | ch |
| Yy | пси | пс | ps |
| Ww | омега | о | 
|
Таблица
Названия групп (номенклатура) неорганических ионов и лиганд
Группа
Названия групп
* - В отечественной литературе соединительную гласную «о» опускают (фтор, хлор, бром, йод).
Источник: Волков А.И., Жарский И.М. Большой химический справочник - Мн.: Современная школа, 2005. - 608 с.
Таблица 7
Последнее изменение этой страницы: 2019-10-04; Просмотров: 1024; Нарушение авторского права страницы