
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Общие признаки массообменных процессовСтр 1 из 20Следующая ⇒
Часть
Разработала канд. техн. наук, доц. ___________ Р.Р.Ибрагимова (подпись, дата)
Уфа 2018
Рекомендуемая литература 1. Касаткин А.Г. Основные процессы и аппараты химической технологии. 14-е изд. (перепечатано с 9-го изд. 1973 г.).- М.: Альянс, 2008.-750с. 2. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. 14 изд. (перепеч. с изд. 1987 г.), -М.: Альянс, 2007.-576с. 3.Скобло А.И., Молоканов Ю.К., Владимиров А.И., Щелкунов В.А. Процессы и аппараты нефтегазопереработки и нефтехимии: Учебник для вузов.- 3-е изд., перераб. и доп. – М.: Недра-Бизнесцентр, 2000, 677 с. 4 Молоканов Ю.К. Процессы и аппараты нефтегазопереработки. – М., Химия, 1980, 408 с. 5. Сугак А.А, Процессы и аппараты химической технологии / А.В.Сугак, В.К.Леонтьев, В.В.Туркин.- М.: Издательский центр «Академия», 2005.- 224с. Основные понятия и законы массообмена Общие признаки массообменных процессов Массообменные или диффузионные процессы связаны с переходом компонентов из одной фазы в другую с целью их разделения. Все массообменные процессы обладают рядом общих признаков. 1. Они применяются для разделения гомогенных смесей. 2. В любом процессе участвуют, по крайней мере, две фазы: жидкая и паровая (перегонка и ректификация), жидкая и газовая (абсорбция), твердая и парогазовая (адсорбция), твердая и жидкая (адсорбция, экстракция), две жидких (экстракция). 3. Переход вещества из одной фазы в другую осуществляется за счет диффузии. 4. Движущей силой массообменных процессов является разность концентраций или градиент концентраций. Процесс протекает в направлении той фазы, в которой концентрация компонента меньше. 5. Перенос вещества из одной фазы в другую происходит через границу раздела фаз, на которой предполагается состояние равновесия фаз. 6. Диффузионные процессы обратимы, т.е. направление процесса определяется законами фазового равновесия. 7.Переход вещества из одной фазы в другую заканчивается при достижении динамического равновесия. Состояние равновесия следует понимать так, что обмен между фазами не прекращается, однако скорости перехода компонентов из одной фазы в другую выравниваются. Классификация массообменных процессов
Ректификация- процесс многократного противоточного контактирования встречных неравновесных потоков пара и жидкости с целью разделения жидких гомогенных смесей на фракции. Абсорбция – процесс избирательного поглощения компонентов газовой смеси жидким поглотителем – абсорбентом. Экстракция- процесс избирательного извлечения компонентов из жидкой смеси (или из твердого вещества) жидким экстрагентом. Адсорбция – процесс избирательного поглощения компонентов газовой или жидкой смеси твердым поглотителем – адсорбентом. Сушка – процесс удаления жидкости (влаги) из твердых материалов Мембранные процессы – избирательное извлечение компонентов смеси или их концентрирование с помощью полупроницаемой перегородки- мембраны. . Ректификация Рис.2.3 Изобарные температурные кривые бинарной смеси Закон-Рауля-Дальтона Изобарные кривые можно построить экспериментально, а также расчетным методом. Точка А1 на кривой кипения жидкости может быть найдена по закону Рауля. Парциальное давление компонента pi идеального раствора равно произведению давления насыщенных паров Pi при данной температуре на мольную концентрацию компонента в жидкой фазе x’: Давление насыщенных паров каждого компонента вычисляют по эмпирическим формулам. Например, по формуле Антуана где А, В, С - константы, зависящие от свойств вещества и определяемые экспериментально; t - температура. Известно, что жидкость начинает кипеть при такой температуре, при которой давление ее насыщенных паров становится равным внешнему давлению. Условие кипящей жидкости:
Откуда
По закону Дальтона парциальное давление компонента газовой смеси равно произведению давления в системе на мольную долю компонента в газовой смеси
При равновесии давление во всех точках системы одинаково. Объединенный закон Рауля-Дальтона pi = PБ x’i = π y’i. ( 25 )
Следовательно, при данных температуры и давления системы равновесные составы паровой и жидкой фаз однозначно определяются давлениями насыщенных паров компонентов смеси.
Энтальпийная диаграмма Для анализа и расчета процессов перегонки и ректификации используют энтальпийные диаграммы, дающие взаимосвязь составов жидкой и паровой фаз с их энтальпиями. Энтальпия (или теплосодержание) жидкости равна количеству тепла, необходимого для нагрева жидкости от 0оС до заданной температуры. Энтальпия пара равна количеству тепла, необходимого для нагрева вещества от 0оС до заданной температуры учетом тепла испарения и перегрева паров. Величина энтальпии жидкости и пара определяется эмпирически по таблицам или по приближенным формулам:
Энтальпийные диаграммы используют при расчетах перегонки и ректификации, когда необходимо одновременно учитывать материальные и тепловые потоки. На энтальпийной диаграмме приведены кривые энтальпии кипящей жидкости и энтальпии насыщенных паров в зависимости от концентрации. Любая точка А на энтальпийной диаграмме, лежащая ниже кривой энтальпии жидкой фазы характеризует систему, состоящую только из жидкой фазы. Любая точка А4, лежащая выше кривой энтальпии паровой фазы, состоит из перегретых паров. Точки, расположенные между кривыми, например А2 характеризует двухфазные системы. Вертикальные отрезки между кривыми энтальпий паровой и жидкой фаз отвечают скрытой теплоте испарения (конденсации) смеси определенного состава. Физический смысл величины скрытой теплоты испарения Т.к. скрытая теплота испарения у разных веществ не совпадают, то энтальпийные кривые жидкости и пара не параллельны. На энтальпийной диаграмме коноды изображаются наклонными прямыми. Поскольку на графиках изобар коноды располагаются горизонтально, т.е. положение их легко определить, а на энтальпийной диаграмме - наклонно под разными углами к оси абсцисс, то для удобства построений энтальпийную диаграмму обычно совмещают с графиком изобарных температурных кривых (рисунок 2.5).
Рис.2.5 Представление процесса ОИ (ОК) бинарной смеси на энтальпийной диаграмме и изобарных температурных кривых
Для бинарной смеси по НКК F× xf=D× yd+W× xw, Где xf - доля НКК в сырье, yd -доля НКК в дистилляте xw - доля НКК в остатке,
Преобразуем W=F-D F× xf= D× yd- (F-D)× xw F× (xf- xw)=D× ( yd- xw) Потоки колонны и соответствующие концентрации взаимосвязаны и не могут устанавливаться произвольно. Работа колонны связана с обменом энергии между фазами, В колонне тепло подводится с сырьем и нагревателем и уходит с дистиллятом, остатком и холодильником. Тепловой баланс ректификационной колонны: Qf+Qн=Qd+Qw+Qх, где Qf –количества тепла вносимого с сырьем, Qн -количество тепла, вносимого нагревателем, Qd -количество тепла, уходящего с дистиллятом, Qw – количество тепла, уносимого с остатком, Qх -количество тепла, снимаемого холодильником-конденсатором. При заданных составах и отборах дистиллята и остатка величины Qd и Qw –постоянная величина. Преобразуем предыдущее уравнение: Qf+( Qн- Qх)= Qd+Qw=const При неизменной температуре и составе сырья Qf=const, тогда величина ( Qн- Qх) =const Исходя из вышеизложенного можно сделать следующие выводы: 1)Разность между Qd и Qw –постоянная величина 2)При увеличении количества тепла, вносимого с сырьем, необходимо уменьшать нагрев. Тепловые потоки должны быть увязаны с материальными потоками и качеством получаемых продуктов. Уравнения рабочих линий 2.7.1 Уравнение рабочей линии верхней части колонны Составим систему уравнений материальных балансов для верхней секции (рисунок 2.6). .
общий:
по низкокипящему компоненту
Подставим одно уравнение в другое:
Поделим на D правую часть уравнения
Обозначим R=gn+1/ D Преобразуем уравнение
При этом R называется флегмовое число. Это уравнение называется уравнением рабочей линии встречных неравновесных потоков верхней части колонны, уравнением концентраций, или уравнением оперативной линии. Оно устанавливает связь встречных потоков пара и жидкости в произвольном сечении колонны. В координатах x - y уравнение представляет собой кривую линию, т.к. в общем случае поток флегмы может изменяться по высоте верхней части колонны, что приводит к изменению тангенса угла наклона этой линии. Если поток флегмы не изменяется по высоте колонны, то рабочая линия будет прямой. На диаграмме рабочая линия верхней части колонны имеет характерные точки (рисунок 2.7). При x=yD
получим, y=yD=x Одна из этих точек D находится на диагонали и ее положение не зависит от потока паров и флегмы. Вторая точка (B) определяется при x = 0 тогда:
Положение точки B зависит от величины флегмового числа R=gn+1/ D. При увеличении R точка B перемещается вниз, а рабочая линия приближается к диагонали. В пределе при R ®¥ (или g ®¥ ), рабочая линия сольется с диагональю ОА. Этот режим называется режим полного орошения.
Рис. 2.7 Рабочие линии на диаграмме x—у: I — равновесная кривая; 2 — рабочая линия верхней части колонны; 3 — то же, нижней.
Проанализируем работу нижней части колонны, для чего рассмотрим потоки ниже сечения 2-2 (рисунок 8.1).
W. xw
Система балансовых уравнений имеет следующий вид:
для низкокипящего компонента:
Решая совместно уравнения, вставим одно уравнение в другое:
Поделим на W:
обозначим П = Gn / W-паровое число:
Выделим y:
Это уравнение называется уравнением рабочей линии парового орошения или уравнение встречных неравновесных потоков в нижней части колонны. В координатах x - y уравнение представляет собой кривую линию, т.к. в общем случае поток пара может изменяться по высоте нижней части колонны, что приводит к изменению тангенса угла наклона этой линии. Если поток пара не изменяется по высоте колонны, то рабочая линия будет прямой.
На диаграмме рабочая линия нижней части колонны имеет характерные точки (рисунок 2.7). Одна из этих точек W находится на диагонали и ее положение не зависит от потока паров и флегмы. x=xw
Другая точка (С) определяется при y = 1, тогда:
Положение точки С зависит от величины парового числа П = Gn / W. При увеличении П точка С перемещается вправо, а рабочая линия приближается к диагонали. В пределе при П®¥ (или G®¥ ), рабочая линия сольется с диагональю ОА. Этот режим называется режим полного орошения.
Эффективность тарелки Рассмотренные методы расчетов позволяют определить число теоретических тарелок, обеспечивающих достижение состояния равновесия между покидающими данную тарелку потоками. На реальной тарелке такое состояние может не достигаться, поэтому изменение концентраций потоков в пределах данной контактной ступени обычно меньше, чем на теоретической тарелке. Для перехода от числа теоретических NT к числу реальных тарелок NД пользуются понятием к.п.д. тарелки
Для расчета величины к.п.д. тарелок существуют различные уравнения, в частности, уравнение Фенске используется в режиме полного орошения:
Тарельчатые колонны Рис. 2.21. Тарелка с S-образными элементами и клапанами
Клапанные тарелки. Принцип действия клапанных тарелок состоит в том, что свободно лежащий над отверстием в тарелке клапан различной формы автоматически регулирует величину площади зазора между клапаном и плоскостью тарелки в зависимости от газопаровой нагрузки и тем самым поддерживает постоянной (в пределах высоты подъема клапана) скорость газа и, следовательно, гидравлическое сопротивление тарелки в целом.
Рис. 2.22 Клапанно-прямоточная тарелка
Высота подъема клапана ограничивается высотой ограничителя (кронштейна, ножки). Отличительной особенностью клапанных тарелок является увеличение их свободного сечения по мере увеличения скорости газа. Благодаря этому скорость газа при его выходе в слой жидкости остается примерно постоянной вплоть до полного открытия клапана. Перекрытие отверстий тарелки саморегулирующимися клапанами позволяет расширить интервал рабочих нагрузок.
Рис.2.23. Типы некоторых колпачков и клапанов: колпачки: а — круглый; б — шестигранный; в — прямоугольный; г — желобчатый; д — S-образный; клапаны: е — прямоугольный; ж — круглый с нижним ограничителем; з — то же с верхним ограничителем; и — балластный; к — дисковый эжекционный перекрестноточный; л — пластинчатый перекрестно-прямоточный; м — S-образный колпачок с клапаном; 1 — диск тарелки; 2 — клапан; 3 — ограничитель; 4 — балласт
Среди клапанных тарелок нового поколения можно отметить дисковые эжекционные (перекрестноточные) и пластинчатые перекрестно-прямоточные тарелки, внедрение которых на ряде НПЗ страны позволило улучшить технико-экономические показатели установок перегонки нефти (рис. 2.23к, л) 1. Эжекционная клапанная тарелка представляет собой полотно с отверстиями (∅ 90 мм) и переливными устройствами. В отверстия полотна тарелок устанавливаются клапаны, представляющие собой вогнутый диск (∅ 110 мм) с просечными отверстиями (каналами) для эжекции жидкости, имеющий распределительный выступ для равномерного стока жидкости в эжекционные каналы. Клапаны имеют 4 ограничительные ножки и 12 эжекционных каналов. Они изготавливаются штамповкой из нержавеющей стали толщиной 0, 8...1, 0 мм. Масса одного клапана составляет всего 80…90 г (а капсульного с паровым пространством — 5…6 кг). При минимальных нагрузках по парам клапаны работают в динамическом режиме. При увеличении нагрузки клапаны приподнимаются в пределе до упора ограничителей и начинается эжекция жидкости над клапанами, что способствует более интенсивному перемешиванию жидкости в надклапанном пространстве. Распределительный выступ на клапане при остановке колонны способствует полному стоку жидкости с тарелки. Опытно-промышленные испытания показали высокие эксплуатационные их достоинства: устойчивость и равномерность работы в широком диапазоне нагрузок без уноса жидкости; исключительно высокий КПД (≈ 80…100 %), высокая производительность, превышающая на ≈ 20 % производительность колпачковых тарелок, и т. д.
Среди известных в настоящее время конструкций клапанных тарелок с перекрестным движением фаз особое место занимает тарелка, разработанная фирмой " Glitsch", с дисковыми клапанами V-1, у которых направляющие с нижними ограничителями подъема штампуются заодно с клапаном и отгибаются затем под углом 90°. Края клапана несколько отогнуты вниз, что повышает локальную скорость газа при выходе его из-под клапана. Эти тарелки многие годы успешно эксплуатируются в промышленности и хорошо себя зарекомендовали.
а — дисковый клапан фирмы " Nutter"; б — дисковый клапан фирмы " Sulzer"; в — трапециевидный клапан ВНИИнефтемаша; г — балластный клапан V-4 фирмы " Glitsch"; д — балластный клапан ВНИИнефтемаша; е — прямоточный клапан РГУ нефти и газа им. И.М. Губкина; 1 — полотно тарелки; 2 — клапан; 3 — коническое углубление; 4 — направляющие; 5 — ограничители вертикального подъема; 6 — ограничители начального зазора; 7 — балласт; 8 — специальный ограничитель подъема; 9 — рычаг; 10 — болт; 11 — отверстия в клапане; 12 — козырьки
На рис. 2.24, а представлена конструкция тарелки с дисковыми клапанами, являющаяся дальнейшим усовершенствованием клапана V-1. В отверстиях полотна 1 тарелки установлены дисковые клапаны 2, которые центрируются тремя, расположенными под углом 120°, направляющими 4, имеющими нижние ограничители подъема 5. Начальный зазор между кромкой диска клапана и полотном тарелки получают при помощи ограничителей 6. Для уменьшения гидравлического сопротивления в центре клапана выполнено коническое углубление 3, направленное навстречу потоку пара, что обеспечивает плавное обтекание паровым потоком диска клапана. При сборке клапанных тарелок в зависимости от диаметра аппарата на полотне одной тарелки устанавливают от нескольких десятков до нескольких тысяч клапанов Существует тарелка с трапециевидными клапанами (рис.2.24, в), у которых меньшее основание трапеции обращено в сторону слива жидкости. С целью повышения производительности тарелки, увеличения поверхности контакта фаз и расширения диапазона устойчивой работы разработаны балластные клапанные тарелки (рис. 2.24, г). При малых нагрузках по пару тарелка работает как обычная с дисковыми клапанами меньшей массы. При увеличении нагрузки дисковый клапан упирается в балласт и работает совместно с ним как один утяжеленный клапан. Такая конструкция позволяет расширить диапазон саморегулирования и уменьшить сопротивление тарелки(на 10…15 %), особенно при низких нагрузках по пару. Представляет интерес конструкция прямоточной клапанной тарелки с групповым балластом (рис. 2.24, д). На рис. 2.25 представлена конструкция прямоточной клапанной тарелки с перфорированными клапанами, в которой выгодно сочетаются повышенная производительность прямоточных клапанных тарелок и высокая эффективность ситчатых тарелок. В отверстиях горизонтального полотна 1 установлены пластинчатые клапаны 2, имеющие отверстия с козырьками 12, высота которых увеличивается в сторону открытия клапанов.
Рис. 2.25 Элемент ситчато-клапанной тарелки При небольших нагрузках пар проходит через отверстия в клапанах и тарелка работает всем сечением как обычная ситчатая. В области повышенных газовых нагрузок одна часть парового потока выходит из-под клапанов в прямотоке с жидкостью, а другая направляется козырьками в отверстия клапанов. Струйные тарелки. У струйных тарелок контактные элементы (просечки, лепестки и т. п.) расположены таким образом, что пар, выходящий в жидкость под некоторым углом к горизонту, приобретает горизонтальную составляющую скорости, совпадающую с направлением движения жидкости по тарелке или под некоторым углом к нему. Благодаря этому можно создать наиболее благоприятные условия для эффективного контакта фаз при высокой производительности контактного устройства. При чисто прямоточном движении фаз и большой скорости пара происходит снос жидкости в направлении сливного кармана, что затрудняет работу переливного устройства и приводит к снижению эффективности работы тарелки. Чтобы избежать этого, прибегают к различным приемам, позволяющим локализировать (скомпенсировать) прямоточное движение фаз и не допустить его распространения на всю тарелку, примером может служить установка поперечных секционирующих перегородок (рис. 2.26, б и д), создание движения фаз в пересекающихся направлениях, когда оси соседних лепестков расположены во взаимно перпендикулярном направлении или образуют пучок прямых (рис. 2.26, в и г) и т.п.
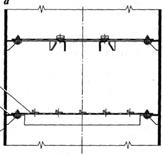
Рис. 2.26. Схема струйно-направленной тарелки с вертикальными поперечными секционирующими перегородками: а — общий вид; б — схема контактной зоны; в — ввод части потока пара поперек потока жидкости; г — ввод части потока пара под углом к потоку жидкости; д — установка поперечных перегородок в форме гребенки: 1 — корпус колонны; 2 — полотно тарелки; 3 — приемный карман; 4 — стенка переливного кармана; 5 — подпорная перегородка; 6 — лепесток (язычок); 7 — вертикальная перегородка; 8 — сливная перегородка; 9 — прорезь в вертикальной перегородке Тарелки провального типа (рис. 2.27) перекрывают все сечение колонны и состоят из отдельных секций, укрепленных на опорном кольце и балках каркаса. Для прохода паровой и жидкой фаз выполнены отверстия или прорези, площадь которых составляет от 10 до 30 % площади всей тарелки. На тарелках провального типа паровая и жидкая фазы контактируют по схеме противотока, благодаря чему происходит интенсивное перемешивание жидкости по всей высоте контактной зоны.
 г г
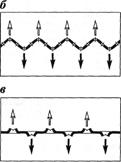
Рис. 2.27. Схемы тарелок провального типа: а — решетчатая тарелка; б — ситчатая волнистая тарелка; в — решетчатая тарелка с отогнутыми кромками щелей; г — ситчатая Пар и жидкость проходят через одни и те же каналы, при этом места стока жидкости и прохода паров случайным образом перемещаются по площади тарелки. Тарелки этого типа гораздо более чувствительны к изменению нагрузок по жидкости и пару и имеют более узкий диапазон рабочих нагрузок, чем тарелки со специальными переливными устройствами. При небольшой паровой нагрузке напор паров недостаточен для образования слоя жидкости на тарелке. При больших паровых нагрузках сопротивление течению жидкости через отверстия тарелки становится столь значительным, что пена заполняет практически все межтарельчатое пространство и нормальный переток жидкости с тарелки на тарелку нарушается. При этом резко возрастает гидравлическое сопротивление потоку паров. Такой режим работы называется захлебыванием и определяет предельные паровую и жидкостную нагрузки колонны. Стандартные провальные решетчатые тарелки диаметром 1000 — 3000 мм имеют ширину прямоугольных прорезей 6X60 мм, шаг от 10 до 36 мм. На двух смежных тарелках прорези выполняют во взаимно перпендикулярных направлениях. На рис. 2.27, а показан прогрессивный вариант изготовления решетчатой провальной тарелки, когда край полотна отгибается и выполняет роль несущей балки. Такая конструкция применяется при переработке коррозионных продуктов и позволяет изготовить полотно и опорные конструкции из легированной стали. Ситчатые тарелки с отбойниками имеют относительно низкое гидравлическое сопротивление, повышенную производительность, но более узкий рабочий диапазон по сравнению с колпачковыми тарелками. Применяются преимущественно в вакуумных колоннах. Для увеличения производительности и эффективности провальных тарелок за счет более равномерного распределения потоков по сечению колонны применяют ситчатые волнистые тарелки (рис.2.27, б), решетчатые тарелки с отогнутыми кромками щелей (рис. 2.27, в). Оценка конструкций тарелок При оценке конструкций тарелок обычно принимают во внимание следующие показатели: производительность; гидравлическое сопротивление; эффективность рабочих нагрузках; диапазон рабочих нагрузок в условиях достаточно высокой эффективности; сопротивление одной теоретической тарелки при различных рабочих нагрузках; простоту конструкции, проявляющуюся в трудоемкости изготовления, монтажа, ремонтов; металлоемкость. Важной характеристикой тарелки является диапазон рабочих нагрузок n = Wmax/Wmin где Wmax и Wmin — максимальная и минимальная допустимые скорости пара в колонне. Чем больше величина п, тем большие колебания нагрузок по жидкой и паровой фазам можно допустить в условиях эксплуатации аппарата с тем или иным типом контактных устройств. На рис. 2.28 показана область устойчивой работы контактных тарелок с переливными устройствами. Максимально допустимая скорость пара в колонне (линия ВС) определяется величиной допустимого уноса жидкости, которая обычно принимается равной 10%. Линия AD определяет минимально допустимые скорости пара, соответствующие 10 % провалу жидкости. Справа область устойчивой работы ограничена линией CD, которая соответствует максимальным нагрузкам по жидкости, соответствующим 85 % режима «захлебывания». Линия АВ определяет минимальные нагрузки по жидкости, при которых на тарелке обеспечивается устойчивый барботажный слой и отсутствует «проскок» пара. Нагрузки по пару и жидкости, соответствующие координатам любой точки внутри области, обеспечивают устойчивую работу аппарата.
W
О Lраб L Рис. 2.28. Область устойчивой работы тарелки с переливными устройствами
Линия ОМ, соединяющая рабочую точку N с началом координат, называется рабочей линией процесса. Пересечение рабочей линии ОМ с прямыми, ограничивающими область устойчивой работы тарелки, позволяет определить максимальную и минимальную допустимую скорость пара в колонне. Построение области устойчивой работы тарелки является одним из основных этапов гидравлического расчета тарелки. В инженерных методиках расчета используются эмпирические зависимости для построения области устойчивой работы, полученные при исследовании контактных устройств на экспериментальных стендах и модельных системах.
Насадочные колонны Насадочные колонны применяются преимущественно в малотоннажных производствах и при необходимости проведения массообменных процессов с малым перепадом давления. Благодаря созданию в последние годы новых типов насадок, позволяющих значительно снизить задержку жидкости в контактной зоне и гидравлическое сопротивление аппарата, создались перспективы применения их для многотоннажных производств (вакуумная ректификация мазута, газоразделение и др.). Основными конструктивными характеристиками насадки являются ее удельная поверхность и свободный объем. Удельная поверхность насадки f — это суммарная поверхность насадочных тел в единице занимаемого насадкой объема аппарата. Удельную поверхность обычно измеряют в м2/м3. Чем больше удельная поверхность насадки, тем выше эффективность колонны, но ниже производительность и больше гидравлическое сопротивление. Под свободным объемом насадки е понимают суммарный объем пустот между насадочными телами в единице объема, занимаемого насадкой. Свободный объем измеряют в м3/м3. Чем больше свободный объем насадки, тем выше ее производительность и меньше гидравлическое сопротивление, однако при этом снижается эффективность работы насадки. Конструкции насадок, применяемых в промышленных аппаратах нефтегазопереработки и нефтехимии, можно разделить на две группы — нерегулярные (насыпные) и регулярные насадки. В зависимости от используемого для изготовления насадки материала они разделяются на металлические, керамические, пластмассовые, стеклянные, стеклопластиковые и др. По способу изготовления элементы насадки бывают штампованные, литые, прокатанные, полученные методом экструзии и т. п. На эффективность работы насадки в значительной степени влияет смачиваемость жидкостью поверхности элементов насадки. Для улучшения смачиваемости элементов насадки их зачастую подвергают специальной обработке, создают искусственным путем шероховатости или делают на поверхности просечки, выступы и т. д.
К насадкам предъявляются следующие основные требования: 1. большая удельная поверхность; 2. хорошая смачиваемость жидкостью; 3. малое гидравлическое сопротивление; 4. равномерность распределения жидких и газовых (паровых) потоков; 5. высокие химическая стойкость и механическая прочность; 6. низкая стоимость.
Насадок, полностью удовлетворяющих всем указанным требованиям, не существует, поскольку некоторые из требований противоречивы, например, пункты 1 и 3. При нормальной эксплуатации насадочных колонн массообмен происходит в основном в пленочном режиме на смоченной жидкостью поверхности насадок. Естественно, чем больше удельная поверхность насадки, тем эффективнее массообменный процесс. Однако насадки с высокой удельной поверхностью характеризуются повышенным гидравлическим сопротивлением. В химической промышленности и нефтегазопереработке применяют разнообразные по форме и размерам насадки, изготавливаемые из различных материалов (керамика, фарфор, сталь, пластмассы и др.)
а б в г д е Рис. 2.29 Типы насадок: кольца: а — Рашига; б — Лессинга; в — Паля; седла: г — Берля; д — «Инталлокс»; ситчатые и из перфорированного металлического листа: е — «Спрейпак», ж — Зульцер; з — Гудлоу; и — складчатый кубик; к — Перформ-Грид Рис 2.33 Конструкции регулярных насадок а – Меллапак б- Инталлокс, в- Ваку-Пак, г- Панченкова Конструкция блочной регулярной насадки Инталлокс, разработанная фирмой " Norton", представлена на рис. 2.33, б и образована из стальных гофрированных листов. Каждый лист при гофрировании делится на несколько участков (на рис. 2.33, б три участка) с отгибкой металла в противоположные стороны. В местах перехода выполняются просечки, что способствует эффективному обновлению поверхности массообмена. Насадка Ваку-пак разработана совместно ВНИИнефтемашем и фирмой " Apparate-und Anlagenbau Germania" (рис. 2.33, в). Она образована из вертикальных гофрированных пластин, изготовленных из просечно-вытяжного листа. Поверхность пластин имеет арочные просечки, направленные вниз и ориентированные в противоположные стороны с обеих сторон пластин. За счет этих просечек обеспечивается зазор в 20 мм между соседними гофрированными пластинами. Такая насадка имеет удельную поверхность 115 м2/м3, свободный объем 98 % и объемную массу 150 кг/м3. При разработке массообменных аппаратов с использованием регулярной насадки необходимо индивидуальное проектирование выбранного типа насадки для данной колонны. Для этого слой насадки разбивают на отдельные блоки с учетом изменения кривизны стенки колонн разного диаметра. В колоннах диаметром до 1 м регулярная насадка монтируется одним блоком через верхнее съемное днище. Высота всех блоков регулярных насадок составляет около 400 мм, максимальная ширина принята с учетом размеров люка-лаза. На современных НПЗ вакуумные колонны установок перегонки нефти оснащены регулярными насадками, что позволяет обеспечить глубокий вакуум в колоннах и существенно увеличить отбор вакуумного газойля и достичь температуры конца кипения до 600 °С. АБСОРБЦИЯ И ДЕСОРБЦИЯ Рис. 3.3. График для расчета процесса абсорбции (десорбции) многокомпонентной смеси При абсорбции сухих газов количество извлекаемых компонентов невелико, что позволяет пользоваться формулой Кремсера 3.5 Процесс десорбции При десорбции поглощенные компоненты газовой смеси должны быть вновь переведены в газообразное состояние. Для этого обычно снижают парциальное давление углеводородов при вводе водяного пара либо повышают температуру насыщенного абсорбента и подводят тепло в нижнюю часть десорбера (рисунок 18.4). В последнем случае десорбер можно рассматривать как отгонную часть ректификационной колонны. Чтобы компонент мог перейти из жидкости в газовую фазу, его парциальное давление в жидкости должно быть выше равновесного. Соответственно и концентрация компонента в жидкой фазе будет больше равновесной. Следовательно рабочая линия буде ниже равновесной (рисунок 18.5)
Рис. 3.4 Графический расчет числа теоретических тарелок в десорбере: АВ — рабочая линия; ОС — кривая равновесия фаз
Для расчета многокомпонентной десорбции используют уравнение Кремсера.:
где /-степень извлечения при десорбции, m число теоретических тарелок, K константа фазового равновесия. Анализ этой формулы оказывает, что при S = const, чем больше m, тем больше . Если уменьшить давление в системе, то К увеличится ( При нагревании системы К увеличится и доля извлечения тоже увеличивается. При заданной степени извлечения при десорбции и десорбционном факторе определяют число теоретических тарелок. Эта формула верна при отпаривании малых порций газа. Конструкции абсорберов Абсорберы разделяют по способу контактирования взаимодействующих фаз на три группы: поверхностные, барботажные и распыливающие, В поверхностных абсорберах поверхностью контакта фаз является зеркало жидкости а — или поверхность стекающей пленки (пленочные абсорберы). К этой группе относятся аппараты со свободной поверхностью; насадочные с насыпной и регулярной насадкой; пленочные, в которых пленка образуется при гравитационном стекании жидкости внутри вертикальных труб или на поверхности листов; механические пленочные с пленкой, формирующейся под действием центробежных сил. В барботажных абсорберах поверхность контакта развивается потоками газа, распределяющегося в жидкости в виде пузырей и струй. К этой группе относятся аппараты со сплошным барботажным слоем с непрерывным контактом между фазами, тарельчатого типа, с подвижной (плавающей) насадкой, с механическим перемешиванием жидкости. В распыливающих абсорберах поверхность контакта образуется путем распыления жидкости на мелкие капли. К этой группе относятся аппараты полые форсуночные, с распылением за счет энергии жидкости, скоростные прямоточные с распылением абсорбента за счет кинетической энергии движущегося с большой скоростью газового потока, механические с распылением жидкости быстро вращающимися элементами. Отдельные типы аппаратов в зависимости от режима работы могут быть отнесены к одной или другой группе, например, насадочные абсорберы при инверсии фаз становятся барботажными аппаратами, а тарельчатые при работе в струйном режиме являются распиливающими. Важными характеристиками, которые необходимо учитывать при выборе конструкции абсорбера, также являются гидравлическое сопротивление, диапазон возможного изменения нагрузок по газу и жидкости, время пребывания жидкости, чувствительность и склонность к загрязнениям. В нефтегазовых производствах наиболее распространены тарельчатые и насадочные абсорберы. Тарельчатый абсорбер (рис. 3.5, а) представляет собой вертикальный аппарат, в верхней части корпуса 1 которого установлен каплеотбойник 2, предотвращающий унос абсорбента потоком газа. Контактирование газового потока и абсорбента осуществляется на контактных тарелках 3 той или иной конструкции. Для ремонта и монтажа внутренних устройств абсорбера через 4 — 5 тарелок установлены люки-лазы 4 условным диаметром не менее 450 мм. В нижней части корпус аппарата приварен к опорной обечайке 5. Насадочный абсорбер (рис. 3.5б) в верхней части оснащен распределителем 2 регенерированного абсорбента. Слой насыпной или регулярной насадки опирается на опорную решетку 4. Для загрузки и выгрузки насадки служат люки 5 и 7.
Рис.3.5 Схемы тарельчатого и насадочного абсорберов а-тарельчатый: 1 — корпус; 2 — каплеотбойник; 3 — тарелка; 4 — люк; 5 — опорная обечайка; б — насадочный: 1 — корпус; 2 — распределительная тарелка; 3 — насадка; 4 — опорная решетка; 5 — загрузочные люки; б — опора; 7 — люки выгрузки насадки. Потоки: / — ненасыщенный абсорбент; 11 — сухой газ; 111 — сырой газ; IV — насыщенный абсорбент Обычно давление в абсорберах при разделении нефтяных попутных газов составляет 1, 6 — 2, 0 МПа, а при извлечении компонентов природного газа, имеющего большее устьевое давление, 4, 0 — 7, 5 МПа. Температура зависит от применяемого хладагента и может составлять при извлечении пропана минус 40 °С, этана минус 80— 100 °С. Диаметр промышленных абсорберов зависит от производительности и достигает 3 м, число тарелок составляет 30 — 40. При промысловой очистке и осушке природного газа производительность по газу одного абсорбера достигает 10 — 35 млн. м3/сут. Для таких условий работы предназначены специальные конструкции абсорберов. На рис 3.6 представлена конструкция многофункционального аппарата, состоящего из трех секций. Исходный газ по тангенциально расположенному штуцеру поступает в первую по ходу газа секцию сепарации. Отделение капельной жидкости в этой секции осуществляется при прохождении газа через сетчатый отбойник 1 и сепарационную тарелку 2, на которой установлены центробежные сепарирующие элементы. Вторая секция предназначена для осушки газа и включает четыре тарелки 4 с контактными элементами центробежного типа.
Каждый прямоточный центробежный элемент состоит из цилиндрического корпуса 12 диаметром 60— 100 мм и оснащен в нижней части тангенциальным завихрителем 17. На небольшом расстоянии от полотна тарелки 11 центробежный элемент оснащен трубкой 15, служащей для подачи жидкости в центр элемента. При контакте с закрученным потоком газа жидкость распределяется по стенке элемента и поднимается вверх.
3.6 Конструкция многофункционального аппарата для очистки и осушки природного газа: 1 — сетчатый отбойник; 2, 5 — сепарационная тарелка; 3 — внутренняя емкость насыщенного гликоля; 4 — тарелка с контактными элементами центробежного типа; 6 — фильтр-патроны; 7 — люк-лаз; 8, 10 — штуцер для дренажа; 9 — штуцер отвода жидкости; 11 — полотно тарелки; 12 — цилиндрический корпус центробежного элемента; 13 — отбойник; 14 — коническая чашка; 15 — трубка для подачи жидкости; 16 — отверстие; 17 — тангенциальный завихритель. Потоки: / — сырой газ; II — насыщенный раствор гликоля; III — сухой газ; IV — регенерированный раствор гликоля Благодаря уменьшению давления внутри элементов жидкость по трубке 15, имеющей отверстие 16 в нижней части, подается внутрь элемента. Насыщенный гликоль собирается во внутренней емкости 3, откуда он отводится на регенерацию. Последняя по ходу газа секция улавливания гликоля образована сепарационной тарелкой 5 и тарелкой, на которой установлены фильтр-патроны б. Фильтр-патроны выполнены в виде перфорированного цилиндрического каркаса с намоткой 10—15 слоев стекловолокна. Изнутри и снаружи слой фильтрующего материала закреплен двумя-тремя слоями рукавной сетки.
ЭКСТРАКЦИЯ Требования к экстрагентам 1. Высокая селективность 2. Нормальная растворяющая способность 3. Большая разность плотностей в зоне вывода экстрактного раствора ( +0, 2) 4. Большая разность температур кипения для экстрагента и и сырьевых компонентов ( 70оС +), что облегчает выделение циркулирующего экстрагента 5. Большое значение коэффициента поверхностного натяжения, чтобы избежать образования стойкой эмульсии 6. Химическая стойкость 7. Малая теплота испарения, если регенерация экстрагента идет ректификацией 8. Малая токсичность 9. Низкая температура застывания Рис. 4.2. Треугольная диаграмма Любая смесь трех компонентов отвечает точке внутри треугольника (например, точка N), двойная смесь отвечает точке на сторонах треугольника. Например, смесь компонентов А и В представлена точкой F на стороне АВ. Вершины треугольника соответствуют концентрациям чистых компонентов. 4.4 Кривая равновесия фаз на треугольной диаграмме Для расчета процесса экстракции с применением треугольной диаграммы необходимо располагать кривой равновесия фаз, определяющей составы фаз, образующихся при расслаивании системы.
На поле треугольной диаграммы отложена бинодальная кривая, отвечающая равновесным рафинатным м экстрактным растворам. Прямая RS, связывающая точки равновесных составов на бинодальной кривой, называется конодой. Коноды не параллельны одна другой.
Рис. 4.3 Бинодальная (равновесная) кривая Рис. 4.4 Бинодальные кривые, Диаграмме При значительном разбавлении раствора компонентом В взаимная растворимость компонентов настолько возрастает, что образуется гомогенный раствор, характеризуемый точкой К. Эту точку называют критической. При дальнейшем увеличении концентрации компонента В в растворе он будет оставаться гомогенным. Любая точка, например N, лежащая внутри контура, ограниченного бинодальной кривой, отвечает двухфазной системе, тогда как любая точка, находящаяся вне этого контура, характеризует однофазную систему (гомогенный жидкий раствор). Если взять смесь трех компонентов, определяемую точкой N, то такая система образует два расслаивающихся раствора (две равновесные жидкие фазы), составы которых после расслаивания характеризуются точками R и S, находящимися на пересечении коноды, проходящей через точку N, с нижней и верхней ветвями бинодальной кривой. Нижняя ветвь бинодальной кривой соответствует небольшим концентрациям компонента L (растворителя), что характеризует рафинатные растворы Rf. Верхняя ветвь бинодальной кривой отвечает высоким концентрациям компонента L и характеризует экстрактные растворы S,. Треугольная диаграмма обладает следующим основным свойством, которое вытекает из материальный баланса смешения. Если при смешении двух систем R и S получается новая система N, то точка характеризующая все три системы, располагается на одной прямой. При этом точка N располагается между точками R и S на расстояниях, обратно пропорцинальноых массам ( объемам) исходных систем R и S, т.е. SR отрезок пропорционален массе системы N, отрезок NR - массе системы S, а отрезок NS - массе системы S
где gR и gs — соответственно количество рафинатного и экстрактного раствора. Каждая бинодальная кривая отвечает определенной температуре и может быть построена на основании экспериментальных данных. При изменении растворимости с изменением температуры бинодальная кривая будет менять свое положение. Поскольку в большинстве случаев взаимная растворимость компонентов повышается с увеличением температуры, область существования расслаивающихся систем сокращается. При некоторой температуре Ткр, называемой критической, компоненты, входящие в состав трехфазной системы, будут полностью растворяться друг в друге, образуя гомогенный жидкий раствор. На рис. 4.4 приведены бинодальные кривые для нескольких температур при условии tx < t2 < t3 < Т Kp.
4.5 Расчет однократной экстракции на треугольной диаграмме Исходное сырье – смесь компонентов А и В отвечает точке F. Проведем однократную экстракцию. Если концентрация растворителя в смеси будет xLN, то получим точку N, на пересечении этой горизонтали с прямой FL, смеси сырья F и растворителя L находятся на прямой FL. Через точку N проводим коноду RS, которая определяет точки R– рафинатного и S-экстрактного растворов. При удалении растворителя из экстрактного раствора S получаем экстракт Э. Точка Э лежит на пересечении прямой LS со стороной АВ треугольника. Аналогично на пересечении прямой LR со стороной АВ определяем точку Р, характеризующую состав получаемого рафината. Концентрации растворителя в экстрактном xLS и рафинатном xLR растворах определяются горизонтальными линиями, проведенными из точек S и R до пересечения со стороной АL треугольника.
Рис. 4.5 Расчет однократной экстракции на треугольной диаграмм
АДСОРБЦИЯ Сущность процесса адсорбции Процесс поглощения газов (паров) или жидкостей поверхностью твердых тел (адсорбентов) называется адсорбцией. Явление адсорбции связано с наличием сил притяжения между молекулами адсорбента и поглощаемого вещества. В промышленности адсорбцию применяют для отбензинивания попутных и природных газов, при разделении газов нефтепереработки для получения водорода и этилена, осушки газов и жидкостей, выделения низкомолекулярных ароматических углеводородов, для очистки масел. Явление адсорбции используется в хроматографии, в противогазах. По сравнению с другими массообменными процессами адсорбция наиболее эффективна в случае малого содержания извлекаемых компонентов в исходной смеси и поэтому адсорбцию обычно используют на конечных технологических стадиях процессов. Различают физическую и химическую адсорбцию (хемосорбцию). При физической адсорбции молекулы адсорбента и поглощаемого вещества не вступают в химическое взаимодействие. При хемосорбции имеет место химическое взаимодействие молекул поглощаемого вещества с адсорбентом. При этом физическая адсорбция всегда обратима, а хемосорбция может быть необратимой. Для процессов хемосорбции характерны закономерности химических реакций ( осуществляется со значительной энергией активации, экзо - или эндотермический эффект реакции, с повышением температуры ее скорость возрастает по закону Аррениуса, и др.) Физическая адсорбция процесс экзотермический, т.е. идет с выделением тепла. Для газов и паров величина теплоты адсорбции мала и примерно равна теплоте их конденсации. Исчерпание адсорбционной способности — проскок определяет время защитного действия адсорбента по отношению к данному компоненту. Количество вещества, адсорбируемого поверхностью, определяется состоянием равновесия и зависит от природы адсорбента и адсорбируемого вещества, концентрации последнего в исходной смеси, температуры процесса, а при адсорбции газовой фазы и от давления. Адсорбируемость углеводородов обычно возрастает с увеличением их молекулярной массы, однако более значительное влияние оказывают структура и размеры их молекул. Так, парафиновые и нафтеновые углеводороды поглощаются в меньшей степени, чем ароматические. Для ароматических углеводородов адсорбируемость возрастает с увеличением числа циклов в молекуле. Сернистые соединения лучше сорбируются, чем содержащие их парафиновые и нафтеновые углеводороды, и имеют близкую адсорбируемость к ароматическим углеводородам. Это затрудняет отделение сернистых соединений от ароматических путем адсорбции. Кислородные, смолистые и особенно азотистые органические соединения, содержащиеся в нефтях и нефтепродуктах, отличаются значительно более высокой адсорбируемостью, чем углеводороды, и отделение этих веществ от углеводородной смеси происходит сравнительно легко. Непредельные низкомолекулярные углеводороды (этилен, пропилен) адсорбируются лучше, чем соответствующие предельные их аналоги (этан, пропан). Адсорбируемость более высокомолекулярных непредельных углеводородов изучена недостаточно. Использование адсорбции для разделения смесей, содержащих непредельные углеводороды, в ряде случаев осложняется тем, что в процессе разделения эти углеводороды подвергаются каталитическому воздействию адсорбента, в связи с чем могут происходить их химические превращения, например полимеризация. Некоторые адсорбенты, например активированный уголь, преимущественно адсорбируют углеводороды, имеющие более высокую температуру кристаллизации, вследствие чего используются для депарафинизации жидких нефтепродуктов 5.2 Характеристики адсорбентов Адсорбенты пористые твердые вещества с сильно развитой поверхностью пор. Удельная поверхность пор может составлять от 200 до 1000 м2 / г, а средний радиус пор от 0, 2 до 10 нм. Адсорбенты применяют в виде таблеток или шариков размером от 2 до 6 мм, а также порошков размером от 20 до 500 мкм. В качестве адсорбентов используют активированный уголь, алюмосиликаты, цеолиты и др. Цеолиты (молекулярные сита) - синтетические адсорбенты с регулируемым размером пор, представляющий собой алюмосиликаты натрия и калия. Синтетические адсорбенты активнее, но значительно дороже природных. В качестве адсорбентов используются активированный уголь, силикагель, алюмосиликаты, цеолиты и др. Цеолиты или молекулярные сита — синтетические или природные адсорбенты с регулярной структурой пор, представляющие собой алюмосиликаты натрия, калия или других элементов. Название произошло от сочетания двух греческих слов «цео» и «лит», т.е. «кипящие камни». Это объясняется тем, что заполняющая поры цеолитов вода при нагревании выделяется, т. е. цеолиты как бы «кипят». Общая химическая формула Ме2/пО А1203 xSi02 уН20, где Me — катион щелочного металла; п — его валентность. В качестве катионов в состав природных цеолитов обычно входят натрий, калий, кальций, реже магний, барий, стронций. Кристаллическая структура цеолитов образована тетраэдрами Si04 и А104. В качестве природных цеолитов используют различные минералы: содалит, шабазит, морденит, фожазит и др. Синтетические цеолиты имеют строение и геометрическую структуру, аналогичные природным цеолитам. Аналогами фожазита являются синтетические цеолиты типа X и Y. Различают синтетические цеолиты типов А, X и Y. Цеолиты типа А относятся к низкокремнистым формам: в них отношение Si02: Al203 не превышает 2. Цеолиты типа X имеют мольное отношение Si02: Al203, которое может изменяться от 2, 2 до 3, 3. Цеолиты типа Y характеризуются вышеупомянутым соотношением в пределах от 3, 1 до 6. При увеличении этого показателя повышается кислотостойкость цеолитов. Размеры входных окон, определяющих избирательность цеолитов, изменяются от 3 до 9 А.
Важной характеристикой адсорбентов является их активность, под которой понимают массу адсорбированного вещества на единицу массы адсорбента в условиях равновесия:
где l масса поглощенных компонентов, g масса адсорбента. По отношению к разным компонентам смеси активность адсорбента различна. Так, парафиновые и нафтеновые углеводороды поглощаются в меньшей степени, чем ароматические, непредельные и гетероатомные углеводороды (содержащие атомы S, N, O). С увеличением размера молекул (молекулярной массы) сорбируемость молекул обычно возрастает. Адсорбенты характеризуются также временем защитного действия, под которым понимают промежуток времени, в течение которого концентрация поглощаемых компонентов на выходе из слоя адсорбента не изменяется. При большем времени работы адсорбента происходит проскок поглощаемых компонентов, связанный с исчерпанием активности адсорбента. В этом случае необходима регенерация адсорбента. В адсорберах периодического действия также имеет место износ адсорбента в результате давления вышележащего слоя адсорбента и условий десорбции. Из этих соображений высоту насыпного слоя в периодических адсорберах принимают обычно не более 3 м.
Изотерма адсорбции Равновесие при адсорбции характеризуется определенной зависимостью между активностью адсорбента и парциальным давлением или концентрацией вещества в смеси. Состояние равновесия описывается уравнением Лэнгмюра:
и Фрейндлиха:
где с- концентрация или парциальное давление адсорбируемого вещества; а- активность (емкость) адсорбента, А1, А2, b, d коэффициенты и показатель степени, зависящие от природы адсорбента, адсорбируемого вещества и температуры. Приведенные уравнения называются уравнениями изотермы адсорбции (рисунок 20.1).
С Р ис. 5.1 Общий вид изотермы адсорбции при разных температурах
Процесс адсорбции состоит из двух стадий: поглощения вещества поверхностью адсорбента и диффузии вещества в порах адсорбента. При адсорбции сначала поглощаются все компоненты смеси, однако после достижения состояния насыщения будет происходить обратный процесс- вытеснение молекул с меньшей степенью активности. Поэтому в слое адсорбента компоненты располагаются послойно по мере уменьшения активности. При десорбции компоненты выходят в обратном порядке. Это используется в препаративной и аналитической хроматографии. Процессу адсорбции способствуют более низкие температуры, адсорбент для газов - повышенное давление. При удалении адсорбированных компонентов из адсорбента (при десорбции), наоборот, следует повышать температуру и понижать давление для газовых смесей. В общем случае твердые частицы адсорбента имеют поры различного размера и формы, поэтому перенос вещества внутри гранул адсорбента может осуществляться одновременно различными способами. Во многих случаях изменение активности адсорбента во времени удовлетворительно описывается следующим уравнением:
где аτ , а — активность адсорбента в момент времени τ и при равновесии (τ → ∞ ); Ка — константа скорости адсорбции. Константа скорости адсорбции Ка зависит от температуры и концентрации адсорбируемого компонента. С увеличением температуры скорость достижения равновесного состояния возрастает, при этом величина активности в условиях равновесия будет меньше, чем при более низкой температуре. Типичные кинетические кривые адсорбции приведены на рис. 5.2.
0 τ Р ис. 5.2 Кинетические кривые адсорбции при разных температурах 5.4 ДЕСОРБЦИЯ Для выделения поглощенных при адсорбции компонентов с целью направления их на дальнейшую переработку применяется процесс десорбции. В тех случаях, когда в газовом потоке или в растворе, проходящем через слой адсорбента, концентрации (парциальные давления) адсорбируемых компонентов ниже равновесных, данные компоненты будут покидать поверхность адсорбента и переходить в газовый (жидкостный) поток, т. е. десорбироваться. Это будет происходить до тех пор, пока не установится новое состояние равновесия. На промышленных адсорбционных установках необходимо производить регенерацию адсорбента с целью восстановления его адсорбционной способности. Поэтому после окончания стадии адсорбции осуществляется стадия десорбции поглощенных компонентов из адсорбента. Десорбция облегчается с повышением температуры и увеличением расхода десорбирующего агента. Десорбция газообразных и легколетучих компонентов облегчается при понижении давления в системе. В результате десорбции адсорбционная способность адсорбента может восстанавливаться полностью или частично в зависимости от адсорбционной способности десорбируемых компонентов, выбранного метода десорбции, рабочих параметров процесса. В ряде случаев оправдано неполное восстановление активности адсорбента, так как при этом сокращаются эксплуатационные затраты. Зависимость активности адсорбента а (по отношению к первоначальной его активности а0) от числа регенераций N представлена на рис.5.3. Приведенная кривая показывает, что наибольшее снижение активности адсорбента наблюдается после первой регенерации. В дальнейшем активность снижается постепенно и в меньшей степени. Такой характер восстановления активности адсорбента объясняется тем, что при регенерации часть его активной поверхности остается занятой адсорбированными компонентами и в дальнейшем исключается из участия в процессе адсорбции. При использовании в качестве десорбирующих агентов полярных растворителей активность адсорбента восстанавливается наиболее полно. При окислительной регенерации активность адсорбента восстанавливается практически полностью. Температурный режим окислительной регенерации для силикагелей обычно 300 + 350 оС, для алюмосиликатов 600 + 650 оС. Недопустим перегрев адсорбента, так как это вследствие спекания пор адсорбента приводит к снижению или полной потере его активности
а/а0 N
Р ис. 5.3 Характер восстановления активности адсорбента при регенерациях
5.5 Методы осуществления процесса адсорбции В промышленности применяют следующие варианты процесса адсорбции: 1. с неподвижным слоем адсорбента; 2. с псевдоожиженным слоем адсорбента. 3. с движущимся слоем адсорбента;
5.5.1 Адсорберы с неподвижным слоем адсорбента Адсорберы с неподвижным слоем адсорбента представляют собой вертикальные аппараты, заполненные гранулированным адсорбентом. В промышленной практике общая высота слоя адсорбента предопределяется необходимым его объемом и величиной гидравлического сопротивления слоя адсорбента; обычно она составляет от 2 до 12 м. После насыщения адсорбента стадия адсорбции прекращается, и адсорбент должен быть регенерирован. Для регенерации через слой насыщенного адсорбента пропускают водяной пар, инертный газ, растворитель и др. Иногда регенерацию адсорбента проводят, выжигая поглощенные компоненты в специальном аппарате. Адсорбент представляет собой зерна неправильной формы размером 2-10 мм. Неподвижный режим адсорбента используют для предотвращения разрушения его.
Рис. 5.4. Распределение концентраций в потоках, покидающих адсорбер по высоте стационарного слоя адсорбента
5.5.2 Адсорберы с псевдоожиженным слоем адсорбента Адсорберы с псевдоожиженным слоем адсорбента позволяют также осуществлять непрерывный процесс адсорбции. В этом случае в качестве адсорбента используются мелкие гранулы (обычно не более 500 мкм). Адсорбер должен иметь несколько слоев для уменьшения возможности проскока газов через слой адсорбента. Газ движется противотоком вверх. Конструктивно адсорбер может иметь один или несколько кипящих слоев (рис. 5.5), обеспечивающих контакт фаз в противотоке (ступенчато-противоточный адсорбер). В таком адсорбере на специальных контактных устройствах (тарелках) осуществляется взаимодействие между газом и порошкообразным адсорбентом, в результате чего адсорбент переводится в состояние псевдоожижения. Адсорбент, двигаясь сверху вниз через переточные устройства, передается с одной контактной ступени на другую. Газ движется в аппарате противотоком снизу вверх. Для отделения из газового потока частичек адсорбента перед выходом из адсорбера газ направляют в циклоны. В аппаратах с псевдоожиженным (кипящим) слоем адсорбента можно интенсифицировать процесс массопередачи при адсорбции за счет уменьшения размера гранул и более интенсивного обновления их контактной поверхности. В процессе адсорбции с псевдоожиженным слоем адсорбента наблюдается самый интенсивный тепло-массоперенос (а также химическая реакция в каталитических процессах), поэтому есть тенденция замены стационарных процессов (адсорбции, катализа) на процессы с псевдоожиженным слоем Использование данной технологии сдерживается следующими недостатком: образование потерь адсорбента при недостаточном пылеулавливании и необходимости добавлять свежий адсорбент.
Рис. 5.5. Схема адсорбера с псевдоожиженным слоем адсорбента: 1 — корпус; 2 — контактная тарелка; 3 — переточное устройство; 4 — циклон; 5 — люк-лаз/ Потоки: / — исходный газ; II — регенерированный адсорбент; III — отработанный газ; /V — отработанный адсорбент 5.5.3 А дсорбер с движущимся слоем адсорбента Адсорбер с движущимся слоем адсорбента обычно представляет собой аппарат, в верхней секции которого осуществляется стадия адсорбции, а в нижней части - стадия десорбции. Для циркуляции адсорбента в системе применяют пневмотранспорт. Адсорберы с движущимся слоем адсорбента применяются для извлечения этилена из его смеси с водородом и метаном, водорода из смеси газов и т.п. В этом случае процесс ведется непрерывно и каждая его стадия осуществляется в определенном аппарате или части аппарата, причем адсорбент последовательно перемещается между отдельными аппаратами по системе пневмотранспорта. В качестве адсорбента часто применяется гранулированный активированный уголь. Потерянный в результате сорбент компенсируется добавлением свежего. При этом размеры зерен в процессе с движущимся слоем адсорбента в 10-30 раз крупнее, чем в псевдоожиженном, это приводит к снижению интенсивности массопереноса, а значит и увеличению размеров аппарата при той же производительности. В зарубежной литературе процессы адсорбции с движущимся слоем адсорбента называют гиперсорбцией. Рис. 5.6 Аппарат с движущимся слоем адсорбента -нет 5.6 О сновы расчета адсорбера При расчете адсорбера обычно пользуются экспериментальными данными по активности адсорбента для соответствующих компонентов смеси. Общее количество поглощенных компонентов в единицу времени:
Если адсорбер имеет неподвижный слой, то при длительности процесса адсорбции будет поглощено следующее количество вещества:
Средняя активность адсорбента:
Необходимое для адсорбции количество адсорбента равно:
Расчет числа теоретических тарелок может быть выполнен с использованием изотермы адсорбции и рабочей линии по аналогии с расчетом других массобменных процессов (рисунок 20.3). Число теоретических тарелок определяется графическим построением ломаной линии между изотермой адсорбции и рабочей линией. На основе такого построения производится определение общего числа теоретических тарелок. Необходимая высота адсорбера определяется по уравнению:
где hэ - высота слоя адсорбента, эквивалентная одной теоретической тарелке, определяется экспериментально.
Рис. 20.3. Графическое определение числа теоретических ступеней изменения концентраций для адсорбера: ОС — изотерма адсорбции; АВ — рабочая линия
Вопросы для самопроверки
55. Рафинатный раствор содержит … 56. КТР при экстракции это …
58. Чем больше коэффициент избирательности при экстракции, тем…
Часть
Разработала канд. техн. наук, доц. ___________ Р.Р.Ибрагимова (подпись, дата)
Уфа 2018
Рекомендуемая литература 1. Касаткин А.Г. Основные процессы и аппараты химической технологии. 14-е изд. (перепечатано с 9-го изд. 1973 г.).- М.: Альянс, 2008.-750с. 2. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. 14 изд. (перепеч. с изд. 1987 г.), -М.: Альянс, 2007.-576с. 3.Скобло А.И., Молоканов Ю.К., Владимиров А.И., Щелкунов В.А. Процессы и аппараты нефтегазопереработки и нефтехимии: Учебник для вузов.- 3-е изд., перераб. и доп. – М.: Недра-Бизнесцентр, 2000, 677 с. 4 Молоканов Ю.К. Процессы и аппараты нефтегазопереработки. – М., Химия, 1980, 408 с. 5. Сугак А.А, Процессы и аппараты химической технологии / А.В.Сугак, В.К.Леонтьев, В.В.Туркин.- М.: Издательский центр «Академия», 2005.- 224с. Основные понятия и законы массообмена Общие признаки массообменных процессов Массообменные или диффузионные процессы связаны с переходом компонентов из одной фазы в другую с целью их разделения. Все массообменные процессы обладают рядом общих признаков. 1. Они применяются для разделения гомогенных смесей. 2. В любом процессе участвуют, по крайней мере, две фазы: жидкая и паровая (перегонка и ректификация), жидкая и газовая (абсорбция), твердая и парогазовая (адсорбция), твердая и жидкая (адсорбция, экстракция), две жидких (экстракция). 3. Переход вещества из одной фазы в другую осуществляется за счет диффузии. 4. Движущей силой массообменных процессов является разность концентраций или градиент концентраций. Процесс протекает в направлении той фазы, в которой концентрация компонента меньше. 5. Перенос вещества из одной фазы в другую происходит через границу раздела фаз, на которой предполагается состояние равновесия фаз. 6. Диффузионные процессы обратимы, т.е. направление процесса определяется законами фазового равновесия. 7.Переход вещества из одной фазы в другую заканчивается при достижении динамического равновесия. Состояние равновесия следует понимать так, что обмен между фазами не прекращается, однако скорости перехода компонентов из одной фазы в другую выравниваются. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Последнее изменение этой страницы: 2019-04-10; Просмотров: 541; Нарушение авторского права страницы