
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Развернутая форма Периодической системы элементов с указанием геохимических ассоциаций ⇐ ПредыдущаяСтр 2 из 2
Mо | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6
| Cs | Ba | TR | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi |
Po | At | Rn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7
| Fr | Ra | Aс |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Элементы магматических месторождений (Mg, Al, P, Sc, Ti, V, Cr, Fe, Co, Ni, Cu, Ru, Rh, Pd, Os, Ir, Pt) | Элементы гидротермальных и колчеданных месторождений (F, S, Cu, Zn, Ga, Ge, As, Se, Mo, Ag, Cd, In, Sn, Sb, Te, Ba, W, Re, Au, Hg, Tl, Pb, Bi, Ra, U) | Элементы газовых месторождений (H, He, C, N, Ne, Ar, Kr, Xe, Rn) | |||
| Элементы пегматитовых и альбитит-грейзеновых месторождений (Li, Be, Rb, Y, Zr, Nb, Mo, Cs, TR, Hf, Ta, W) | Элементы экзогенных месторождений (H, Li, B, C, N, O, F, Na, Mg, Al, Si, P, S, Cl, K, Ca, Sc, Ti, V, Mn, Fe, Co, Ni, Br, Rb, Sr, Y, Zr, Sn, I, Ba, TR, Hf, Pt, Au, Ra, U) |
| |||
Месторождения руд золота
1. Применение вида в промышленности.
2. Геохимические особенности.
3. Промышленные минералы.
4. Требования к рудам и концентратам.
5. Геолого-промышленные типы месторождений.
6. Рейтинг геолого-промышленных типов месторождений.
Руды золота – твердые полезные ископаемые, содержащие золото в количестве, выгодном для добычи. Начало золотодобыче в России было положено в 1745 г., когда было открыто первое коренное месторождение золота – Березовское, расположенное на Среднем Урале в Свердловской области. (при Елизавете Петровне).
Государственный доклад, 2016
Россия. На 1.01.2016 г. (Гос. доклад, 2016).
Запасы 13 тыс. т (А+В+С1 и С2) 3 место в мире после ЮАР и Канады.
Добыча из недр – 286,6 т. 3 место после Китая и Австралии
Производство золота 294, 8 т, в т.ч. 13% из вторичного сырья.
Экспорт 42,5 (14,4%)
Потребление ювелирной промышленностью 34 т (11,5%)
Закупки в госрезервы – 208 (70,6%)
Средняя цена в 2016 г.40 долл./г
Ставка налога на добычу 6 %
1. Применение золота.
Ювелирная промышленность. С 1990 по 1999 г. ею ежегодно потреблялось от 81,5 до 88,5 % произведенного золота, что составляет от 2188 до 3233 т в год.
Область инвестиций (от 5,2 до 15,4 %) - покупка золота в слитках кредитными учреждениями (банками),
Область тезаврации (от греч. thesaurus – сокровище)– покупка золота частными лицами. Так, в 1999 г. на инвестиции в золото приходилось 328 т, а на тезаврацию слитков – 279 т.
Электронная промышленность (5,5 – 7,1 %) - применяется для покрытия контактов изделий повышенной надежности.
Кроме того, золото применяется в стоматологии, изготовлении монет, медалей и для других целей (Боярко, 2001).
- валютный металл,
- ювелирное дело,
- электроника,
- медицина.
Цена (2000 г.) более 1000$/унцию или 35.3 $/ г (при курсе ≈ 60руб за доллар ≈ 2120 руб/г). Унция – 28,35 г.
2. Геохимические особенности.
Кларк Au 4 10-7%. Содержание золота в рудах n1 г/т (n 10-4%).
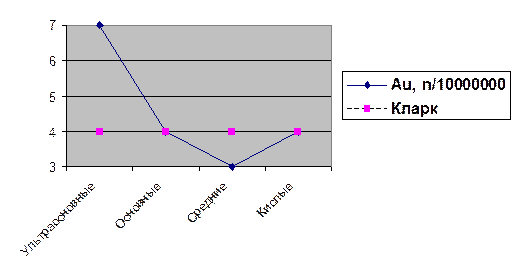
Рис. 6.1. Распределение средних содержаний золота по магматическим породам
Такое распределение обеспечивает тяготение наиболее крупных месторождений, особенно докембрийских, к зеленокаменным поясам.
Химическая миграция и осаждение золота (Реми Г., 1966) (Реми Г. Курс неорганической химии. М.: Мир, Т. I, 1963, 920 с. Т. II, 1966, 836 с.).
Положение в Период системе: № 79, I группа, побочная подгруппа, 6-й период.
На внешнем 6 слое один 6s1 электрон, на 5-м s2p6d10. Атом золота может легко отдавать 1 внешний (6s1) электрон и 2 электрона с 5-го слоя (5d2). Это обусловливает его 1 и 3 валентность.
Одновалентные соединения Au либо очень трудно растворимы (AuCl), либо образуют прочные комплексы. Трехвалентное золото более подвижно и легко мигрирует.
Золото растворяется в водных растворах хлора при обычной температуре
Au + 3/2 Cl2 = AuCl3 или Au+3 + 3 Cl-1.
Растворению способствует образование комплексных тетрахлороаурат-ионов
AuCl3 + Cl-1 = [AuCl4]-1 Это комплексный анион.
При избытке кислорода и недостатке хлора образуются оксотрихлороаурат-ионы
Au + 3/2 Cl2 + Н2О = [Au+3ОCl3]-2 + 2Н+1
Следовательно Au легко мигрирует в окислительной обстановке.
Золото осаждается из хлоридного раствора в восстановительных условиях, такими ионами как Fe+2, Sn+2, SO3-2, NO2-1. Ионами ртути оно восстанавливается чаще всего только до однозарядного состояния
Au+3 + Hg2+2 = Au+1 + 2 Hg+2
Au+1 сразу выделяется в виде гидроксида золота в результате реакции с водой:
Au+1 + НОН = AuОН + Н+1.
Одновременно другая часть ионов одновалентного золота по реакции 3Au+1 = Au+3 + 2 Au
и в конечном счете превращается в самородное золото .
Металлическое золото могут осаждать органические вещества и окись углерода из растворов хлорида трехвалентного металла.
Могут образовываться коллоидные гидрозоли, частицы которых имеют отрицательный заряд.
Золото образует растворимые комплексные соединения с серой
Тиосульфатоаураты Na3[Au+1(S2O3)2] ½ H2O и
Сульфитоаураты [Au+1(SO3)2]-3.
Таким образом
- большой радиус иона способствует накоплению золота в остаточных расплавах,
- золото мигрирует в окислительной щелочной обстановке, что способствует миграции его с кремнезёмом и серой,
- золото отлагается на кислотном геохимическом барьере с кварцем и сульфидами,
- золото отлагается на восстановительном геохимическом барьере, обусловленном присутствием органики (углеродистых толщ), соединений серы и других восстановителей,
- миграция золота в форме коллоидных частиц, а также в сорбированной форме на органических и глинистых частицах способствует его концентрации на электролитических геохимических барьерах, например в прибрежноморских условиях,
В результате золото концентрируетс с сульфидами и кварцем в продуктах гидротермальной деятельности.
В экзогенных условиях
-устойчивость к выветриванию,
-высокая плотность (19,3 г/см3)
способствуют накоплению золота в россыпях на гидродинамических барьерах.
И.Я. Некрасов: "Наиболее яркой геохимической особенностью золота является его космополитизм".
3. Промышленные типы золотых руд и минералы
Различают руды
- собственно золотые,
- золотосодержащие.
Таблица 6.1. Промышленные минералы
Минеральный
Химическая формула
Структура
Сингония
Габитус
Вид
Минералы золота
Интерметаллиды
Золото самородное
Координационная
Кубическая
Октаэдрический, кубический
Электрум
Кюстелит
Калаверит
Последнее изменение этой страницы: 2019-04-11; Просмотров: 198; Нарушение авторского права страницы