Составляем таблицу параметров характерных точек цикла.
Для точки a: 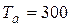 К, К, 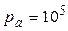 Па, Па,
 м3/кг; м3/кг;
Для точки с:  К, К,  Па, т.к. Па, т.к.  , то , то
 Па. Па.
Из соотношения параметров адиабатного процесса 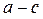 найдем объем в т. с: найдем объем в т. с:
 ; ;
 м3/кг. м3/кг.
Для точки z:  К, К,  Па. Па.
Из соотношения параметров изобарного процесса  найдем объем в т. z: найдем объем в т. z:
 ; ; 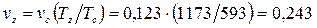 м3/кг. м3/кг.
Для точки b из соотношения параметров адиабатного процесса  : :
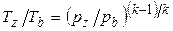 ; ;  ; ;
 , ,  Па, Па,
тогда из соотношения параметров изобарного процесса 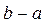 найдем объем в т. b: найдем объем в т. b:
 ; ;  м3/кг. м3/кг.
Данные сведем в таблицу 1.
Таблица 1 – Сводная таблица термодинамических параметров в характерных точках цикла
| Обозначе-
ние точки
| Давление р, Па
| Удельный объем v, м3/кг
| Температура Т, К
| | a
| 
| 0, 866
|
| | c
| 
| 0, 123
|
| | z
| 
| 0, 243
|
| | b
| 
| 1, 71
|
|
Удельная работа цикла по общей формуле
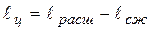
Удельную работу цикла для цикла с изобарным подводом теплоты
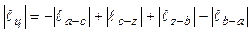 , ,
где  - удельная работа сжатия по адиабате - удельная работа сжатия по адиабате  , равная , равная
 кДж/кг; кДж/кг;
 - удельная работа расширения по изобаре - удельная работа расширения по изобаре  : :
 кДж/кг; кДж/кг;
 - удельная работа расширения по адиабате - удельная работа расширения по адиабате  : :
 кДж/кг; кДж/кг;
 - удельная работа сжатия по изобаре - удельная работа сжатия по изобаре  : :
 кДж/кг. кДж/кг.
Тогда удельная работа цикла
 кДж/кг. кДж/кг.
Определение теплоты, термического КПД и оптимальной степени повышения давления цикла
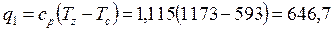 кДж/кг; кДж/кг;
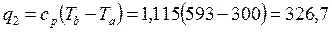 кДж/кг. кДж/кг.
Для проверки определим работу цикла по формуле
 кДж/кг кДж/кг
Термический КПД цикла  по формуле для цикла ГТУ с изобарным подводом теплоты (2.2.5) равен по формуле для цикла ГТУ с изобарным подводом теплоты (2.2.5) равен
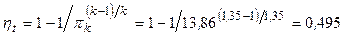
или по общей формуле
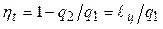 ; ;
 . .
Расхождение значений должно составлять не более 0, 1 - 0, 3%.
Определим погрешность вычислений
%=(0, 495-0, 495)/0, 495=0%.
Определим оптимальную степень повышения давления   опт опт
 опт= опт=  . .
Расчет изменения термодинамических функций рабочего тела
Определяем изменение энтальпии и внутренней энергии для каждого процесса цикла по общим формулам:
 ; ;  . .
для процесса  : :
 кДж/кг, кДж/кг,
 кДж/кг; кДж/кг;
для процесса  : :
 кДж/кг, кДж/кг,
 кДж/кг; кДж/кг;
для процесса  : :
 кДж/кг, кДж/кг,
 кДж/кг; кДж/кг;
для процесса 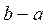 : :
 кДж/кг, кДж/кг,
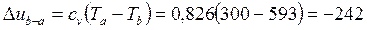 кДж/кг. кДж/кг.
Определение изменения энтропии в процессе цикла
Энтропия начальной точки для цикла с изобарным подводом теплоты
 , ,
где 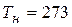 К; К;  Па, Па,
 Дж/(кг× К) Дж/(кг× К)
для процесса  : :
 , т.к. процесс , т.к. процесс 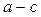 - адиабатный; - адиабатный;
для процесса  : :
 Дж/(кг× К); Дж/(кг× К);
для процесса  : :
 , т.к. процесс , т.к. процесс 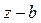 - адиабатный; - адиабатный;
для процесса  : :
 Дж/(кг× К). Дж/(кг× К).
Полученные данные сводятся в сводную таблицу термодинамических функций (табл. 2).
Построение рабочей и тепловой диаграмм цикла
Для изображения адиабатных процессов расширения и сжатия и p-v координатах вычислим параметры промежуточных точек 1 и 2 в этих процессах. Выбираем давление в т. 1 и 2 - одинаковое
 Па, Па,
тогда
 м3/кг; м3/кг;
 м3/кг. м3/кг.
Для изображения изобарных процессов 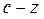 и и 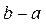 в T-s координатах примем промежуточные значения температур этих процессов и вычислим изменение энтропии для промежуточных процессов в T-s координатах примем промежуточные значения температур этих процессов и вычислим изменение энтропии для промежуточных процессов  и и  : :
 К, К,  К К
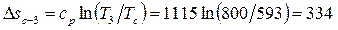 Дж/(кг× К); Дж/(кг× К);
 Дж/(кг× К). Дж/(кг× К).
При этих изменениях энтропии значения энтропии в точках цикла будут определены как:
 Дж/(кг× К), Дж/(кг× К), 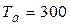 К; К;
 Дж/(кг× К), Дж/(кг× К),  К; К;
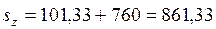 Дж/(кг× К), Дж/(кг× К),  К; К;
 Дж/(кг× К), Дж/(кг× К), 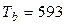 К; К;
 Дж/(кг× К), Дж/(кг× К),  К; К;
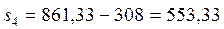 Дж/(кг× К), Дж/(кг× К), 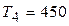 К. К.
По полученным значениям на двух листах формата А4 в масштабе строятся циклы в p-v и T-s - диаграммах (рис. 8).
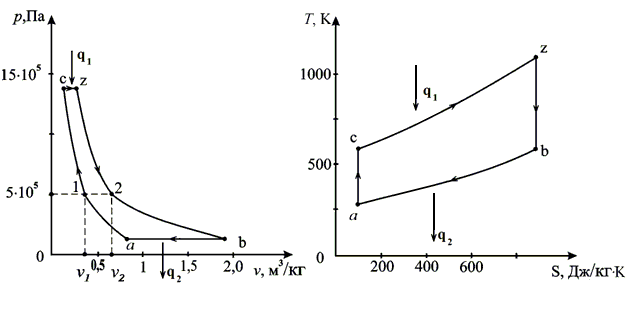
Рис.8 Цикл ГТУ с изобарным подводом теплоты в p, v- и T, s – диаграммах
Оформление курсовой работы
Курсовая работа оформляется в соответствии с установленными требованиями ГОСТ 2.105-95 (с учетом изменения №1 от 22.06.2006 №117-ст). Работа должна содержать: титульный лист, задание на курсовую работу, содержание, исходные данные, теоретическую часть, основную часть (расчетно-пояснительную и графическую части), заключение (выводы), список использованных источников литературы, приложение (поясняющие материалы).
Курсовую работу оформляют на листах формата А4. На титульном листе указывают: министерство, наименование института, кафедры, название дисциплины, полное название курсовой работы, номер варианта, группу и фамилию студента, руководителя курсовой работы.
Единицы измерения должны быть представлены в системе СИ.
Каждый пункт расчета должен сопровождаться краткими пояснениями.
Формулы должны начинаться с новой строки с необходимыми пояснениями буквенных обозначений.
Сдача работы осуществляется в установленные учебным планом сроки. Оценка курсовой работы выставляется по результатам ее защиты.
ЛИТЕРАТУРА
1. Луканин В.Н., Шатров М.Г., Камфер Г.М. Теплотехника. - М.: Высшая школа, 1999.
2. Кузовлев В.А. Техническая термодинамика и основы теплопередачи. - М.: Высшая школа, 1983.
3. Нащокин В.В. Техническая термодинамика. – М.: Высшая школа, 1980.
ПРИЛОЖЕНИЕ
Таблица 1 - Средние массовые теплоёмкости газов при постоянном давлении  , кДж/( , кДж/( 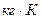 ) )
 C C
|  O O  
| N  (атмос-ферный)
(атмос-ферный)
| CO
| CO 
| H  O O
| O 
| Воздух
(абс. сухой)
| |
| 0, 9148
0, 9232
0, 9353
0, 9500
0, 9651
0, 9793
0, 9927
1, 0048
1, 0157
1, 0258
1, 0350
1, 0434
1, 0509
1, 0580
1, 0647
1, 0714
1, 0773
1, 0831
1, 0886
1, 0940
1, 0990
1, 1041
1, 1087
1, 1137
1, 1183
1, 1229
| 1, 0304
1, 0316
1, 0346
1, 0400
1, 0475
1, 0567
1, 0668
1, 0777
1, 0881
1, 0982
1, 1078
1, 1170
1, 1258
1, 1342
1, 1422
1, 1497
1, 1564
1, 1631
1, 1690
1, 1748
1, 1803
1, 1853
1, 1903
1, 1946
1, 1991
1, 2029
| 1, 0396
1, 0417
1, 0463
1, 0538
1, 0634
1, 0748
1, 0861
1, 0978
1, 1091
1, 1200
1, 1304
1, 1401
1, 1493
1, 1577
1, 1656
1, 1731
1, 1798
1, 1865
1, 1924
1, 1983
1, 2033
1, 2083
1, 2129
1, 2176
1, 2217
1, 2259
| 0, 8148
0, 8658
0, 9102
0, 9487
0, 9826
1, 0128
1, 0396
1, 0639
1, 0852
1, 1045
1, 1225
1, 1384
1, 1530
1, 1660
1, 1782
1, 1895
1, 1995
1, 2091
1, 2179
1, 2259
1, 2334
1, 2405
1, 2468
1, 2531
1, 2586
1, 2636
| 1, 8594
1, 8728
1, 8937
1, 9192
1, 9477
1, 9778
2, 0092
2, 0419
2, 0754
2, 1097
2, 1436
2, 1771
2, 2106
2, 2429
2, 2743
2, 3048
2, 3346
2, 3630
2, 3907
2, 4166
2, 4422
2, 4661
2, 4895
2, 5121
2, 5334
2, 5544
| 0, 607
0, 636
0, 662
0, 687
0, 708
0, 724
0, 737
0, 754
0, 762
0, 775
0, 783
0, 791
0, 795
__
__
__ __
__
__
__
__
__
__
__
__
__
| 1, 0038
1, 0062
1, 0118
1, 0191
1, 0283
1, 0387
1, 0454
1, 0603
1, 0710
1, 0815
1, 0907
1, 0998
1, 1072
1, 1106
1, 1242
1, 1313
1, 1380
1, 1443
1, 1501
1, 1560
1, 1610
1, 1664
1, 1710
1, 1757
1, 1803
1, 1840
|
Пример оформления титульного листа
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«Ижевский государственный технический университет имени М.Т. Калашникова»
(ФГБОУ ВПО «ИжГТУ имени М.Т. Калашникова»)
Чайковский технологический институт (филиал)
Кафедра Автомобильный транспорт
Курсовая работа
по дисциплине «Теплотехника»
на тему «Расчет и анализ газового цикла» № варианта
«Расчет теплопередачи» № варианта
Выполнил: студент группы
Ф.И.О.
Проверил: к.т.н., доцент
Чепикова Т.П.
Чайковский 2012
Варианты заданий для КР по теплотехнике
«Расчет и анализ газового цикла»
(1 часть КР)
| № варианта
| Название цикла
| |
| а) Прямой цикл Карно
| | 1.
| tmax=2500C, tmin=300C, p1=1МПа, p3=120кПа, mсм=1кг,
массовые доли компонентов: N2=0, 75, CO=0, 1, CO2=0, 1, H2O=0, 05
| | 2.
| t1=10000C, p1=1МПа, p2=0, 5MПа,  =0, 862 м3,
массы компонентов: mСO2=2, 5кг, mN2=1, 5кг, mO2=0, 5кг, mСO=0, 5кг =0, 862 м3,
массы компонентов: mСO2=2, 5кг, mN2=1, 5кг, mO2=0, 5кг, mСO=0, 5кг
| | 3.
| tmax=2270C, p1=1МПа, p3=0, 1MПа,  =0, 178 м3, mсм=1, 5кг,
массовые доли компонентов: N2=0, 74, CO=0, 05, CO2=0, 15, H2O=0, 06 =0, 178 м3, mсм=1, 5кг,
массовые доли компонентов: N2=0, 74, CO=0, 05, CO2=0, 15, H2O=0, 06
| | 4.
| p3=140кПа, t3=450C, p1=9МПа,  =0, 345 м3, массы компонентов: mСO2=1, 5кг, mN2=3кг, mН2O=0, 5кг, mСO=1, 5кг =0, 345 м3, массы компонентов: mСO2=1, 5кг, mN2=3кг, mН2O=0, 5кг, mСO=1, 5кг
| | 5.
| t4=3500C, p4=0, 3МПа, p2=1, 8MПа,  =0, 743 м3, mсм=0, 8кг,
массовые доли компонентов: N2=0, 73, CO=0, 06, CO2=0, 14, H2O=0, 07 =0, 743 м3, mсм=0, 8кг,
массовые доли компонентов: N2=0, 73, CO=0, 06, CO2=0, 14, H2O=0, 07
| | 6.
| р2=811кПа, t4=200C, Т2=700К, p4=145кПа, массы компонентов:
mO2=1, 2кг, mСO2=1, 4кг, mN2=1, 6кг, mСO=0, 8кг
| | 7.
| p2=410кПа, Т2=500К, p3=0, 2МПа, 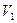 =0, 277 м3, mсм=1, 2кг,
массовые доли компонентов: N2=0, 72, O2= 0, 05, CO2=0, 15, H2O=0, 08 =0, 277 м3, mсм=1, 2кг,
массовые доли компонентов: N2=0, 72, O2= 0, 05, CO2=0, 15, H2O=0, 08
| | 8.
| р1=2МПа, Т1=800К, p3=120кПа, Т3=300К, массы компонентов:
mO2=0, 5кг, mСO2=1, 3кг, mN2=2, 8кг, mН2O =0, 2кг
| |
| б) Цикл ДВС со смешанным подводом теплоты (цикл Сабатэ-Тринклера)
| | 9.
| pа=0, 1МПа, t2=300C, 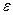 =17, =17,  =2, =2,  =1, 2, mсм=3кг,
массовые доли компонентов: N2=0, 73, O2= 0, 05, CO2=0, 13, H2O=0, 04, CO=0, 05 =1, 2, mсм=3кг,
массовые доли компонентов: N2=0, 73, O2= 0, 05, CO2=0, 13, H2O=0, 04, CO=0, 05
| | 10.
| pа=0, 1МПа, Та=288К, 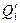 =840кДж, =840кДж, 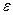 =15, =15,  =1, 8, массы компонентов: mO2=0, 5кг, mСO2=1кг, mN2=2, 6кг, mН2O =0, 1кг =1, 8, массы компонентов: mO2=0, 5кг, mСO2=1кг, mN2=2, 6кг, mН2O =0, 1кг
| | 11.
| pа=0, 1МПа, t2=270C, 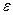 =15, pz=5, 5МПа, =15, pz=5, 5МПа,  =1340кДж, mсм=2кг, массовые доли компонентов: N2=0, 71, O2= 0, 1, CO2=0, 1, H2O=0, 09 =1340кДж, mсм=2кг, массовые доли компонентов: N2=0, 71, O2= 0, 1, CO2=0, 1, H2O=0, 09
| | 12.
| pа=0, 2МПа, tа=180C, 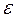 =16, =16,  =4, =4, 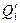 =8552, 81кДж, =8552, 81кДж,  =348кДж, массы компонентов: mO2=0, 2кг, mСO2=1, 5кг, mN2=2, 2кг, mСO=1, 05кг =348кДж, массы компонентов: mO2=0, 2кг, mСO2=1, 5кг, mN2=2, 2кг, mСO=1, 05кг
| | 13.
| tmin=270C, pmin=0, 1МПа, 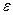 =14, =14,  =3, 5, =3, 5,  =1, 7, mсм=2, 8кг, массовые доли компонентов: N2=0, 65, O2= 0, 15, CO2=0, 15, CO=0, 05 =1, 7, mсм=2, 8кг, массовые доли компонентов: N2=0, 65, O2= 0, 15, CO2=0, 15, CO=0, 05
| | 14.
| pа=0, 4МПа, tmin=250C, 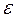 =18, =18,  =1, 9, =1, 9,  =1, 6, массы компонентов: mO2=0, 6кг, mСO2=1, 2кг, mN2=2, 2кг, mСO=0, 6кг =1, 6, массы компонентов: mO2=0, 6кг, mСO2=1, 2кг, mN2=2, 2кг, mСO=0, 6кг
| | 15.
| Тmin=300К, pmin=140кПа, 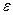 =19, =19,  =2, 3, =2, 3,  =1560кДж/кг, mсм=1кг, массовые доли компонентов: N2=0, 74, O2= 0, 1, CO2=0, 1, CO=0, 05, H2O=0, 01 =1560кДж/кг, mсм=1кг, массовые доли компонентов: N2=0, 74, O2= 0, 1, CO2=0, 1, CO=0, 05, H2O=0, 01
| | 16.
|  =1750кДж, tа=400C, pа=0, 1МПа, =1750кДж, tа=400C, pа=0, 1МПа, 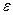 =12, =12,  =3, 8, массы компонентов: mO2=0, 5кг, mСO2=0, 3кг, mN2=1, 5кг, mН2O =0, 2кг =3, 8, массы компонентов: mO2=0, 5кг, mСO2=0, 3кг, mN2=1, 5кг, mН2O =0, 2кг
| | 17.
| pmin=100кПа, tmin=450C,  =0, 08 м3/кг, pz=6, 8МПа, =0, 08 м3/кг, pz=6, 8МПа,  =1, 42, mсм=1кг, массовые доли компонентов: N2=0, 75, O2= 0, 15, CO2=0, 08, H2O=0, 02 =1, 42, mсм=1кг, массовые доли компонентов: N2=0, 75, O2= 0, 15, CO2=0, 08, H2O=0, 02
| | 18.
| pа=1бар, tа=270C,  =106, 86 бар, =106, 86 бар, 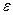 =21, =21,  =1, 57, показатель политропы сжатия n1=1, 38, политропы расширения n2=1, 22, R=287кДж/кг*К, сv=0, 718кДж/кг*К, ср=1, 005кДж/кг*К, m=1кг =1, 57, показатель политропы сжатия n1=1, 38, политропы расширения n2=1, 22, R=287кДж/кг*К, сv=0, 718кДж/кг*К, ср=1, 005кДж/кг*К, m=1кг
| |
| в) Цикл ДВС с изохорным подводом теплоты (цикл Отто)
| | 19.
| pа=0, 1МПа, tа=270C, 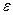 =10, Q1=1, 13МДж, mсм=1, 6кг, массовые доли компонентов: N2=0, 7, O2= 0, 15, CO2=0, 1, H2O=0, 01, CO=0, 04 =10, Q1=1, 13МДж, mсм=1, 6кг, массовые доли компонентов: N2=0, 7, O2= 0, 15, CO2=0, 1, H2O=0, 01, CO=0, 04
| | 20.
| pа=0, 1МПа, tа=900C, 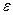 =8, =8,  =1, 6, mсм=3кг, массовые доли компонентов: N2=0, 72, O2= 0, 15, CO2=0, 05, H2O=0, 08 =1, 6, mсм=3кг, массовые доли компонентов: N2=0, 72, O2= 0, 15, CO2=0, 05, H2O=0, 08
| | 21.
| pа=0, 1МПа, tа=270C, 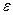 =9, =9,  =4, массы компонентов: mСO2=1, 2кг, mN2=2, 2кг, mН2O =0, 1кг, mСO=0, 5кг =4, массы компонентов: mСO2=1, 2кг, mN2=2, 2кг, mН2O =0, 1кг, mСO=0, 5кг
| | 22.
| pа=100кПа, tа=800C, 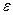 =11, =11,  =1, 85, mсм=3, 2кг, массовые доли компонентов: N2=0, 73, CO=0, 07, CO2=0, 13, H2O=0, 07 =1, 85, mсм=3, 2кг, массовые доли компонентов: N2=0, 73, CO=0, 07, CO2=0, 13, H2O=0, 07
| | 23.
| pа=190кПа, tа=800C,  =1, 6, =1, 6,  =0, 22 м3/кг, mсм=1кг, массовые доли компонентов: N2=0, 74, O2= 0, 16, CO2=0, 09, H2O=0, 01 =0, 22 м3/кг, mсм=1кг, массовые доли компонентов: N2=0, 74, O2= 0, 16, CO2=0, 09, H2O=0, 01
| | 24.
| pmin=0, 09МПа, Тmin=353К, Тmax=673К,  =2, 3, mсм=3, 4кг, массовые доли компонентов: N2=0, 72, O2= 0, 04, CO2=0, 16, H2O=0, 08 =2, 3, mсм=3, 4кг, массовые доли компонентов: N2=0, 72, O2= 0, 04, CO2=0, 16, H2O=0, 08
| |
| г) Цикл ДВС с изобарным подводом теплоты (цикл Дизеля)
| | 25.
| pmin=0, 1МПа, ТZ=800К,  =0, 88 м3/кг, =0, 88 м3/кг, 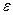 =13, mсм=1кг, массовые доли компонентов: N2=0, 74, CO=0, 05, CO2=0, 15, H2O=0, 06 =13, mсм=1кг, массовые доли компонентов: N2=0, 74, CO=0, 05, CO2=0, 15, H2O=0, 06
| | 26.
| pа=0, 15МПа, tа=800C, 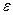 =15, =15,  =1, 3, mсм=1, 3кг, массовые доли компонентов: O2= 0, 1, N2=0, 7, CO2=0, 11, H2O=0, 09 =1, 3, mсм=1, 3кг, массовые доли компонентов: O2= 0, 1, N2=0, 7, CO2=0, 11, H2O=0, 09
| | 27.
| pа=0, 2МПа, tа=500C, 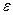 =16, =16,  =1, 4, n=1, 38 – политропное расширение и сжатие, mсм=1кг, массовые доли компонентов: O2= 0, 16, N2=0, 7, CO2=0, 1, H2O=0, 01, CO=0, 03 =1, 4, n=1, 38 – политропное расширение и сжатие, mсм=1кг, массовые доли компонентов: O2= 0, 16, N2=0, 7, CO2=0, 1, H2O=0, 01, CO=0, 03
| | 28.
| pа=0, 15МПа, tа=700C, 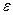 =10, =10,  =2, 3, массы компонентов: mСO2=1, 1кг, mN2=1, 8кг, mН2O =0, 3кг, mСO=0, 8кг, mO2=0, 2кг =2, 3, массы компонентов: mСO2=1, 1кг, mN2=1, 8кг, mН2O =0, 3кг, mСO=0, 8кг, mO2=0, 2кг
| |
| д) Цикл ГТУ с изобарным подводом теплоты без регенерации (цикл Брайтона)
| | 29.
| pа=90кПа, tа=270C, pс=0, 9МПа, tz=6000C, mсм=1, 4кг, массовые доли компонентов: N2=0, 74, CO2=0, 13, H2O=0, 08, CO=0, 05
| | 30.
| pа=0, 08МПа, tа= - 100C, 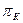 =5, =5,  =3, mсм=1, 7кг, массовые доли компонентов: O2= 0, 16, N2=0, 72, CO2=0, 04, H2O=0, 08 =3, mсм=1, 7кг, массовые доли компонентов: O2= 0, 16, N2=0, 72, CO2=0, 04, H2O=0, 08
| | 31.
| tz=9500C, pа=0, 1МПа, 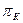 =8, =8,  =2, 2, mсм=1, 6кг, массовые доли компонентов: O2= 0, 2, N2=0, 61, CO2=0, 1, H2O=0, 09 =2, 2, mсм=1, 6кг, массовые доли компонентов: O2= 0, 2, N2=0, 61, CO2=0, 1, H2O=0, 09
| | 32.
| 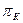 =9, =9,  =2, 8, pа=0, 8МПа, tа= -120C, mсм=1, 5кг, массовые доли компонентов: O2= 0, 1, N2=0, 75, CO2=0, 1, H2O=0, 01, CO=0, 04 =2, 8, pа=0, 8МПа, tа= -120C, mсм=1, 5кг, массовые доли компонентов: O2= 0, 1, N2=0, 75, CO2=0, 1, H2O=0, 01, CO=0, 04
| | 33.
| 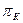 =9, =9,  =2, 8, pа=0, 8МПа, tа= -120C, n=1, 3 – политропное расширение и сжатие, mсм=1кг, массовые доли компонентов: O2= 0, 05, N2=0, 8 CO2=0, 1, H2O=0, 01, CO=0, 04 =2, 8, pа=0, 8МПа, tа= -120C, n=1, 3 – политропное расширение и сжатие, mсм=1кг, массовые доли компонентов: O2= 0, 05, N2=0, 8 CO2=0, 1, H2O=0, 01, CO=0, 04
| | 34.
| pа=0, 15МПа, pс=0, 7МПа, tа=180C, tz=8300C, массы компонентов: mСO2=1, 6кг, mN2=1, 9кг, mН2O =0, 2кг, mСO=0, 7кг, mO2=0, 1кг
| | 35.
| pа=0, 1МПа, pс=0, 5МПа, tа=150C, tz=7500C, массы компонентов: mСO2=1, 4кг, mN2=2, 4кг, mН2O =0, 4кг, mСO=0, 2кг
| | 36.
| Tmin=300К, pmin=0, 09МПа, Tmax=1181К, 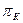 =14, массы компонентов: mO2=0, 3кг, mСO2=1, 5кг, mN2=2, 6кг, mН2O =0, 5кг =14, массы компонентов: mO2=0, 3кг, mСO2=1, 5кг, mN2=2, 6кг, mН2O =0, 5кг
| |
| е) Цикл ГТУ с изобарным подводом теплоты с регенерацией теплоты
| | 37.
| pа=0, 08МПа, tа= - 100C, 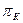 =5, =5,  =3, mсм=1, 4кг, массовые доли компонентов: O2= 0, 06, N2=0, 74, CO2=0, 14, H2O=0, 02, CO=0, 04 =3, mсм=1, 4кг, массовые доли компонентов: O2= 0, 06, N2=0, 74, CO2=0, 14, H2O=0, 02, CO=0, 04
| | 38.
| tz=9500C, pа=0, 1МПа, 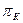 =9, =9,  =2, 2, массы компонентов: mСO2=1, 2кг, mN2=2, 2кг, mН2O =0, 2кг, mСO=0, 3кг, mO2=0, 4кг =2, 2, массы компонентов: mСO2=1, 2кг, mN2=2, 2кг, mН2O =0, 2кг, mСO=0, 3кг, mO2=0, 4кг
| | 39.
| 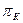 =12, =12,  =2, 7, pа=150кПа, tа= - 150C, массы компонентов: mСO2=1, 6кг, mN2=2, 2кг, mН2O =0, 1кг, mСO=0, 4кг, mO2=0, 4кг =2, 7, pа=150кПа, tа= - 150C, массы компонентов: mСO2=1, 6кг, mN2=2, 2кг, mН2O =0, 1кг, mСO=0, 4кг, mO2=0, 4кг
| | 40.
| 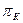 =8, =8,  =2, 7, pа=150кПа, tа= - 150C, n=1, 36 – политропное расширение и сжатие, mсм=1кг, массовые доли компонентов: O2= 0, 2, N2=0, 61, CO2=0, 1, H2O=0, 09 =2, 7, pа=150кПа, tа= - 150C, n=1, 36 – политропное расширение и сжатие, mсм=1кг, массовые доли компонентов: O2= 0, 2, N2=0, 61, CO2=0, 1, H2O=0, 09
| | 41.
| 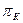 =10, =10,  =2, 5, pа=0, 085МПа, tа= - 200C, массы компонентов: mСO2=1, 1кг, mN2=1, 9кг, mН2O =0, 2кг, mСO=0, 1кг, mO2=0, 2кг, n=1, 42 – политропное расширение, n=1, 3 – политропное сжатие =2, 5, pа=0, 085МПа, tа= - 200C, массы компонентов: mСO2=1, 1кг, mN2=1, 9кг, mН2O =0, 2кг, mСO=0, 1кг, mO2=0, 2кг, n=1, 42 – политропное расширение, n=1, 3 – политропное сжатие
|
ПРИЛОЖЕНИЕ
Таблица - Удельные газовые постоянные и молярные массы некоторых газов и водяного пара
| Наименование газа
| Химическая формула
| Удельная газовая постоянная R, Дж/(кг*К)
| Молярная масса 
| | Водород
| H2
| 4124, 3
| 2, 0159
| | Метан
| CH4
| 518, 25
| 16, 043
| | Аммиак
| NH3
| 488, 20
| 17, 031
| | Азот
| N2
| 296, 8
| 28, 013
| | Воздух
| -
| 287, 10
| 28, 970
| | Кислород
| O2
| 259, 80
| 31, 996
| | Углекислый газ
| CO2
| 188, 90
| 44, 0079
| | Окись углерода
| CO
| 296, 80
| 28, 011
| | Водяной пар
| H2O
| 461, 50
| 18, 014
|
Популярное:
|

