
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Бийский технологический институт (филиал)Стр 1 из 31Следующая ⇒
Бийский технологический институт (филиал) государственного образовательного учреждения высшего профессионального образования «Алтайский государственный технический университет им. И.И. Ползунова»
Ю.Н. Денисов, Н.А. Орлова, Е.А. Пазников
ОСНОВНЫЕ ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ ЧАСТЬ 2 ТИПОВЫЕ ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
Рекомендовано Сибирским региональным учебно-методическим центром высшего профессионального образования для межвузовского использования в качестве учебного пособия для студентов специальностей 240701 «Химическая технология органических соединений азота», 240702 «Химическая технология полимерных композиций, порохов и твердых ракетных топлив», 240901 «Биотехнология», 240706 «Автоматизированное производство химических предприятий» по курсу «Основные процессы и аппараты химических технологий» и для студентов специальностей 260601 «Машины и аппараты пищевых производств», 260204 «Технология бродильных производств и виноделие» по курсу «Процессы и аппараты пищевых производств»
Бийск Издательство Алтайского государственного технического университета им. И.И. Ползунова 2010 УДК 66.01
Рецензенты: зам. директора ИПХЭТ СО РАН по НР д.х.н. С.Г. Ильясов; зав. кафедрой ХТиИЭ к.т.н., доцент И.А. Лебедев.
Денисов, Ю.Н. Основные процессы и аппараты химической технологии. Часть 2: Типовые процессы и аппараты химической технологии: курс лекций / Ю.Н. Денисов, Н.А. Орлова, Е.А. Пазников; Алт. гос. техн. ун-т, БТИ. – Бийск: Изд-во Алт. гос. техн. ун-та, 2010. – 156 с.
ISBN 978-5-9257-0196-6
В настоящем учебном издании излагается материал по четырем модулям курса, с пятого по восьмой, в которых рассматриваются общие закономерности и принципы анализа и расчета процессов химической технологии. Изложены основы теории гидравлики, тепловых и массообменных процессов. Данный материал служит фундаментом для дальнейшего изучения курсов ПАХТ и ПАПП. Курс лекций предназначен для студентов специальностей 240901 «Биотехнология», 240702 «Химическая технология полимерных композиций, порохов и твердых ракетных топлив», 240701 «Химическая технология органических соединений азота», 240706 «Автоматизированное производство химических предприятий», 260601 «Машины и аппараты пищевых производств», 260204 «Технология бродильных производств и виноделие» очной, очно-заочной и заочной форм обучения.
УДК 66.01
ISBN 978-5-9257-0196-6 © Денисов Ю.Н., Орлова Н.А., Пазников Е.А., 2010 © БТИ АлтГТУ, 2010 СОДЕРЖАНИЕ
ПРЕДИСЛОВИЕ
Изучение весьма нелегкого для студентов курса «Основные процессы и аппараты химической технологии» (ПАХТ) требует грамотной постановки задач, логически выдержанного хода решений, анализа найденных результатов, то есть постоянной работы на понимание. Успешность обучения будет зависеть и от индивидуальных особенностей студентов, и от степени их подготовки к овладению данной системой знаний и умений, степени мотивации, интереса к изучаемой дисциплине, общих интеллектуальных умений, уровня и качества организации учебного процесса и других причин. Предусмотреть, как пойдет познавательный процесс у каждого студента, невозможно, но известно необходимое условие, которое определяет его успешность – это целенаправленная, систематическая, планомерная самостоятельная работа студента. Современная методика преподавания ориентирована, прежде всего, на выработку комплекса определенных умений, необходимых будущему специалисту, и умений не только узкоспециальных, но и фундаментальных, таких как, например, умение учиться. Предлагаемая технология обучения применяется более 10 лет на кафедре «Процессы и аппараты химической технологии» Бийского технологического института АлтГТУ им. И.И. Ползунова и показала свою эффективность. Переход на многоуровневую систему высшего образования и, как следствие, усложнение учебного материала в связи с изменением принципов построения учебных планов и курсов потребовали в последние годы интенсификации обучения и существенной самостоятельной учебной деятельности студентов. Определенный вклад в решение этих задач должна внести разработка и внедрение в учебный процесс научно обоснованных, современных образовательных технологий, среди которых особое место занимает модульно-рейтинговая технология обучения (МРТО). Модульно-рейтинговая технология имеет целью поставить студента перед необходимостью регулярной самостоятельной учебной работы в течение всего семестра. Это достигается делением учебного материала курса на крупные блоки (модули), по завершении которых студент сдает промежуточные (модульные) экзамены (ПЭ). Полученные им баллы за все ПЭ суммируются и составляют его рейтинг по данной дисциплине. При этом баллы, полученные за текущую учебную работу, рассматриваются как допуск студента к промежуточным экзаменам. Осаждение
Осаждение – это процесс разделения суспензии, эмульсии, аэрозолей в гравитационном, центробежном и электрических полях. К основным видам осаждения относят осаждение под действием силы тяжести – отстаивание, осаждение под действием центробежных сил – циклонирование и осадительное центрифугирование, очистка газов в электрическом поле. При движении материальной частицы в жидкой среде или при обтекании неподвижной частицы потоком жидкости возникают гидродинамические сопротивления, величины которых зависят в первую очередь от гидродинамических условий, природы сплошной среды и формы обтекаемых частиц. Закон сопротивления в этом случае определяется явлениями, происходящими в пограничном слое. Независимо от режима движения и формы твердого тела, движущегося в жидкости, сила сопротивления R среды может быть выражена в общем виде законом Ньютона: где F – лобовое сечение частицы (рисунок 5.2), м2 (это площадь проекции частицы на площадь, нормальную направлению ее движения), для шарообразной частицы ρср – плотность сплошной среды, кг/м3; wос – скорость движения частицы или среды, м/с; ξ – коэффициент сопротивления среды; dч – диаметр частицы, м.
Рисунок 5.2 – Проекция лобового сечения частицы
где ∆р – перепад давлений, преодолеваемый движущимися телами, Н/м2. Таким образом, коэффициент сопротивления пропорционален критерию Эйлера, который характеризует отношение перепада статического давления в потоке к его кинетической энергии и зависит от модифицированного критерия Рейнольдса и формы частицы. Модифицированный критерий Рейнольдса высчитывается по формуле где mср – коэффициент вязкости сплошной среды, Па∙с. Величина сопротивления преимущественно определяется явлениями, протекающими в пограничном слое, который окружает частицу и движется с такой же скоростью, что и сама жидкость (свойство жидкости – адгезия).
2) Переходный режим наблюдается при значениях 2 < Re ≤ 500, возникают силы инерции. Происходит отрыв потока, образуются вихри, возникает перепад давлений ΔР = Р1 – Р2 (Р1 – давление лобовой части частицы; Р2 – давление кормовой части). При этом режиме коэффициент сопротивления определяется по уравнению
3) Турбулентный режим (рисунок 5.4) наблюдается при значениях 500 < Re ≤ 2·105, сопротивление определяется только силами инерции, трение отсутствует. ξ = 0,44 = const. (5.10) Из сказанного следует, что зависимость коэффициента сопротивления от критерия Рейнольдса будет иметь вид, представленный на рисунке 5.5.
Рисунок 5.5 – Зависимость коэффициента сопротивления от критерия Рейнольдса (для шарообразной твердой частицы)
Для тел, форма которых отличается от шара, значения коэффициента сопротивления больше и зависят не только от модифицированного критерия Рейнольдса, но также и от коэффициента формы Ф, т.е.
где f – поверхность шара, м2; fш – поверхность шара, имеющего тот же объем, что и данная частица с поверхностью f, м2.
Классификация отстойников Аппараты, которые применяются для осаждения, называются отстойники. Различают отстойники: непрерывного действия – все процессы протекают непрерывно; полунепрерывного действия – подача разделяемой смеси и вывод очищенной сплошной фазы проводят непрерывно, удаление сгущенной дисперсной фазы – периодически; периодического действия – все процессы протекают периодически. Для разделения суспензий применяются одноярусные отстойники непрерывного действия с гребковой мешалкой (рисунок 5.7). Диаметр нормализованных аппаратов составляет от 1,8 до 30 м, в некоторых случаях может быть до 100 м. Для увеличения эффективности разделения и экономии производственных площадей применяются многоярусные отстойники, представляющие собой несколько отстойников, поставленных друг на друга и имеющих общий вал для гребковых мешалок.
Рисунок 5.7 – Одноярусный отстойник непрерывного действия с гребковой мешалкой
Отстойник непрерывного действия с коническими полками изображен на рисунке 5.8. К достоинствам отстойников этого типа относятся отсутствие движущихся частей и простота обслуживания. Для разделения эмульсий используется отстойник, схема которого представлена на рисунке 5.9. Главным условием эффективной работы этого аппарата являются ламинарные или близкие к нему движения жидкости в корпусе аппарата. Общими достоинствами описанных аппаратов является простая конструкция (низкие капитальные затраты) и низкое гидравлическое сопротивление (низкие экономические затраты). Недостаток – низкая степень разделения.
Расчет отстойников Отстойник непрерывного действия для разделения суспензий представляет собой полый резервуар цилиндрической или прямоугольной формы (рисунок 5.10).
Необходимым условием является то, что время пребывания частиц (τ пр) в аппарате должно быть больше времени осаждения (τ ос). τпр = L/wж ; Определив объемный расход осветленной жидкости по уравнению расхода, получим тогда
Из формулы (5.27) следует общий вывод: производительность отстойника не зависит от высоты аппарата, а определяется только скоростью и поверхностью осаждения (рисунок 5.11). При выводе уравнения (5.27) не учитывался ряд обстоятельств, ухудшающих процесс отстаивания в реальных промышленных аппаратах, поэтому при инженерных расчетах рекомендуется увеличивать значения поверхности на 30…35 %. Необходимо отметить, что при создании отстойной аппаратуры возможности для интенсификации процесса незначительны. Для того чтобы интенсифицировать процесс осаждения, необходимо: а) увеличить диаметр частиц, для этого используют такие методы, как коагуляция, флокуляция; б) подогреть суспензию, так как при повышении температуры наблюдается уменьшение плотности и вязкости сплошной среды; в) заменить силовое поле на центробежное. В гравитационных отстойниках на частицу действует сила тяжести: Таким образом, центробежная сила больше силы тяжести в Кр раз, и эта величина называется фактором разделения или центробежным фактором. Фактор разделения является важной характеристикой при осаждении в центробежном поле, т.к. разделяющая способность аппаратов при прочих равных условиях зависит от его величины. Он показывает, во сколько раз скорость осаждения частиц твердой фазы в центробежном поле больше скорости подобного процесса в гравитационном поле.
Фильтрование
Процессом фильтрования в химической промышленности называют разделение суспензий или пылей с помощью пористой перегородки – фильтра, способной задерживать взвешенные частицы, находящиеся в жидкости или газе. Фильтрование может обеспечить почти полную очистку жидкости или газа от взвешенных частиц и в этом отношении имеет преимущество перед процессами осаждения. Принципиальная схема процесса представлена на рисунке 5.12. Различают следующие виды фильтрования: а) фильтрование с образованием осадка на фильтровальной перегородке; б) фильтрование с закупориванием пор фильтровальной перегородки. Движущей силой процесса фильтрования является разность давлений ΔР. Это может быть гидростатическое давление, избыточное давление над перегородкой, вакуум под перегородкой, центробежное поле (фильтрующая центрифуга, рисунок 5.13).
1 – фильтровальная перегородка; 2 – осадок Рисунок 5.12 – Схема фильтрования
В качестве фильтрующих материалов в промышленных аппаратах применяют естественные и искусственные зернистые и пористые тела: песок, графит, ткани, сетки, пористые пластические массы и т.д.
Классификация фильтров
Промышленные фильтры классифицируются по различным признакам: а) по принципу действия на фильтры периодического и непрерывного действия; б) по величине рабочего давления – на вакуум-фильтры и фильтры, работающие под давлением; в) по технологическому признаку фильтры подразделяют на жидкостные (для разделения суспензий), фильтрующие центрифуги (также для разделения суспензий) и газовые (для очистки газов). В фильтрах периодического действия осадок удаляется после прекращения процесса фильтрования, в фильтрах непрерывного действия – по мере необходимости без остановки процесса. Все рассмотренное выше относилось к фильтрованию суспензий. Процесс фильтрования может быть применен также для разделения газовых неоднородных систем. Принцип действия таких аппаратов тот же, что и для разделения суспензий, однако при очистке газов в большинстве случаев применяют фильтрование с закупориванием пор. Расчеты газовых фильтров основываются исключительно на экспериментальных данных. Существуют различные типы фильтровальных перегородок, выбор которых определяется размером дисперсных частиц, температурой газа, его химическими свойствами, а также допустимым гидравлическим сопротивлением.
Тяжести
Для разделения газовых неоднородных систем в гравитационном поле применяются газоходы и пылеосадительные камеры (рисунок 5.15). Пылеосадительные камеры испо-льзуются для грубой (предварительной) очистки сильно запыленных газов, содержащих частицы размером не менее нескольких десятков микрометров. Достоинствами полочных камер являются простота их конструкции, небольшое гидравлическое сопротивление, а недостатком - громоздкость, обусловленная малой скоростью осаждения частиц под действием силы тяжести.
Расчет циклона
При расчете циклона обычно заданы следующие параметры: – производительность V, м3/с; – минимальный диаметр частиц dmin; – температура газа tгаза; – содержание дисперсной фазы а, % и форма частиц. Расчет циклона ведется в следующем порядке: 5.6.3.1 Выбирают марку циклона (т.е. задаются коэффициентом сопротивления ξ, который является постоянным для данного циклона независимо от его диаметра). 5.6.3.2 Определяют скорость движения газа в циклоне через гидравлическое сопротивление циклона, которое можно представить уравнением
5.6.3.3 Выбирают оптимальное значение величины Δp/ρ для данного типа циклона и определяют скорость воздушного потока в циклоне wц: 5.6.3.4 По уравнению расхода определяют диаметр циклона:
5.6.3.5 Для полученного значения диаметра по нормалям находят все остальные размеры. 5.6.3.6 Проверяют, может ли обеспечить выбранный циклон достаточную степень очистки для частиц заданного диаметра. Если степень очистки будет недостаточна, необходимо внести корректировку в выбираемые параметры (тип циклона, Δp/ρ, ξ). Для увеличения производительности требуются циклоны с большим диаметром, а это, в свою очередь, снижает степень очистки. В таких случаях применяют батарейные циклоны, в которых организуется совместная параллельная работа циклонов меньшего диаметра (рисунок 5.19).
1 – корпус; 2 – газораспределительная камера; 3 – корпуса циклонных элементов; 4 – трубные решетки; 5 – бункер для пыли Рисунок 5.19 – Батарейный циклон
Мокрая очистка газов Путем смачивания и поглощения частиц пыли жидкостью достигается высокая степень извлечения пыли из газа. Мокрая очистка газа особенно желательна в тех случаях, когда необходимо охлаждение газа независимо от его очистки. При охлаждении влажного газа водяные пары конденсируются на содержащихся в нем пылинках (центры конденсации), вследствие чего увеличивается вес пылинок и облегчается выделение их из газа. Выделение пыли в мокрых пылеуловителях происходит под действием: – сил тяжести (при прямолинейном движении газа через аппарата); – сил инерции (при резком изменении направления газового потока); – центробежных сил (при вводе газа в аппарат с большой скоростью по касательной к внутренней поверхности аппарата). В последнем случае достигается наиболее тщательная очистка газа. Физическая сущность процесса показана на рисунке 5.21 и заключается в том, что запыленный газ контактирует с каплями жидкости, которые оседают, увлекая за собой твердые частицы. Существуют две модели мокрой очистки. Первая – это увеличение твердых частиц каплями жидкости – возникает в результате адгезии жидкости к поверхности частиц или в результате набухания частиц при поглощении влаги. Необходимым условием для этого является возможность смачивания частиц жидкостью.
Рисунок 5.21 – Схема проведения мокрой очистки газа
Вторая – фильтрование через зернистый слой. При этом капли воды рассматриваются как зерна. Смачивание и поглощение пыли водой производится тремя способами: 1) при стекании воды пленкой по внутренним стенкам аппарата (насадочные и центробежные скрубберы); 2) при разбрызгивании воды по всему объему (полые скрубберы, скрубберы Вентури); 3) при пропускании газа через слой жидкости (барботажные пылеуловители); 4) при комбинировании первых двух способов. Мокрую очистку газов применяют в тех случаях, когда наряду с вышеуказанными ограничениями хорошо отработаны мероприятия по предотвращению брызгоуноса и утилизации отработанных стоков. Достоинства мокрой очистки газов: – низкие эксплуатационные и капитальные затраты; – высокая степень разделения; – возможность совмещения очистки с другими процессами (например, с абсорбцией, осаждением). Недостатки: – из неоднородной системы «газ – твердое тело» получается другая неоднородная система «жидкость – твердое тело», следовательно, требуется дополнительное оборудование; – большой расход жидкости; – увлажнение и охлаждение газов, что не всегда допустимо; – большой брызгоунос; – высокая коррозия оборудования. Аппараты для очистки газов При анализе этой аппаратуры можно увидеть, что рост эффектив-ности обычно связан с увеличением затрат энергии и размеров аппаратов. Пылеосадительные камеры и циклоны по капитальным и эксплуатационным затратам предпочтительнее других аппаратов, но они улавливают лишь крупные частицы. Поэтому их используют для предварительной очистки газов перед электрофильтрами и рукавными фильтрами. Электрофильтры и рукавные фильтры дают лучший эффект очистки от пыли при меньших скоростях газа, то есть при использовании аппаратов большего размера. Циклоны и скрубберы Вентури обеспечивают тем более эффективное разделение, чем больше их гидравлическое сопротивление, то есть чем больше затраты энергии на перекачивание газа. Поэтому в каждом случае следует выбирать аппарат с учетом конкретных условий. В электрофильтрах можно добиться высокой степени очистки газа, в том числе и от очень мелких частиц. Однако они часто требуют предварительной подготовки газа, непригодны для отделения частиц с небольшим удельным электрическим сопротивлением. Рукавные фильтры дают высокую степень очистки для частиц любого размера более 1 мкм, однако способны работать при небольшой запыленности исходного газа; требуют поддержания его температуры в определенных пределах. По капитальным затратам рукавные фильтры дешевле электрофильтров, но расходы на их эксплуатацию больше. Аппараты мокрой очистки эффективны для очистки газов от пыли средней дисперсности. Наиболее целесообразно их применение, если желательно увлажнение газов. Эти аппараты достаточно просты в изготовлении, сравнительно дешевы, эксплуатационные расходы невелики. Однако их использование сопряжено с большим расходом воды, требуется серьезная защита аппаратов от коррозии.
Образование неоднородных систем
Наряду с уже рассмотренными гидромеханическими процессами в химической технологии большое значение имеют еще два гидромеханических процесса: перемешивание в жидкой среде и псевдоожижение твердого зернистого и пылевидного материала.
Перемешивание Перемешивание – это процесс многократного относительного перемещения макроскопических объемов среды. Цели перемешивания определяются назначением процесса. В случае гомогенизации, приготовления суспензий, нагревания или охлаждения гомогенной среды перемешивание используют в основном для выравнивания температурного и концентрационного полей, благодаря чему повышается скорость химической реакции. В случае гетерогенных процессов, реакция в которых складывается из нескольких последовательных стадий и если химическая реакция является определяющей, то перемешивание используется для выравнивания концентрационного поля. В связи с этим необходимо обеспечить интенсивную циркуляцию потока. Перемешивание увеличивает степень турбулентности системы, что приводит к уменьшению толщины диффузионного пограничного слоя, а это, в свою очередь, обеспечивает увеличение и непрерывность обновления поверхности межфазного контакта, что вызывает существенное ускорение тепло- и массообменных процессов. Перемешивание применяют в процессах абсорбции, выпаривания, экстрагирования и других процессах химической, нефтяной, пищевой промышленности. Процесс перемешивания характеризуется интенсивностью и эффективностью, а также расходом энергии на его проведение. Интенсивность перемешивания – это количество энергии, вводимое в единицу времени в единицу объема перемешивания среды. Чем выше интенсивность перемешивания, тем больше энергетические затраты. Интенсивность перемешивания обусловливает характер движения жидкости в аппарате. Эффективность перемешивания – это параметр, характеризующий качество проведения процесса. Существуют следующие виды перемешивания: механическое перемешивание с помощью мешалки, пневматическое (барботажное) перемешивание, циркуляционное перемешивание с помощью насоса, статическое перемешивание – перемешивание в потоке. Механическое перемешивание получило наибольшее распространение в химической промышленности. Перемешивание осуществляется с помощью мешалок, которые представляют собой вращающийся вал с закрепленными на нем лопастями различной формы. Вращение мешалок вызывает движение жидкости, структура потока в которой зависит от типа аппарата и типа мешалки. Так, для пропеллерной мешалки структура потока показана на рисунке 5.22. При вращении мешалок образуется воронка, которая снижает эффективность перемешивания. Для уменьшения негативного влияния воронки в аппарате устанавливаются отражательные перегородки.
Работу механической мешалки можно описать с помощью уравнений гидродинамики.
где Здесь dм – диаметр мешалки, м; n – частота вращения мешалки, с-1. Здесь N – энергия, потребляемая мешалкой, Вт; Vсек – расход жидкости, создаваемый мешалкой, м3/с. Решив совместно эти уравнения, после преобразований получим так называемый критерий мощности мешалки
Установлено, что расход мощности на перемешивание зависит также от вязкости жидкости μ, размеров аппарата – диаметра D, высоты слоя жидкости Н, расстояния мешалки от дна hм, следовательно, общая функция для определения расхода мощности будет выражаться следующим образом: Порядок расчета мешалок: 1) выбирают тип мешалки; 2) выбирают диаметр мешалки и число оборотов; 3) определяют критерий Рейнольдса; 4) определяют критерий мощности по зависимости числа Рейнольдса; 5) определяют энергию, потребляемую мешалкой, по уравнению Достоинства мешалок: – высокая эффективность; – достаточно низкая потребляемая энергия. Недостатки мешалок: – сложность использования в сильно агрессивных средах; – сложность изготовления уплотнительных устройств. Пневматическое перемешивание осуществляется пропусканием газа через жидкость, для чего устанавливают газораспределительную решетку или используют барботер, который представляет собой расположенные по дну аппарата трубы с отверстиями, с помощью которых осуществляется барботаж газа через слой обрабатываемой жидкости (рисунок 5.23). Подобное перемешивание является малоинтенсивным процессом. Расход энергии при этом выше, чем при механическом перемешивании. Пневматическое перемешивание применяется в следующих случаях: когда допустим контакт газа и жидкости; при наличии маловязких жидкостей; при работе с агрессивными средами. Пневматическое перемешивание не применяется для обработки летучих жидкостей в связи со значительными потерями перемешиваемого продукта.
Рисунок 5.23 – Схема барботажного смесителя Циркуляционное перемешивание – это многократное перемещение жидкости через схему: аппарат – циркуляционный насос – аппарат, то есть перемешивание жидкости происходит по замкнутому контуру. Недостатком такого вида перемешивания является низкая эффективность. Статическое перемешивание. Для смешения потоков жидкости различного состава в последнее время начали применять статические смесители – устройства, не содержащие подвижных частей и устанавливаемые непосредственно на трубопроводах. Действие таких устройств основано на использовании энергии потока для создания высоких локальных напряжений сдвига. С этой целью в смесительной секции устанавливают различные турбулизирующие вставки (рисунок 5.24).
а - вставка из полуперегородок; б - диафрагмовая вставка; в - винтовая вставка; г - струйные смесители; 1, 2 – входы компонентов смеси; 3 – выход смеси Рисунок 5.24 – Схема устройств для перемешивания в потоке
Псевдоожижение Псевдоожижение – движение потока через слой зернистых или пористых материалов, а также насадочных элементов самых разнообразных размеров и форм. Если через слой зернистого материала, находящегося на решетке, снизу пропускать жидкость или газ, то при малых скоростях потока слой соприкасающихся друг с другом частиц остается неподвижным (рисунок 5.25а). С увеличением скорости потока промежутки между частицами увеличиваются. Частицы приходят в движение и ведут себя как пузырьки пара или газа в жидкости (рисунок 5.25б).
При движении через слой крупных пузырей наружная поверхность слоя разрывается, и группы частиц перемещаются вместе с пузырями по высоте слоя, способствуя интенсивному перемешиванию твердой фазы. В аппаратах малого диаметра пузыри, образующиеся вблизи газораспределительной решетки, часто сливаются в один большой пузырь, заполняющий все сечение аппарата, и слой частиц, расположенный выше такого пузыря, поднимается вверх, как поршень (рисунок 5.25г). Псевдоожижение дает возможность перемещать твердые частицы по трубам; уменьшает сопротивления в газовой фазе; выравнивает поля температур и концентраций. Однако при этом происходит уменьшение движущей силы процесса, появляется возможность проскока газа, происходит износ аппаратуры и возникает необходимость использования гидроочистительного оборудования. Структура зернистого слоя характеризуется: а) порозностью (долей свободного объема) б) удельной поверхностью в) эквивалентным диаметром каналов г) скоростью витания Условием перехода неподвижного слоя частиц во взвешенное состояние является равенство силы гидравлического сопротивления весу его частиц:
где S – площадь поперечного сечения аппарата, м2; Н – высота неподвижного слоя, м; ρт , ρ – плотности твердых частиц и псевдоожиженного агента, кг/м3. Схема расчета критической скорости Wкр
Экспериментальные данные для определения критической скорости могут быть представлены в форме зависимости критического числа Рейнольдса Reкр от критерия Архимеда Ar. Например, для слоя сферических частиц одинакового диаметра, принимая порозность e=0,4, уравнение для критерия Рейнольдса
где
Вопросы для самоконтроля 1. Перечислите основные свойства неоднородных систем. 2. Что представляют собой суспензии, эмульсии, аэрозоли? 3. Опишите зависимость коэффициента сопротивления от числа Рейнольдса при движении частицы в сплошной среде. 4. Под действием каких сил может проводиться осаждение? 5. Как определяют скорость осаждения частиц в гравитационном поле? 6. Дайте классификацию отстойников. 7. Что такое стесненное осаждение? 8. Каково назначение гребковой мешалки в отстойниках непрерывного действия? 9. Получите уравнения для определения поверхности осаждения отстойника. 10. Что является движущей силой фильтрования? 11. Получите дифференциальное уравнение фильтрования. 12. Что такое константы фильтрования? Как определяют и где их используют? 13. Дайте классификацию фильтров. 14. Какова физическая сущность процесса осаждения в центробежном поле? 15. Что такое фактор разделения в процессах осаждения под действием центробежных сил? 16. Приведите схему расчета циклона. 17. Опишите физическую сущность процесса осаждения в электрическом поле. 18. Перечислите достоинства и недостатки мокрой очистки газов. 19. Каковы принципы выбора аппарата для разделения неоднородных систем? 20. Что такое перемешивание? Какие виды перемешивания вы знаете? 21. Как определить необходимую мощность мешалки? 22. Как определяют скорость начала псевдоожижения? МОДУЛЬ 6. ТЕПЛОВЫЕ ПРОЦЕССЫ Тепловые процессы представляют собой обмен теплом между двумя теплоносителями. Тепловые процессы имеют большое значение в химической промышленности по следующим причинам. Большинство химических процессов являются эндо- или экзотермическими и, следовательно, управление химико-технологическими процессами (ХТП) в конечном счете сводится к подводу или отводу тепла. В себестоимости любой продукции химической промышленности стоимость тепловой энергии составляет значительную часть, т.е. эффективная организация тепловых процессов положительно сказывается на эффективности всего производства. Особенности тепловых процессов: а) широкий диапазон температур теплопереноса (от температур, близких к абсолютному нулю, до несколько тысяч градусов выше нуля); б) теплоперенос осуществляется в агрессивных средах и при высоких давлениях, что предъявляет особые требования к аппаратурному оформлению этих процессов. Основными характеристиками тепловых процессов являются: – количество передаваемого тепла, от которого зависят размеры теплообменных аппаратов; – основной размер теплообменного аппарата – теплопередающая поверхность (или поверхность теплообмена).
Греющие теплоносители
6.1.1.1 Топочные газы представляют собой газообразные продукты сгорания твердого, жидкого или газообразного топлива. Преимущества: отпадает использование промежуточных теплоносителей, нагрев до 1100°С. Недостатки: низкий коэффициент теплоотдачи от газа к стенке; сложность поддержания заданной температуры на заданном уровне; неравномерность обогрева теплообменной поверхности; выделение продуктов неполного сгорания, которые осаждаются на теплообменной поверхности, что приводит к увеличению сопротивления, корродирующего действия; достаточно жесткие условия нагрева за счет высоких перепадов температур между топочными газами и нагреваемой средой. 6.1.1.2 Нагревание электрическим током. Осуществляется в электропечах, которые подразделяются на электропечи сопротивления (прямого и косвенного действия) и печи индукционные и высокочастотные, в которых обогрев осуществляется током высокой частоты. Достоинства: получение любого желаемого температурного режима, который можно легко поддерживать и регулировать. 6.1.1.3 Водяной пар – самый распространенный промежуточный теплоноситель. Достоинства: высокий коэффициент теплоотдачи, легкость транспортировки на большие расстояния, возможность точного регулирования температуры за счет изменения давлений, доступность, большое количество выделяемого тепла при конденсации. Этот теплоноситель возможно использовать при температурах до 200°С. Недостатки: водяной пар обладает коррозийной способностью, при росте температуры растет давление. 6.1.1.4 Вода. Можно использовать горячую воду с температурой до 100 °С или перегретую до 300…350 °С. Достоинства: дешевизна, доступность. Недостатки: использование перегретой воды требует применения металлоемкой (толстостенной) аппаратуры и довольно сложной арматуры. 6.1.1.5 Высококипящие органические теплоносители (ВОТ) делятся на три основные группы: – органические теплоносители. К ним относятся глицерин, этиленгликоль, ароматические и неароматические масла, смеси органических веществ (смесь дифениловая). Температурный диапазон органических теплоносителей достигает 350 °С, при этом давление не меняется, т.е. остается постоянным. Эти теплоносители не ядовиты и не токсичны, однако являются пожаровзрывоопасными; термически не устойчивы (разлагаются на кокс и газы); – ионные теплоносители образуют кремнийорганические жидкости (силиконы) и расплавы солей или их смесей. В качестве примера можно привести нитрит-нитратную смесь (40 % NaNO2, 7 % NaNO3, 53 % KNO3). Предельная температура лежит в области 550 °С и ограничивается термической стойкостью этих теплоносителей. Теплоносители данной группы отличаются малой токсичностью и агрессивностью по отношению к конструкционным материалам; – жидкометаллические теплоносители представляют собой жидкие металлы и их сплавы и характеризуются самой высокой термостойкостью. Вследствие этого температурный диапазон обогрева находится в области до 2000 °С. В качестве примера жидкометаллических теплоносителей можно привести висмут, свинец, ртуть, натрий, литий, олово, кадмий. Большинство металлических теплоносителей огне-, пожаро- и взрывобезопасны и практически не воздействуют на малоуглеродистые и легированные стали. Исключение составляют калий и натрий, которые отличаются чрезвычайно высокой химической активностью и воспламеняются со скоростью взрыва. Главным недостатком этих теплоносителей является высокая токсичность их паров. Хладоагенты 6.1.2.1 Вода является самым распространенным хладоагентом. В промышленности используется артезианская вода – температура от 8 до 12 °С; открытый водоем – температура от 4 до 25 °С; оборотная вода – 30 °С. Достоинства: доступность, дешевизна, термически устойчива. Недостатки: коррозионная активность, температурный диапазон зависит от климатических и временных условий. 6.1.2.2 Низкотемпературные жидкости используют для создания температур ниже 5…20 °С, которые обычно не достигаются охлаждением водой. К числу таких теплоносителей относятся жидкий аммиак, фреоны, диоксид углерода, холодильные рассолы – водные растворы неорганических солей, например KCl, NaCl, CaCl (их температурный диапазон зависит от концентрации). При охлаждении холодильными рассолами и парами низкокипящих жидкостей пользуются холодильными установками. 6.1.2.3 Воздух по сравнению с водой более доступен, и несмотря на то, что он обладает значительно меньшим коэффициентом теплоотдачи и объемной теплоемкости, в современной технологии наблюдается тенденция к замене воды как охлаждающего агента воздухом. Воздух в отличие от воды не загрязняет поверхность теплоотдачи отложениями, не корродирует теплообменную аппаратуру, что положительно сказывается на увеличении срока службы воздушных холодильников. Наиболее широко воздух в качестве охлаждающего агента используется в смесительных теплообменниках – градирнях, являющихся основным элементом оборудования водооборотного цикла. Теплообменные аппараты
Теплообменные аппараты – это аппараты, предназначенные для передачи теплоты от одного теплоносителя, нагретого до более высокой температуры, к другому. При проектировании и конструировании теплообменных аппаратов необходимо учитывать многочисленные факторы, влияющие на процесс теплопередачи, и противоречивые требования, предъявляемые к теплообменникам (ТО). Теплообменные аппараты должны удовлетворять следующим требованиям: а) обеспечивать условия протекания технологического процесса; б) иметь возможно более высокий коэффициент теплопередачи; в) иметь низкие гидравлические сопротивления; г) обладать устойчивостью теплообменных поверхностей против коррозии; д) обеспечивать доступность поверхности теплопередачи для очистки; е) обладать технологичностью конструкции с точки зрения их изготовления; ж) обеспечивать экономичное использование материалов.
Таблица 6.2 - Рекомендуемые значения скоростей теплоносителей
Змеевиковые теплообменники | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 С погружными змеевиками С погружными змеевиками
Могут быть как с одним, так и с несколькими змеевиками |   С наружными змеевиками С наружными змеевиками
|
В погружных теплообменниках змеевики погружаются в жидкость, находящуюся в корпусе аппарата. Они имеют сравнительно небольшую поверхность теплообмена. Широко распространены теплообменники с наружными змеевиками, так как они позволяют проводить процесс при давлениях до 6 МПа.
Преимуществами змеевиковых теплообменников являются простота изготовления и доступность поверхности теплообмена для осмотра и ремонта. Недостатки: громоздкость и трудность внутренней очистки труб.
Методика теплового расчета
Целью теплового расчета является определение поверхности теплообмена совместным решением уравнений теплопередачи и теплового баланса при заданных расходах теплоносителей и температурных условиях (при этом задаются значения конечных температур теплоносителей).
Площадь теплопередающей поверхности определяют методом последовательных приближений, при этом для выбранной конструкции аппарата величина теплопередающей поверхности находится из основного уравнения теплопередачи:
 (6.1)
(6.1)
Тепловой поток (Q) определяют из уравнения теплового баланса.
Движущую силу рассчитывают исходя из теплового режима аппарата, например
 (6.2)
(6.2)
Значения коэффициента теплопередачи в первом приближении принимают сугубо ориентировочно на основании опытных данных.
Находят ориентировочно площадь теплопередающей поверхности и вычерчивают эскиз аппарата.
На следующем этапе рассчитывают значения коэффициентов теплоотдачи, термического сопротивления стенки и коэффициента теплопередачи применительно к выбранным конструкции и размерам аппарата.
По вычисленному коэффициенту теплопередачи уточняют величину площади теплопередающей поверхности и эскиз аппарата.
Расчет ведется до совпадения принятых величин и величин, полученных в результате расчета (расхождение не должно превышать 3…5 %).
Этапы расчета:
а) проектировочный расчет:
– выбор конструкции аппарата, определяющих размеров (диаметры, длины, высоты по стандартам), скоростей и места расположения теплоносителей (трубное, межтрубное);
– определение тепловой нагрузки  ;
;
– составление теплового баланса Q = Q1= Q2, из которого можно определить расход теплоносителя;
– определение параметров температурного режима процесса (Δtcp);
– выбор физических параметров теплоносителей;
– приближенная оценка коэффициентов теплоотдачи, теплопередачи и поверхности теплообмена;
– выбор типа нормализованного варианта конструкции, площади теплопередающей поверхности (Fнорм), диаметра внутренних труб, высоты труб и других параметров;
б) уточненный или проверочный расчет, необходимость которого возникает, например, если в результате проектировочного расчета был выбран нормализованный аппарат со значительным запасом поверхности:
– при известных поверхности, начальных температурах теплоносителей и их расходах определяют количество тепла и поверхность теплообмена (Fрасч);
– сопоставляют значения Fрасч и Fнорм.;
– тепловой расчет должен быть увязан с конструкционным и гидравлическим расчетами;
в) технико-экономический расчет;
г) выбор оптимального варианта.
Выпаривание
Выпаривание – это процесс концентрирования нелетучих или малолетучих веществ путем удаления летучего растворителя в виде пара при температуре кипения. Выпаривание отличается от испарения тем, что испарение происходит с поверхности при различных температурах (даже ниже температуры кипения), а выпаривание происходит из всего объема кипящего раствора.
Выпаривание используется для повышения концентрации раствора или для получения чистых труднолетучих растворов. Скорость процесса выпаривания определяется скоростью подвода тепла.
Для осуществления процесса выпаривания необходимо теплоту от теплоносителя передать кипящему раствору, что возможно лишь при наличии разности температур между ними. При расчете процесса выпаривания эту разность температур между теплоносителем и кипящим раствором называют полезной разностью температур.
Тепло для выпаривания можно подводить любыми теплоносителями, применяемыми при нагревании. Однако в большинстве случаев в качестве греющего агента при выпаривании используют насыщенный водяной пар, который называют греющим, или первичным.
Первичным служит пар, получаемый из парогенератора, либо отработанный пар, либо пар промежуточного отбора паровых турбин. Пар, образующийся при выпаривании кипящего раствора, называется вторичным.
Тепло, необходимое для выпаривания раствора, обычно подводят через стенку, отделяющую теплоноситель от раствора. В некоторых случаях концентрирование растворов осуществляют при непосредственном соприкосновении выпариваемого раствора с топочными газами или другими газообразными теплоносителями.
Таким образом, выпаривание является типичным процессом переноса тепла. Основное отличие процесса выпаривания от тепловых процессов заключается в особенностях его аппаратурного оформления и методе расчета выпарных установок.
Процесс выпаривания может проводиться под атмосферным давлением, вакуумом или под избыточным давлением.
Выбор давления связан со свойствами выпариваемого раствора и возможностью использования тепла вторичного пара.
В случае выпаривания под атмосферным давлением вторичный пар чаще всего выбрасывается в атмосферу и не используется. Такой способ является простым, но экономически невыгодным.
Выпаривание под вакуумом позволяет уменьшить температуру кипения раствора, поэтому можно выпаривать нетермостойкие растворы, можно выпаривать растворы с высокой температурой кипения, например, растворов щелочей, а также концентрировать растворы с использованием теплоносителя (пара) невысоких параметров; увеличивается полезная разность температур, а следовательно, уменьшается поверхность теплообмена.
Применение вакуума дает возможность использовать в качестве греющего агента, кроме первичного пара, вторичный пар самой выпарной установки, что снижает расход первичного пара и, следовательно, затраты на проведение процесса.
Недостатками выпаривания под вакуумом являются необходимость конденсации вторичного пара и применение вакуум-насоса для откачки неконденсирующегося пара, что ведет к увеличению эксплуатационных расходов и удорожанию установки.
В случае выпаривания под давлением выше атмосферного вторичные пары имеют повышенные параметры и их можно использовать как для выпаривания, так и для других нужд, не связанных с процессом выпаривания. Если этот пар используется для посторонних нужд, то его называют экстра-паром. Отбор экстра-пара позволяет лучше использовать тепло, чем при выпаривании под вакуумом. Однако подобное выпаривание сопряжено с повышением температуры кипения раствора. Поэтому данный способ применяется лишь для выпаривания термостойких веществ. Кроме того, для выпаривания под давлением необходимы греющие агенты с более высокой температурой.
Виды выпаривания
Существует несколько способов выпаривания:
а) простое однокорпусное выпаривание;
б) многократное, или многокорпусное выпаривание. Это выпарные установки, состоящие из нескольких выпарных аппаратов, или корпусов, в которых вторичный пар каждого предыдущего корпуса направляется в качестве греющего в последующий корпус;
в) выпаривание с тепловым насосом, применение которого позволяет сэкономить первичный пар.
Два последних способа энергетически выгодны при больших производительностях (от нескольких кубических метров выпариваемого раствора в час и выше), что характерно для промышленности, где выпаривание проводят по непрерывному принципу. В аппаратах непрерывного действия обычно создают условия для интенсивной циркуляции раствора, то есть в таких аппаратах гидродинамическая структура потоков близка к модели идеального смешения, поэтому концентрация раствора в таких аппаратах ближе к конечной, что приводит к ухудшению условий теплопередачи.
 Периодическое выпаривание проводят при малых производительностях и необходимости упаривания раствора до существенно высоких концентраций.
Периодическое выпаривание проводят при малых производительностях и необходимости упаривания раствора до существенно высоких концентраций.
Процесс выпаривания проводят в выпарных аппаратах (ВА). Схематично процесс вы-паривания можно представить, как показано на рисунке 6.7.
Рассмотрим принципиальную схему одиночного непрерывно действующего выпарного аппарата с естественной циркуляцией раствора на примере аппарата с внутренней центральной циркуляционной трубой (рисунок 6.8).
Поверхность теплопередачи на единице объема в маленькой трубке больше, раствор в ней кипит лучше, поэтому там образуется парожидкостная смесь с большим содержанием вторичного пара. В большой трубе жидкость опускается, а в кипятильных трубках поднимается. Происходит циркуляция, с увеличением циркуляции увеличивается коэффициент теплоотдачи.
Кроме этого, циркуляция предотвращает отложение солей на кипятильных трубах.

Из кипятильных труб пар выбрасывается с большой скоростью и ударяется о брызгоотбойник. Большие капли возвращаются вниз, мелкие улавливаются каплеуловителем и возвращаются в раствор.
Достоинством однокорпусного выпарного аппарата является простота конструкции, а недостатком – большие энергозатраты, поскольку пар выбрасывается в атмосферу.
Расчет выпарного аппарата
Технологический (тепловой) расчет выпарного аппарата при его проектировании сводится к определению поверхности нагрева при заданных условиях работы выпарного аппарата (рисунок 6.16). Расчет заключается в решении систем уравнений материального, теплового балансов и теплопередачи с учетом дополнительных условий.
При расчете заданы обычно следующие параметры:
Sн – производительность аппарата, кг/с;
хн, хк – соответственно начальная и конечная массовые доли растворенного вещества.
Этапы расчета выпарного аппарата:
а) определить количество растворителя W, которое необходимо выпарить, чтобы повысить концентрацию от хн до хк ;
б) определить количество теплоты, которое необходимо для выпаривания этого количества растворителя;
в) определить расход теплоносителя (в большинстве случаев пара) Dг.п.;
г) определить поверхность нагрева F, м2;
д) выбрать стандартный выпарной аппарат по стандарту.
Из-за большого количества неизвестных величин расчет становится громоздким. Поэтому его выполняют методом последовательных приближений. Задаются значениями соответствующих величин, выполняют расчет и в случае существенного расхождения принятых и рассчитанных величин принимают новые значения тех же величин для последующего приближения. Предварительно выполняют приближенный расчет, который позволяет выяснить ориентировочные показатели работы аппарата.
Количество выпариваемого раствора W определяют исходя из общего балансового соотношения (Пр-Ух+Ис-Ст=Нак).
Поскольку рассматривается непрерывный процесс, количество субстанции, которая приходит в аппарат, равно количеству субстанции, которая уходит Пр=Ух. То есть материальный баланс выпарной установки будет выглядеть так:
 (6.21)
(6.21)
или по растворенному веществу
 . (6.22)
. (6.22)
Сопоставив уравнения (6.21) и (6.22), получим
 . (6.23)
. (6.23)
Таким образом, из уравнения (6.23) можно найти количество выпариваемой воды, если задана конечная концентрация раствора; или конечную концентрацию раствора при заданном количестве выпаренной воды.

с – удельная теплоемкость, Дж/кгК; t – температура, К; Н – энтальпия, Дж/кг; G – расход раствора, кг/с; D – расход пара, кг/с; Q – количество тепла, Вт; х – концентрация, %; φ – влажность пара, %
Рисунок 6.16 – К расчету поверхности нагрева
выпарного аппарата
Количество теплоты и расход греющего пара определяют из теплового баланса (Пр=Ух).
| Приход теплоты: | Уход теплоты: |
| – с греющим паром | – с упаренным раствором  ; ;
|
– со вторичным паром  ; ;
| |
| – с исходным раствором | – с паровым конденсатом  ; ;
|
– теплота концентрирования  ; ;
| |
– потери в окружающую среду  . .
|
Из уравнения теплового баланса находят расход греющего пара на выпаривание:
 . (6.24)
. (6.24)
Таким образом, греющий пар используется для нагревания исходного раствора до температуры кипения, испарения влаги из раствора с учетом теплового эффекта концентрирования раствора и тепловых потерь в окружающую среду.
В случае, если раствор поступает в аппарат при температуре кипения, отсутствуют тепловой эффект концентрирования раствора и тепловые потери в окружающую среду, удельный расход пара можно определить по упрощенной формуле:
 . (6.25)
. (6.25)
Движущую силу процесса выпаривания определяют по формуле
 . (6.26)
. (6.26)
Коэффициент теплопередачи
 (6.27)
(6.27)
Поверхность греющей камеры
 . (6.28)
. (6.28)
Выбор числа корпусов
 Практически выбор числа корпусов наиболее рационально проводить исходя из технико-экономических соображений. С увеличением числа корпусов достигается все большая экономия греющего пара и снижается общая стоимость пара, необходимого для выпаривания (эксплуатационные расходы). Одновременно с увеличением числа корпусов возрастают капитальные затраты и соответственно расходы.
Практически выбор числа корпусов наиболее рационально проводить исходя из технико-экономических соображений. С увеличением числа корпусов достигается все большая экономия греющего пара и снижается общая стоимость пара, необходимого для выпаривания (эксплуатационные расходы). Одновременно с увеличением числа корпусов возрастают капитальные затраты и соответственно расходы.
Условно зависимость капитальных и эксплуатационных затрат от числа корпусов можно изобразить так, как на рисунке 6.17.
Стоимость капиталь-ных вложений и эксплуатационные затраты определяют суммарные затраты. Минимум этих затрат соответствует оптимальному числу корпусов.
Вопросы для самоконтроля
1. Назовите виды теплоносителей для подвода теплоты в теплообменную аппаратуру.
2. Перечислите достоинства и недостатки нагрева насыщенным водяным паром.
3. Какие методы и теплоносители можно использовать для нагрева до высоких температур?
4. Охарактеризуйте водооборотные циклы химических предприятий.
5. Дайте классификацию теплообменных аппаратов.
6. Опишите устройство и принцип действия кожухотрубчатых теплообменников.
7. Приведите классификацию кожухотрубчатых теплообменников.
8. Что представляют собой змеевиковые теплообменники?
9. Когда используют теплообменники с оребренными трубами?
10. Покажите схему проектного расчета поверхностных теплообменников.
11. Покажите сущность процесса выпаривания, области его практического применения.
12. Раскройте конструктивные особенности выпарных аппаратов, их основные отличия от теплообменников.
13. Что понимается под полезной разностью температур выпарного аппарата? В чем различие при расчете средней движущей силы в теплообменниках и выпарных аппаратах?
14. Что понимают под вторичным паром и экстра-паром?
15. Составьте материальный и тепловой баланс однокорпусной выпарной установки.
16. Постройте температурный график выпарной установки.
17. В чем принципиальные различия прямоточной и противоточной схем выпаривания?
18. Дайте классификацию выпарных аппаратов.
19. Как выбирают число корпусов выпарной установки?
20. С какой целью в выпарных аппаратах применяют принудительную циркуляцию выпариваемого раствора?
21. Перечислите вспомогательное оборудование для выпарной установки.
22. Что представляет собой барометрический конденсатор?
Абсорбция
Абсорбция – это процесс избирательного поглощения растворимого компонента (абсорбтива) газовой или паровой смеси жидкостным поглотителем – абсорбентом. Обратный процесс – выделение из абсорбента растворенных в нем газов носит название десорбции.
В химической технологии абсорбция используется для получения готового продута (абсорбция хлороводорода водой в производстве соляной кислоты, окислов азота в производстве азотной кислоты), выделения ценных компонентов из газовых смесей (получение бензола из коксового газа, ацетилена из газов крекинга), улавливания вредных и нефтяного газов от сероводорода.
Различают два вида абсорбции:
а) физическую абсорбцию, когда поглощение газа жидкой фазой может происходить за счет растворения его в абсорбенте, при этом не происходит химического взаимодействия между поглотителем и поглощаемым веществом;
б) хемосорбцию, когда поглощение газа жидкой фазой происходит в результате его химического взаимодействия с абсорбентом, парциальное давление над поглотителем определяется константами химических взаимодействий.
При выборе абсорбента к нему предъявляется ряд требований:
– селективность – способность избирательного поглощения извлекаемого компонента;
– максимальная растворимость поглощаемого компонента в жидкой фазе (это приведет к уменьшению расхода абсорбента);
– низкая летучесть во избежание его потерь с уходящим газом;
– пожаро-, взрывобезопасность, дешевизна, доступность, нетоксичность.
Кинетика процесса
Абсорбции
Скорость процесса абсорбции может быть представлена по аналогии с прошлым семестром, так, в соответствии с единым кинетическим законом примени-тельно к абсорбции уравнение массопередачи запишется:
 (7.12)
(7.12)
Коэффициенты массопередачи определяются по уравнениям
 (7.13)
(7.13)
и
 , (7.14)
, (7.14)
где  – коэффициент массоотдачи от потока газа к поверхности контакта фаз, м/с;
– коэффициент массоотдачи от потока газа к поверхности контакта фаз, м/с;
 – коэффициент массоотдачи от поверхности контакта фаз к потоку абсорбента, м/с.
– коэффициент массоотдачи от поверхности контакта фаз к потоку абсорбента, м/с.
Конструкции абсорберов
Выбор типа абсорбера определяется видом контакта потоков газа и жидкости. Для создания развитой поверхности контакта фаз газ пропускают через колонну с насадкой, орошаемой жидкостью, – насадочные абсорберы (рисунок 7.7), либо через аппарат, в котором жидкость распыливается форсунками или вращающимися механическими элементами – распыливающие абсорберы (рисунок 7.8). Для хорошо растворимых газов используют поверхностные абсорберы, в которых газ пропускают над поверхностью жидкости или над поверхностью текущей пленки жидкости – пленочные (рисунок 7.9). Кроме того, газ может распределяться в жидкости в виде струек и пузырьков – барбо  тажные абсорберы (рисунок 7.10).
тажные абсорберы (рисунок 7.10).
К абсорбционным аппаратам предъявляются следующие требования:
– абсорбер должен обладать развитой поверхностью контакта фаз;
– иметь большие предельные нагрузки по жидкости, газу или пару;
– иметь небольшое гидравлическое сопротивление;
– иметь небольшую стоимость и т.д.
Наиболее широкое распространение получили насадочные и барботажные тарельчатые абсорберы.


а б
а – пленочный каскадный абсорбер; б – трубчатый абсорбер
Рисунок 7.9 – Пленочные абсорберы

а – с неорганизованным переливом жидкости;
б – с переливными устройствами
Рисунок 7.10 – Барботажные абсорберы
Насадочные аппараты
Насадочные абсорберы представляют собой колонны, заполненные насадкой. Жидкость стекает по поверхности насадочных тел в виде тонкой пленки. Контакт газа со стекающей жидкостью происходит по поверхности смоченной насадки, поэтому насадка должна иметь как можно большую поверхность в единице объема.
Для того чтобы насадка работала эффективно, она должна удовлетворять следующим основным требованиям:
– обладать большой поверхностью в единице объема;
– хорошо смачиваться орошающей жидкостью;
– оказывать малое гидравлическое сопротивление газовому потоку;
– равномерно распределять орошающую жидкость;
– быть стойкой к химическому воздействию жидкости или газа, движущихся в колонне;
– иметь малую плотность;
– обладать высокой механической прочностью;
– иметь невысокую стоимость.
Насадок, полностью удовлетворяющих всем указанным требованиям, не существует, так как, например, увеличение удельной поверхности насадки влечет за собой увеличение гидравлического сопротивления аппарата и снижение предельных нагрузок. В промышленности применяют разнообразные по форме и размерам насадки, которые в той или иной мере удовлетворяют требованиям, являющимся основными при проведении конкретного процесса. Практическое значение имеют хордовая и кольцевая насадки, спиральная и сетчатая металлические насадки.
При работе насадочных аппаратов наблюдаются следующие гидродинамические режимы: пленочный, подвисания, эмульгирования и режим захлебывания (рисунок 7.11).
Первый режим – пленочный – жидкость стекает в виде пленки. Этот режим наименее интенсивный, но наиболее распространен из-за низкого гидравлического сопротивления.
Второй – режим подвисания – жидкость задерживается в каналах насадки; скорость течения жидкости уменьшается, а толщина ее пленки и количество удерживаемой жидкости увеличиваются. Газ и жидкость наиболее турбулизованы, увеличивается коэффициент массопередачи.
Третий – режим эмульгирования – газ пробулькивает через жидкость; жидкость накапливается в свободном объеме насадки, соответствует максимальной эффективности насадочных колонн. Коэффициент массопередачи имеет наибольшее значение. Этот режим обладает недостатками: его трудно поддерживать, резко повышается гидравлическое сопротивление, снижается движущая сила процесса.
 Четвертый – режим уноса жидкости – режим нерабочий.
Четвертый – режим уноса жидкости – режим нерабочий.
Основным показателем работы насадочной колонны является гидравлическое сопротивление, которое определяет энергетические затраты на перемещение газа через аппарат и служит важным показателем режима работы и состояния насадки в колонне.
Тарельчатые аппараты
Представляют собой вертикальные цилиндрические колонны, в которых на определенном расстоянии друг от друга по высоте колонны размещены горизонтальные перегородки – тарелки для развития поверхности контакта фаз.
Процесс массопереноса в тарельчатых колоннах осуществляется в газожидкостной среде, которая создается на тарелках. Следовательно, процесс проходит ступенчато, в отличие от насадочных колонн, в которых массоперенос происходит непрерывно.
По способу слива жидкости с тарелки, аппараты подразделяются на колонны с тарелками со сливными устройствами и без сливных устройств - «провальные» (рисунок 7.12).
В «провальных» тарелках отсутствуют переливные трубы. При этом одновременно с взаимодействием фаз на тарелке происходит сток жидкости на нижерасположенную тарелку – «проваливание» жидкости.
Тарелки со сливными устройствами бывают колпачковые (рисунок 7.12а), ситчатые (рисунок 7.12б) и клапанные (рисунок 7.12в). Режимы работы тарельчатых колонн, как и насадочных, определяются скоростью газа.
Пузырьковый (барботажный) режим работы характеризуется небольшими скоростями газа, газ в виде отдельных пузырьков движется через слой жидкости.
Пенный режим возникает при увеличении скорости газа, когда на тарелке образуется газожидкостная система - пена.
 Струйный (инжекторный) режим возникает при дальнейшем увеличении скорости газа, который проходит через газожидкостной слой в виде газовых струй, не разрушаясь. Поверхность контакта намного меньше, чем в пенном режиме.
Струйный (инжекторный) режим возникает при дальнейшем увеличении скорости газа, который проходит через газожидкостной слой в виде газовых струй, не разрушаясь. Поверхность контакта намного меньше, чем в пенном режиме.
Расчет абсорберов
Исходные данные: расход газа G, его начальная и конечная концентрации, начальная концентрация абсорбента.
Определяются: расход абсорбента L, диаметр D абсорбера, высота абсорбера Н, его гидравлическое сопротивление ΔР.
7.1.9.1 Расход абсорбента определяется из уравнения материального баланса. Конечная концентрация абсорбента обычно не задана. Поэтому принимают ее как концентрацию поглощаемого газа в жидкости, находящейся в равновесии с газом.
7.1.9.2 Диаметр абсорберов определяют по уравнению расхода:
 , (7.15)
, (7.15)
где w 0 – фиктивная скорость газа, то есть скорость, отнесенная к полному сечению абсорбера, м/с.
7.1.9.3 Высота абсорберов определяется в зависимости от их типа:
– для насадочных с помощью уравнения массопередачи:
 – по газовой фазе;
– по газовой фазе;
и
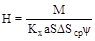 – по жидкой фазе,
– по жидкой фазе,
где а – удельная поверхность, м2/м3;
ψ – коэффициент смачиваемости насадки;
– для ступенчатых (тарельчатых) абсорберов в большинстве случаев определяют методом теоретической ступени (теоретической тарелки) и КПД колонны или методом построения кинетической кривой. Определение числа теоретических ступеней (теоретических тарелок) рассматривалось в разделе «Основы массопередачи».
Гидравлическое сопротивление абсорберов ΔР зависит от гидродинамических режимов, которые определяются скоростью газа и конструктивными особенностями аппарата. Оптимальную скорость определяют технико-экономическим расчетом, при этом рассматривая влияние скорости на гидравлическое сопротивление, диаметр и высоту аппарата.
Перегонка и ректификация
Перегонка – это процесс разделения жидких смесей путем их частичного испарения при кипении с последующей конденсацией образующихся паров.
Если парциальные давления компонентов, составляющих исходную смесь, различны, т.е. различна летучесть компонентов, то состав дистиллята будет отличаться от состава исходной смеси: в нем будет содержаться больше легколетучего (с большим парциальным давлением) компонента. Различают два вида перегонки: простую (дистилляция), сложную перегонку (ректификация).
Перегонка применяется для разделения и очистки сжиженных газов в химической, пищевой, фармацевтической, нефтехимической и других отраслях промышленности.
Перегонка проводится: под вакуумом (для термически нестойких или токсичных веществ), под атмосферным давлением, под избыточным давлением (сжиженный газ).
Тепловой расчет колонны
Тепловой баланс ректификационной колонны представлен на рисунке 7.22.

Рисунок 7.22 – К тепловому
расчету ректификационной колонны
Теплота, затрачиваемая на проведение процесса ректификации, вносится в систему с теплоносителем в кипятильнике. Для проведения процесса ректификации необходимо подвести тепло для испарения флегмы, испарения дистиллята, нагрева кубового остатка от температуры кипения смеси до температуры кипения остатка.
Расход греющего пара на проведение процесса определяют из теплового баланса (Пр=Ух).
| Приход теплоты: | Уход теплоты: |
| – с греющим паром Qгр.п.; | – с кубовым остатком Qкуб.; |
| – с исходным раствором Qисх.; | – со вторичным паром Qвт.п.; |
| – с флегмой Qф | – потери в окружающую среду Qпот.. |
Уравнение теплового баланса для ректификационной колонны:
 (7.30)
(7.30)
Жидкостная экстракция
Жидкостная экстракция – это процесс извлечения одного или нескольких компонентов жидкой смеси другой жидкостью, не смешивающейся или ограничено смешивающейся с первой.
Две взаимно нерастворимые жидкости и распределяемый между ними целевой компонент образуют экстракционную систему.
Экстракция используется: при незначительном содержании извлекаемого компонента в смеси (при ректификации потребовалось бы большее количество тарелок); при близких температурах кипения компонентов смеси; при выделении термически нестойких веществ (процесс экстракции протекает при комнатной температуре).
Достоинства процесса экстракции: низкие энергетические затраты (извлечение компонентов проводится при комнатной температуре).
Недостатки экстракции: ввод в систему третьего компонента, что обусловливает его последующее выделение, а это приводит к увеличению материальных затрат.
Выбор экстрагента
Оптимальным является экстрагент, обеспечивающий минимум капитальных и эксплуатационных затрат.
Требования, предъявляемые к экстрагенту:
– высокая селективность (избираемость);
– плотность, отличная от плотности первого растворителя В, (ρА ≠ ρВ);
– минимальная взаимная растворимость в растворителе исходного раствора;
– минимальная токсичность, низкая коррозионная активность, доступность, дешевизна, пожаро-, взрывобезопасность.
В качестве экстрагентов наиболее часто используют: органические кислоты, соли органических оснований, нейтральные растворители (спирт, вода). Если используют воду, то процесс называется выщелачиванием.
Кинетика экстракции
Кинетические закономерности процесса определяются основными законами массопередачи. При экстракции происходит массообмен между жидкими фазами и распределяемое вещество переходит из одной жидкости в другую. Для развития поверхности фазового контакта одну из жидкостей диспергируют до капель. Процесс переноса вещества при экстракции представляет собой перенос вещества из сплошной фазы к поверхности капли; перенос вещества через поверхность капли; распределение вещества внутри капли. Диффузионное сопротивление может быть как в сплошной фазе, так и в самой капле. Интенсивность процесса переноса вещества определяется положениями:
– чем больше размер капель, тем больше интенсивность массопередачи в каплю, т.е. создаются более благоприятные условия для возникновения конвективных потоков;
– поверхностно-активные вещества снижают перенос вещества в каплю, т.е., адсорбируясь на поверхности, они уменьшают конвективные потоки;
– существенное влияние на интенсивность переноса в системе «жидкость – жидкость» оказывают процессы с изменением размера капель, т.е. обновление поверхности контакта фаз при слиянии и дроблении.
Классификация экстракторов
Экстракционные аппараты классифицируют по разным признакам.
По принципу взаимодействия контактирующих фаз экстракционные аппараты можно разделить на два класса: работающие с непрерывным контактом фаз или со ступенчатым контактом фаз.
По расположению аппарата экстракторы подразделяются на вертикальные, горизонтальные и центробежные.
Важнейшим признаком классификации экстракторов является отсутствие или наличие подвода энергии извне. Экстракторы бывают без подвода внешней энергии (насадочные, тарельчатые, полые) и с подводом внешней энергии (роторно-дисковые, пульсационные, центробежные, вибрационные).
Расчет экстракторов
Целью расчета экстракторов является определение необходимого количества экстрагента, количества и концентрации экстракта и рафината.
Порядок расчета экстракционных аппаратов такой же, как и других массообменных аппаратов:
1) определение условий равновесия;
2) составление материального баланса;
3) определение движущей силы;
4) расчет коэффициентов массопередачи: КХ, КУ;
5) определение диаметра и высоты аппарата.
Расчет может проводиться как аналитически, так и графически (треугольная диаграмма).
Вопросы для самоконтроля
1. Раскройте принцип процесса абсорбции. Для решения каких задач применяют этот процесс?
2. Как составляется материальный баланс абсорбции? Раскройте понятие рабочей и равновесной линий данного процесса.
3. Составьте тепловой баланс абсорбции.
4. Что называют минимальным и оптимальным расходом абсорбента?
5. Дайте классификацию абсорбционных аппаратов.
6. Раскройте принцип действия насадочных колонн.
7. Каков порядок расчета абсорберов?
8. Приведите примеры схем установок с однократным и многократным использованием абсорбента.
9. Раскройте принцип ректификации. Изобразите схему ректификационной колонны и укажите на ней потоки жидкости и пара.
10. Сформулируйте законы Рауля и Дальтона.
11. Изобразите схему установки непрерывной ректификации бинарной смеси.
12. Составьте материальный баланс ректификационной колонны для разделения бинарной смеси.
13. Напишите уравнения рабочих линий для верхней и нижней частей ректификационной колонны.
14. Составьте тепловой баланс ректификационной колонны.
15. Как определяется оптимальное флегмовое число?
16. Раскройте сущность процесса жидкостной экстракции. Покажите схемы проведения процесса, области применения.
17. Поясните треугольные диаграммы и построение равновесных кривых.
18. Раскройте основы кинетики процесса экстракции, покажите лимитирующие стадии процесса.
19. Опишите принципиальные схемы экстракции.
20. Раскройте принцип расчета экстракторов.
21. Раскройте принципы интенсификации жидкостной экстракции.
С УЧАСТИЕМ ТВЕРДОЙ ФАЗЫ
К группе массообменных процессов с участием твердой фазы относятся сушка, адсорбция, кристаллизация и ионный обмен.
Сушка – процесс удаления влаги из твердых влажных материалов путем ее испарения. Этот процесс представляет собой переход влаги из твердого влажного материала в газовую или паровую фазу. Применяют в технике для предварительного обезвоживания перерабатываемых веществ или обезвоживания готового продукта.
Адсорбция – избирательное поглощение газов, паров или растворенных в жидкости веществ твердым поглотителем, способным поглощать одно или несколько веществ из смеси. Этот процесс представляет собой переход вещества из газовой, паровой или жидкой фазы в твердую. Применяют для извлечения того или иного вещества (или веществ) достаточно низкой концентрации из их смеси.
Кристаллизация – процесс выделения твердого растворенного вещества из его раствора (кристаллизация из раствора) или процесс выделения твердой фазы при затвердевании веществ, находящихся в расплавленном состоянии (кристаллизация из расплава).
Ионный обмен – избирательное извлечение ионов из растворов электролитов. Этот процесс представляет собой переход извлекаемого вещества из жидкой фазы в твердую. Применяют для извлечения веществ из растворов, в которых эти вещества находятся при низких концентрациях.
Растворение и экстрагирование (выщелачивание) – извлечение на основе избирательной растворимости какого-либо вещества из твердого пористого материала. Применяют для извлечения ценных или токсичных компонентов из твердых материалов.
Особенностью всех перечисленных процессов является нестационарность процесса и многообразие элементарных механизмов массопередачи в твердом теле. При данном типе массообмена перенос массы во внешней фазе (жидкость, газ, пар) осуществляется конвективной и молекулярной диффузией, а в твердой фазе механизм переноса обусловлен многообразием твердых пористых материалов. Элементарные виды переноса в твердом пористом материале: молекулярная и конвективная диффузии.
Молекулярная диффузия вещества в матрице твердого тела – обмен местами атомов с вакантными узлами кристаллической решетки либо обмен местами двух соседних атомов. Молекулярная диффузия может быть свободной и кнудсеновской. Свободная диффузия молекул в капиллярах возникает в достаточно широких порах, радиус которых больше длины свободного пробега молекул. Стесненная, или кнудсеновская, диффузия возникает в случае, когда движение молекул определяется столкновениями со стенками пор.
Наряду со свободной и стесненной диффузией в объеме пор существует и диффузионный поток по их поверхности – термодиффузия, поскольку молекулы и в адсорбированном состоянии находятся в тепловом движении. Термодиффузия описывается законом Фика:
 , (8.1)
, (8.1)
где D – коэффициент эффективной диффузии, коэффициент массопроводности (справочная величина), м2/с.
Конвективная диффузия вещества в каналах возникает под действием разности температур и давлений по длине поры. Конвективный перенос возникает, когда длина свободного пробега молекул значительно меньше радиуса поры.
8.1 Сушка
Сушка – это процесс удаления влаги из твердых материалов путем ее испарения и отвода образующихся паров.
Применяется с целью:
– повышения качества конечного продукта;
– предотвращения слеживаемости материала;
– удешевления транспортировки.
По физической сущности сушка является процессом совместного тепломассопереноса и сводится к перераспределению и перемещению влаги под воздействием теплоты из глубины высушиваемого материала к его поверхности и последующему ее испарению.
По способу подвода тепла к высушиваемым материалам различают следующие виды сушки:
– конвективная – сушильный агент и высушиваемый материал непосредственно соприкасаются друг с другом;
– контактная – тепло передается от теплоносителя к материалу через разделяющую их стенку. Отсутствует контакт между высушиваемым веществом и сушильным агентом, что важно при сушке гигроскопичных и окисляющихся материалов или тогда, когда влага является ценным компонентом;
– инфракрасная – с помощью теплового излучения (для сушки пленочных материалов);
– сушка токами высокой частоты – под действием переменного электрического тока заряженные частицы, дипольные молекулы внутри материала начинают колебаться, передвигаются, т.е. совершают механическое движение, при этом выделяется тепло, которое идет на испарение влаги;
– сублимационная сушка – удаление влаги из материала после предварительного ее перевода в твердое состояние (замораживание). Чаще всего используют вакуум, испарение происходит при низких температурах.
Сушка, как и выпаривание, является очень дорогим процессом (для испарения влаги, требуется много энергии), поэтому сушке должно предшествовать механическое удаление влаги: центрифугирование, отжим и др.
Выбор сушильного агента
В качестве сушильных агентов могут выступать: воздух, топочные газы, перегретый пар, инертный газ.
Достоинствами воздуха как сушильного агента являются его доступность, дешевизна. Однако, используя воздух, невозможно достичь высоких температур. Использование топочных (дымовых) газов в качестве сушильного агента позволяет достичь высоких температур, кроме того, при использовании топочных газов отпадает необходимость в калорифере. Однако существует возможность загрязнения высушиваемого материала примесями, содержащимися в газах. С помощью перегретого пара можно достигать очень высоких температур, однако при этом возрастает и давление пара. Инертный газ применяется при сушке гигроскопичных, окисляющихся на воздухе веществ.
Наиболее часто в процессе сушки в качестве сушильного агента используется воздух. Поэтому целесообразно рассмотреть физические свойства влажного воздуха.
Равновесие процесса сушки
Обозначим давление жидкости в материале рм, парциальное давление пара в газовом потоке рп. Условием равновесия сушки является разность давления пара жидкости в материале и парциального давления пара в газовом потоке. Достижению равновесия соответствует предельная влажность материала, называемая равновесной влажностью.
Направление массопереноса определяется содержанием влаги в материале и окружающей среде или абсолютными значениями рм и рп. Если рп > рм, перенос влаги осуществляется из газа к твердому телу, то есть происходит процесс сорбции (увлажнения). В противоположном случае, когда рп < рм, перенос влаги осуществляется из твердой фазы в газовую, то есть идет процесс десорбции (сушки).
Величина рм зависит от температуры, влажности материала и от характера связи влаги с материалом. Существует несколько форм связи влаги с материалом (перечислены в порядке убывания энергии связи): химическая влага, адсорбционная влага, капиллярная влага, осмотическая влага, механически удерживаемая влага.
Материальный баланс сушки
 |
Тогда материальный баланс процесса сушки запишется:
 , или
, или  , (8.3)
, (8.3)
по высушиваемому материалу
 , (8.4)
, (8.4)
 . (8.5)
. (8.5)
Целью материального баланса является определение количества испаренной влаги
 . (8.6)
. (8.6)
По сушильному агенту материальный баланс запишется
 , (8.7)
, (8.7)
где L – расход воздуха, кг/с.
 . (8.8)
. (8.8)
Формула (8.8) позволяет рассчитать количество свежего воздуха, необходимого для удаления W кг влаги из влажного материала.
При расчете и анализе процесса сушки используется понятие «удельный расход воздуха».
Удельный расход воздуха – это расход воздуха, необходимый для испарения 1 кг влаги [кг сухого воздуха/кг испаряемой влаги]
 (8.9)
(8.9)
или
 . (8.10)
. (8.10)
Удельный расход воздуха легко определяется по диаграмме «I-x», при этом задаются значением х0 и определяют значение х2.
По известному расходу воздуха на сушку выбирают вентилятор необходимой мощности и производительности.
Схемы процессов сушки
8.1.7.1 Сушка с многократным промежуточным подогревом воздуха изображена на рисунке 8.10. На рисунке 8.11 показано построение процесса сушки на диаграмме «I–x».

Рисунок 8.10 – Схема сушки с многократным промежуточным
подогревом воздуха

Рисунок 8.11 – Построение процесса сушки с многократным
промежуточным подогревом на диаграмме «I–x».
8.1.7.2 Сушка с частичным возвратом отработанного воздуха показана на рисунке 8.12.

Рисунок 8.12 – Схема сушки с частичным возвратом отработанного воздуха
Кинетика процесса сушки
Скорость сушки определяется с целью расчета продолжительности сушки.
 Из рисунка 8.13 видно, что движущей силой процесса сушки является разность парциальных давлений вблизи поверхности материала и в окружающей среде.
Из рисунка 8.13 видно, что движущей силой процесса сушки является разность парциальных давлений вблизи поверхности материала и в окружающей среде.
Кинетика сушки характеризуется изменением средних значений влагосодержания материала и средних температур.
Скорость сушки зависит:
– от внутренней структуры материала, его теплофизических свойств, размеров, формы и состояния внешней поверхности;
– от параметров сушильного агента – его температуры, относительной влажности, скорости движения относительно материала.
Кинетика сушки характеризуется изменением во времени средней влажности, отнесенной к количеству абсолютно сухого материала (рисунок 8.14). Зависимость между влажностью материала и временем изображается кривой сушки, которую строят по опытным данным.
Данные о скорости сушки, полученные с помощью кривых сушки, изображаются в виде кривых скорости сушки, которые строят в координатах «скорость сушки – влажность материала».
 В общем случае процесс сушки состоит из двух стадий: перемещения влаги из глубины к поверхности материала и испарения влаги с поверхности материала.
В общем случае процесс сушки состоит из двух стадий: перемещения влаги из глубины к поверхности материала и испарения влаги с поверхности материала.
Под скоростью сушки понимают изменение влажности материала в единицу времени, т.е. первую производную функции  , которая обычно рассматривается по абсолютной величине. Кривая скорости сушки, соответствующая кривой сушки, изображена на рисунке 8.15.
, которая обычно рассматривается по абсолютной величине. Кривая скорости сушки, соответствующая кривой сушки, изображена на рисунке 8.15.

В зависимости от того, какая из стадий является лимитирующей, различают периоды внутренней и внешней диффузии. В начале сушки, когда влажность материала высокая, скорость процесса постоянна (ВС). Это объясняется тем, что испарение влаги с поверхности материала успевает компенсироваться ее подводом из глубины. Это первый период сушки, для которого характерны:
– постоянная скорость сушки;
– постоянная температура материала, которая равна температуре мокрого термометра. Температура мокрого термометра – когда температура испаряющейся жидкости соответствует температуре смоченного термометра (т.е. температура газа равна температуре жидкости).
Скорость первого периода сушки определяется по уравнению
 , (8.21)
, (8.21)
где F – поверхность испарения, м2;
β – коэффициент массоотдачи, м2/с.
Из уравнения (8.21) можно определить продолжительность сушки в первом периоде:
 . (8.22)
. (8.22)
В этом периоде скорость сушки определяется температурой сушильного агента, скоростью движения воздуха относительно материала и поверхностью материала.
По мере испарения влаги влажность материала уменьшается, при достижении значения хкр на поверхности материала появляются сухие места и скорость сушки начинает падать (второй период сушки).
Для второго периода сушки характерны: образование на поверхности сухих мест, углубление поверхности испарения внутрь материала, повышение температуры материала.
Скорость сушки во втором периоде определяется по уравнению
 , (8.23)
, (8.23)
где К – коэффициент скорости сушки;
х – текущее влагосодержание.
Из уравнения (8.23) продолжительность сушки во втором периоде
 . (8.24)
. (8.24)
Во втором периоде сушки скорость зависит от пористости материала, размера пор, температуры и влажности сушильного агента. Следовательно, чем мельче материал, тем быстрее идет сушка.
Общее время сушки будет складываться из продолжительности сушки в первом и втором периодах. Чем пористее материал, тем больше продолжительность сушки в первом периоде, чем больше толщина материала, тем больше продолжительность сушки во втором периоде.
Расчет сушилок
Для проектирования сушильной установки должны быть заданы:
1) конструкция сушилки;
2) вид сырого материала, подвергающегося сушке и сушильного агента;
3) производительность;
4) режим сушки (температура сушки, кривая сушки, скорость сушильного агента и др.);
5) начальная и конечная влажность материала.
Необходимо определить: основные физические параметры высушиваемого материала и сушильного агента, количество испаряемой влаги, расход воздуха на сушку, расход тепла, размеры сушилки.
Для определения поверхности сушилки вводится понятие напряжения сушилки по влаге – А. Напряжение сушилки по влаге может быть объемное  и поверхностное
и поверхностное  .
.
В этом случае необходимо определить скорость, время, в зависимости от типа сушилки напряжение по влаге или (Аs, или Av), поверхность или объем сушилки.
Кристаллизация
Кристаллизация – процесс выделения твердой фазы из растворов, расплавов и паров.
Применяется с целью выделения твердой фазы, разделения веществ, очистки веществ и выращивания монокристаллов.
Кристаллизация состоит из двух основных стадий – образования зародышей кристаллов и роста кристаллов. Обе стадии протекают одновременно.
Если wобр > wрост, то получается большое количество мелких кристаллов, если wобр < wрост, то образуются кристаллы больших размеров.
Начало кристаллизации осуществляется в центрах кристаллизации, в качестве которых могут выступать механические примеси, шероховатость стенок.
Условие протекания процесса – пересыщение раствора, т.е. действительная концентрация раствора вещества должна быть выше равновесной.
Величина предельного пересыщения зависит от свойств растворенного вещества и растворителя, температуры раствора, скорости охлаждения, наличия примесей, механического воздействия.
Кинетика процесса
Как уже говорилось выше, процесс кристаллизации протекает в две стадии: образование центров кристаллов и рост кристаллов.
Кристаллизация идет с достаточной скоростью лишь в пересыщенных растворах. В подобных растворах на начальном этапе образуются «зародыши» кристаллов.
Начало и скорость образования кристаллов зависит от степени пересыщения, природы растворенного вещества и растворителя, наличия нерастворимой твердой фазы, наличия электрического поля.
Причина появления «зародышей» – флуктуация концентраций, в результате которой образуются «дозародыши» кристаллов, представ-ляющие собой скопления молекул или ионов растворенного вещества. При достижении некоторого критического размера «дозародышей» образуются зародыши кристаллов. Начиная с некоторого критического размера rкр в пределах от 0,5 до 5нм, начинается быстрый рост зародышей и образование большого числа полидисперсных кристаллов. Чем меньше критический размер кристалла, тем больше должна быть степень пересыщения раствора. Эта закономерность выражается следующим образом:
 (8.32)
(8.32)
где с – действительная концентрация раствора на момент начала кристаллизации, кг/м3;
с* – равновесная концентрация (равновесная растворимость), кг/м3;
σ – поверхностное натяжение, Н/м;
М – молекулярная масса кристаллов;
ρт – плотность кристаллов, кг/м3.
Отношение  называется степенью пересыщения.
называется степенью пересыщения.
На стадии роста кристаллов происходит образование крупных кристаллов за счет массообмена с жидкой фазой.
Скорость обеих стадий можно повысить, увеличивая степень пересыщения, увеличивая температуру, используя интенсивное перемешивание, добавляя нерастворимые твердые частицы.
Рост самого кристалла протекает в две стадии:
1) диффузионная – подвод растворенного вещества к поверхности зародыша. Скорость этой стадии определяется по уравнению
 , (8.33)
, (8.33)
где G – масса кристаллической фазы, кг;
βс – коэффициент массоотдачи в жидкой фазе;
с – концентрация вещества в объеме раствора, кг/м3;
сп – концентрация вещества у поверхности кристалла, кг/м3;
2) рост кристалла. Скорость этой стадии определяется:
 , (8.34)
, (8.34)
где βт – коэффициент массоотдачи в твердой фазе;
с* – концентрация насыщения, кг/м3.
Если скорость одной из стадий будет велика, следовательно, вторая стадия будет лимитировать процесс.
В случае соизмеримых скоростей процессов в сплошной и дисперсной фазах общая скорость процесса определится по уравнению массопередачи:
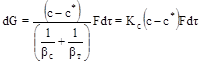 , (8.35)
, (8.35)
где  – коэффициент массопередачи при кристаллизации.
– коэффициент массопередачи при кристаллизации.
Конструкции аппаратов
Аппараты, в которых осуществляют процесс кристаллизации, называются кристаллизаторы.
По условию образования и роста кристаллов кристаллизаторы классифицируются на поверхностные, в которых образование кристаллов происходит на охлаждаемой поверхности, и объемные, в которых образование и рост кристаллов происходят во всем объеме аппарата. Существуют также аппараты смешанного типа, в которых образование и рост кристаллов происходят на охлаждаемой поверхности и в объеме аппарата; они бывают прямоточные, емкостные и циркуляционные.
По типу создания условий пересыщения кристаллизаторы можно подразделить на три группы: изогидрические, вакуумные и испарительные.
На рисунке 8.20 представлена схема устройства изогидрического поверхностного вальцового кристаллизатора, который используется для кристаллизации солей с существенно снижающейся раствори-мостью при понижении температуры.
Вальцовые кристаллизаторы применяются для кристаллизации из расплавов или из растворов с небольшим содержанием маточного раствора. Недостаток: мелкокристалличность получаемого продукта, присутствие примесей в готовом продукте.
Негативным фактором при кристаллизации является отложение накипи и кристаллов на стенках аппарата – инкрустация. Чтобы снизить ее, нужно перемешивать раствор и полировать стенки аппарата.
Из объемных кристаллизаторов наибольшее распространение получил аппарат с рубашкой и мешалкой. На рисунке 8.21 изображен изогидрический кристаллизатор периодического действия. Раствор в нем охлаждается при постоянном количестве растворителя до температуры, ниже температуры насыщения. В результате охлаждения раствор становится пересыщенным, что приводит к возникновению процесса кристаллизации.




Адсорбция
Адсорбция – процесс поглощения вещества из смеси газовых паров или растворов поверхностью или объемом пор твердого тела – адсорбента.
Поглощаемое вещество, находящееся в газе (жидкости), называется адсорбтивом, а поглощаемое вещество – адсорбатом.
Адсорбция применяется с целью очистки и осушки газов, очистки и осветления растворов, разделения парогазовых смесей, а также извлечения ценных летучих растворителей из смеси.
Кинетика адсорбции
Рассмотрим рисунок 8.24а. Газовый поток с начальной концентрацией ун поглощаемого вещества непрерывно подается в неподвижный слой адсорбента. Через некоторое время на начальном участке слоя адсорбента поглощение практически прекращается из-за насыщения адсорбента поглощаемым веществом. Сорбирующиеся вещества «проскакивают» через этот слой, и зона адсорбции перемещается в следующие слои. Изменение фронта адсорбции изображено на рисунке 8.24б.
На рисунке 8.24:
U – скорость перемещения фронта адсорбции;
h0 – участок слоя адсорбента, на котором происходит изменение концентрации от ун до концентрации, соответствующей началу «проскока».
 , (8.38)
, (8.38)

Рисунок 8.24 – Движение фронта адсорбции по слою адсорбента
где  – число единиц переноса в газовой фазе;
– число единиц переноса в газовой фазе;
 – объемный коэффициент массопередачи.
– объемный коэффициент массопередачи.
Как уже говорилось выше, при процессе адсорбции существуют две области: внутридиффузионная и внешнедиффузионная. Процесс протекает в той или иной области в зависимости от значения критерия Био (Вid). Если значение Вid ≥ 30, то скорость процесса определяется скоростью массопроводности внутри зерна адсорбента. Если значение Вid ≤ 0,1, то скорость процесса зависит от скорости массопередачи в газовой фазе.
Классификация адсорберов
Адсорберы можно разделить по условиям работы на следующие группы: а) с неподвижным адсорбентом; б) с движущимся зернистым адсорбентом; в) с псевдоожиженным пылевидным адсорбентом.
Адсорберы с неподвижным слоем адсорбента весьма просты по устройству и представляют собой цилиндрические вертикальные или горизонтальные емкости, заполненные адсорбентом. Примером адсорберов с неподвижным слоем адсорбента может служить аппарат, изображенный на рисунке 8.25. В тех случаях, когда адсорбция проводится из жидкой фазы, в качестве адсорберов используется обычная фильтровальная аппаратура.

1 - цилиндрический корпус; 2 - решетка; 3,4 - штуцеры
Рисунок 8.25 – Вертикальный адсорбер
с неподвижным зернистым адсорбентом
Аппараты с движущимся зернистым адсорбентом можно подразделить на аппараты типа полых колонн (применяются при адсорбции из газовой фазы) и аппараты с механическими транспортными приспособлениями (применяются при адсорбции из жидкой фазы).
Аппараты с псевдоожиженным пылевидным адсорбентом разделяют на одноступенчатые и многоступенчатые. Одноступенчатый адсорбер изображен на рисунке 8.26.

1 – корпус; 2 – газораспределительная решетка;
Рисунок 8.26 – Одноступенчатый адсорбер с псевдоожиженным
адсорбентом
Расчет адсорберов
8.3.5.1 Составляют материальный баланс адсорбции исходя из условия равновесия:
 . (8.39)
. (8.39)
Поскольку 
 , а содержание поглощаемого компонента в адсорбенте хн = 0, то из уравнения (8.39) находят количество адсорбента
, а содержание поглощаемого компонента в адсорбенте хн = 0, то из уравнения (8.39) находят количество адсорбента
 (8.40)
(8.40)
или конечную концентрацию адсорбтива в газовой фазе:
 . (8.41)
. (8.41)
8.3.5.2 Находят диаметр адсорбера исходя из уравнения расхода:
 , (8.42)
, (8.42)
где w – скорость газового потока, м/с;
V – расход газовой смеси, м3.
8.3.5.3 Находят высоту адсорбера:
 , (8.43)
, (8.43)
где ρн – насыпная плотность адсорбента, кг/м3.
8.3.5.4 Рассчитывают продолжительность адсорбции:
 . (8.44)
. (8.44)
Мембранные процессы
Мембранными процессами называют процессы разделения смесей посредством полупроницаемых мембран.
Мембрана – полупроницаемая перегородка, пропускающая определенные компоненты жидких и газовых смесей.
Мембранные процессы в настоящее время применяются достаточно широко. В химической промышленности мембранные процессы применяются для выделения высокомолекулярных соединений, разделения азеотропных смесей, очистки и концентрирования растворов. В биотехнологии мембранные процессы используют для выделения биологически активных веществ. В пищевой промышленности – для концентрирования соков, для получения высококачественных сахаров. Наиболее широко мембранные процессы применяются для обработки воды и водных растворов, для очистки сточных вод.
Классификация мембран
Мембраны бывают полимерные (полупроницаемые) и с жесткой структурой (металлические, из пористого стекла и т.д.). Полупроницаемые мембраны разделяют на две группы: пористые и непористые. В последние годы получили широкое распространение ядерные мембраны. Пористые полимерные и металлические мембраны применяют для проведения процессов обратного осмоса и ультрафильтрации. Для процессов разделения жидких смесей методом испарения через мембрану используют непористые полимерные мембраны, являющиеся квазигомогенными гелями.
Требования, предъявляемые к мембранам:
– селективность;
– высокая удельная производительность (проницаемость);
– химическая стойкость;
– механическая прочность.
Расчет мембранных процессов
При расчете мембранных процессов известными параметрами являются количество (  ) и состав исходного раствора (
) и состав исходного раствора (  ), концентрация пермеата (
), концентрация пермеата (  ), выход пермеата (
), выход пермеата (  ) (рисунок 8.29).
) (рисунок 8.29).

Рисунок 8.29 – К расчету мембранных процессов
Порядок расчета:
1) определяют количество пермеата:
 ; (8.47)
; (8.47)
2) составляют материальный баланс по потокам:
 ; (8.48)
; (8.48)
3) составляют материальный баланс по компоненту:
 ; (8.49)
; (8.49)
4) определяют эффективность мембраны:
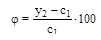 ; (8.50)
; (8.50)
5) выбирают тип мембраны;
6) находят рабочую поверхность мембраны из основного уравнения массопередачи:
 , (8.51)
, (8.51)
где М – количество компонента, проходящего через мембрану.
Вопросы для самоконтроля
1. Охарактеризуйте массоперенос в твердой пористой фазе.
2. Запишите уравнение массопередачи для систем с участием твердой фазы.
3. В чем состоит сущность конвективной, контактной, радиационной, сублимационной и диэлектрической сушки?
4. Перечислите и охарактеризуйте виды связи влаги с материалом.
5. Раскройте принципы построения диаграммы «I–x» состояния влажного воздуха. Как определяются параметры влажного воздуха с помощью этой диаграммы?
6. Составьте тепловой баланс конвективной сушки.
7. В чем особенности материального баланса конвективной сушки?
8. Поясните принципы построения кривых и их использования для расчета скорости и времени сушки.
9. Что понимается под кристаллизацией?
10. Проведите анализ диаграмм состояний системы «газ –жидкость – твердое тело».
11. Составьте материальный и тепловой баланс кристаллизации.
12. Поясните особенности кинетики кристаллизации.
13. Опишите устройство и принцип действия кристаллизаторов.
14. Назовите наиболее рациональные области применения адсорбции.
15. Охарактеризуйте равновесие при адсорбции.
16. Как составляется материальный баланс адсорбции?
17. Покажите устройство и принцип действия адсорберов с неподвижным слоем адсорбента.
18. Раскройте принципы и назовите стадии расчета адсорберов.
19. Что понимается под мембранными процессами разделения? Дайте их классификацию.
20. Что является движущей силой баромембранных процессов? Как ее рассчитывают?
21. Дайте классификацию мембран.
22. Приведите схему расчета мембранных процессов.
ПРИЛОЖЕНИЕ А
(обязательное)
Основные термины и определения
Абсолютная влажность – количество водяных паров, содержащихся в 1 м3 влажного воздуха.
Абсорбент – жидкий поглотитель для избирательного поглощения абсорбтива в процессе абсорбции.
Абсорбция – избирательное поглощение газов или паров жидкости поглотителем (абсорбентом). Этот процесс представляет собой переход вещества из газовой или паровой фазы в жидкую.
Адсорбент – твердое тело, на поверхности пор которого конденсируется поглощаемое вещество (адсорбтив) в процессе адсорбции.
Адсорбция – избирательное поглощение газов, паров или растворенных в жидкости веществ твердым поглотителем, способным поглощать одно или несколько веществ из смеси. Этот процесс представляет собой переход вещества из газовой, паровой или жидкой фазы в твердую. Применяют для извлечения того или иного вещества (или веществ) достаточно низкой концентрации из их смеси.
Азеотропная перегонка – перегонка с введением специальных растворителей, применяется для разделения азеотропных смесей. При азеотропной перегонке применяют растворители, образующие с одним из компонентов азеотропную смесь с минимальной температурой кипения. Растворитель удаляется с дистиллятом.
Азеотропные смеси (нераздельнокипящие) – смеси, обладающие следующими особенностями: 1) имеют минимальную или максимальную температуру кипения по сравнению со смесями этих компонентов другого состава; 2) испарение азеотропной смеси, как и чистых веществ, происходит при постоянной температуре; 3) азеотропная смесь испаряется без изменения состава.
Активность адсорбента – количество вещества, поглощенного единицей веса (или объема) адсорбента за время от начала адсорбции до начала «проскока», определяет динамическую активность адсорбента. Количество вещества, поглощенное тем же количеством адсорбента за время от начала адсорбции до установления равновесия, характеризует статическую активность.
Аэрозоли – системы, состоящие из твердых или жидких частиц, взвешенных в газообразной среде (например, пыль, дым, туман).
Бинодальная кривая (кривая равновесия) – кривая, разбивающая диаграмму на две области. Область, ограниченная этой кривой, соответствует двухфазным (расслаивающимся) системам и является рабочей частью треугольной диаграммы. Область диаграммы, лежащая вне этой кривой, соответствует гомогенной системе.
Влагосодержание воздуха – количество водяного пара (кг), приходящееся на 1 кг абсолютно сухого воздуха.
Влажный воздух – смесь сухого воздуха с водяным паром.
Водоотводчики (конденсатоотводчики) – устройства, применяемые для удаления из аппарата конденсата без выпуска с ним пара.
Водяной пар – теплоноситель (насыщенный водяной пар), имеющий следующие преимущества: 1) высокий коэффициент теплоотдачи; 2) большое количество тепла, выделяемое при конденсации единицей количества пара; 3) возможность транспортировки по трубопроводам на значительные расстояния; 4) равномерность обогрева, так как конденсация пара происходит при постоянной температуре; 5) легкое регулирование обогрева.
Вторичный пар – пар, образующийся при выпаривании растворов.
Выпаривание – процесс концентрирования растворов, заключающийся в удалении растворителя путем испарения при кипении.
Высота единицы переноса – высота участка, соответствующая одной единице переноса.
Гетерогенные (неоднородные) системы – системы, состоящие из двух или нескольких фаз. Фазы, составляющие систему, могут быть в принципе механически отделены одна от другой.
Гигроскопическая точка – равновесная влажность, соответствующая полному насыщению среды влагой.
Гидравлическая депрессия – температурная поправка, которая учитывает повышение давления в аппарате вследствие гидравлических потерь при прохождении вторичного пара через ловушку и выходной трубопровод.
Гидравлический радиус – отношение площади сечения потока S к смоченному периметру канала (трубопровода) П: rг = S / П.
Гидростатическая депрессия – температурная поправка, которая вызывается тем, что нижние слои жидкости в аппарате закипают при более высокой температуре, чем верхние (вследствие гидростатического давления верхних слоев).
«Глухой» пар – пар, который не соприкасается с обогреваемой жидкостью, жидкость отделена от него стенкой, через которую и передается тепло.
Градирни – аппараты башенного типа, в которых охлаждаемый воздух движется снизу вверх навстречу стекаемой жидкости. При этом охлаждение происходит не только за счет теплоотдачи, но в значительной степени и за счет испарения части жидкости.
Граничные условия – условия, характеризующие взаимодействие среды с телами, ограничивающими объем, в котором протекает процесс.
Греющий пар – насыщенный водяной пар, используемый в качестве теплоносителя в выпарных аппаратах.
Движущая сила гидродинамического процесса – разность давлений между двумя точками или сечениями аппарата.
Движущая сила процессов массопереноса – в общем случае разность химических потенциалов распределяемого компонента в фазах. В частных случаях - разность между рабочими и равновесными концентрациями: Dу = у - у* или Dх = х* - х .
Десорбция – процесс, обратный абсорбции или адсорбции, то есть выделение растворенного газа из жидкости или выделение сорбированного вещества из твердого поглотителя.
Диаграмма « I - х» – диаграмма состояния влажного воздуха, разработанная Л.К. Рамзиным, на которой наглядно изображается и с достаточной точностью для технических расчетов определяется изменение основных свойств воздуха при нагревании, охлаждении и осушке. Диаграмма построена в координатах «энтальпия (ось ординат) – влагосодержание (ось абсцисс)». Угол между осями координат составляет 135оС.
Дисперсная фаза – внутренняя фаза, находящаяся в тонко раздробленном состоянии.
Дисперсность D – величина, обратная поперечному размеру частиц.
Дисперсный состав – процентное содержание частиц различного размера.
Дистиллят – конденсированные пары компонента с большей летучестью, образующиеся при разделении смеси в процессе перегонки или ректификации.
Диффузионное сопротивление – величина, обратная коэффициенту массопередачи: R = 1/ Кх,у.
Диффузия – движение частиц среды, приводящее к переносу вещества и выравниванию концентраций или установлению их равновесного распределения.
Диэлектрическая сушка – сушка, производимая путем нагревания высушиваемых материалов токами высокой частоты.
Дым - система, состоящая из газа и распределенных в нем твердых частиц размерами от 0,3 до 5 мкм; она образуется при горении.
Единый кинетический закон: Скорость процесса прямо пропорциональна движущей силе и обратно пропорциональна сопротивлению.
Закон Генри – равновесное парциальное давление пропорционально содержанию растворенного газа в растворе.
Закон Дальтона – полное давление газовой смеси равно сумме парциальных давлений компонентов.
Закон Рауля – парциальное давление пара каждого компонента идеальных смесей зависит от температуры и содержания данного компонента и пропорционально молярной доле данного компонента в смеси.
Законы равновесия определяют условия, при которых перенос любой субстанции прекращается.
Излучательная способность – полное количество энергии, излучаемое в единицу времени единицей поверхности тела. Е = Q/Ft.
Изотерма адсорбции – кривая, характеризующая адсорбционное равновесие, при котором устанавливается определенная зависимость между концентрацией адсорбированного вещества и его концентрацией в фазе, соприкасающейся с адсорбентом.
Изотермическая поверхность – геометрическое место всех точек с одинаковой температурой.
Инверсия фаз – переход дисперсной фазы в сплошную или наоборот, возможный при определенном массовом соотношении фаз.
Интенсивность перемешивания определяется количеством энергии, подводимой к единице объема (или массы) перемешиваемой жидкости в единицу времени.
Ионный обмен – избирательное извлечение ионов из растворов электролитов. Этот процесс представляет собой переход извлекаемого вещества из жидкой фазы в твердую. Применяют для извлечения веществ из растворов, в которых эти вещества находятся при низких концентрациях.
Капельная конденсация пара – образование капель конденсата на несмачиваемой поверхности.
Кинетика кристаллизации – скорость процесса кристаллизации, определяемая скоростью диффузии растворенного вещества через пограничный слой либо скоростью слияния вещества с телом кристалла.
Кинетическая кривая – основа графического метода определения числа реальных ступеней, геометрическое место точек рабочих концентраций в фазах на выходе со ступени.
Коагуляция – процесс укрупнения твердых частиц вследствие их слипания.
Коалесценция – процесс укрупнения капель или пузырей путем их слияния.
Колпачковые тарелки. В колпачковых тарелках газ барботирует через жидкость, выходя из прорезей колпачков, расположенных на каждой тарелке. В прорезях газ дробится на мелкие струйки, которые при выходе из прорези почти сразу поднимаются вверх и, проходя через слой жидкости на тарелке, сливаются друг с другом.
Конвективная сушка – сушка путем непосредственного соприкосновения сушильного агента (нагретого воздуха, топочных газов) с высушиваемым материалом.
Конвекция – перенос тепла путем перемещения макрообъемов среды в направлении теплопереноса, то есть этот механизм характерен только для сред, которые обладают текучестью.
Контактная сушка – сушка путем нагревания высушиваемого материала тем или иным теплоносителем через стенку, проводящую тепло.
Концентрация вещества – отношение количества какого-либо компонента смеси (молярная концентрация, моль/м3) или его массы (массовая концентрация, кг/м3) к объему смеси. На практике часто используют безразмерную величину – массовую, молярную или объемную долю, равную отношению массы, количества или объема какого-либо компонента смеси соответственно к массе, количеству или объему смеси.
Коэффициент избытка флегмы – отношение рабочего флегмового числа к минимальному.
Коэффициент массоотдачи bу, х показывает, какое количество вещества переходит от единицы поверхности раздела фаз в ядро потока или наоборот в единицу времени при движущей силе, равной единице.
[bу, х] = [М/ FDх,у] = [м/с].
Коэффициент массопередачи К показывает, какое количество распределяемого вещества переходит из фазы в фазу в единицу времени через единицу поверхности контакта фаз при движущей силе, равной единице; характеризует скорость процесса переноса вещества из одной фазы в другую. К = 1/ R , где R – сопротивление.
Коэффициент молекулярной диффузии D показывает, какое количество вещества диффундирует в единицу времени через единицу поверхности при градиенте концентрации, равном единице. [D] = =[M¶n/Ft¶c] = [м2/с].
Коэффициент полезного действия колонны h равен отношению числа теоретических ступеней к числу необходимых рабочих (действительных) ступеней nд (h зависит от скоростей фаз, физических свойств, структуры потоков и других факторов): h = nт / nд.
Коэффициент распределения (константа фазового равновесия) – отношение концентраций распределяемого компонента в фазах при равновесии: m = y*/x.
Коэффициент смачиваемости насадок – коэффициент, учитывающий неполное смачивание насадки, вследствие чего в процессе массопередачи участвует не вся поверхность насадки, а лишь некоторая активная ее часть.
Коэффициент сушки – количество (кг) испаренной влаги в 1 с, приходящееся на 1кг сухого вещества.
Коэффициент теплоотдачи a показывает, какое количество теплоты передается от теплоносителя к 1 м2 поверхности стенки (или от стенки с поверхностью 1 м2 к теплоносителю) в единицу времени при разности температур между теплоносителем и стенкой в 1 К. [a] = = [Q / Ft Dt] = [Вт/ м2*К] = [Дж/ м2*с*К].
Коэффициент теплопередачи К показывает, какое количество теплоты передается от горячего теплоносителя к холодному за одну секунду через 1 м2 разделяющей теплопроводящей стенки при разности температур между теплоносителями в 1 К.
Коэффициент теплопроводности l показывает, какое количество теплоты проходит вследствие теплопроводности в единицу времени через единицу поверхности теплообмена при падении температуры на один градус на единицу длины нормали к изотермической поверхности [l] = [-Q / Ft*(¶l/¶t) ] = [Дж / м*с*К] = [Вт/м*К].
КПД Мерфри (эффективность ступени или тарелки) – отношение изменения концентрации данной фазы на ступени к движущей силе на входе той же фазы в ступень; обозначают Еу и Ех.
Кристаллизация – процесс выделения твердого растворенного вещества из его раствора (кристаллизация из раствора) или процесс выделения твердой фазы при затвердевании веществ, находящихся в расплавленном состоянии (кристаллизация из расплава).
Критерии теплового подобия:
критерий Пекле характеризует соотношение между интенсивностью переноса теплоты конвекцией и теплопроводностью в движущемся потоке: Ре = wl/а;
критерий Био – безразмерный комплекс, который характеризует соотношение между внешним и внутренним теплопереносом:
Bi = al/l;
критерий Грасгофа характеризует соотношение сил трения, инерции и подъемной силы, обусловленной различием плотностей в отдельных точках неизотермического потока: Gr = gl3 bDt/n2;
критерий Нуссельта характеризует интенсивность перехода теплоты на границе раздела фаз. Характеризует отношение суммарного переноса теплоты конвекцией и теплопроводностью (т.е. теплоотдачей) к теплоте, передаваемой теплопроводностью;
критерий Прандтля характеризует вязкостные и температуропроводные свойства теплоносителя; связь скоростного и температурного полей: Pr = n/а;
критерий Фурье характеризует условия подобия неустановившихся процессов теплоотдачи: Fo = at/l2;
критерий Шервуда (диффузионный критерий Нуссельта) – безразмерный комплекс, который характеризует отношение скорости переноса вещества (конвективного и молекулярного - b) к молекулярному переносу (D). (Sh является аналогом теплового критерия Нуссельта, а также является определяемым критерием, поскольку в него входит величина b.)
Критическая влажность – влажность, соответствующая начальной точке периода падающей скорости сушки.
Лимитирующая стадия при массопередаче - стадия, которая определяет общую скорость процесса. Если коэффициент bх велик, то 1/bу >> m/bх и Ky » bу, то есть лимитирующей стадией процесса является диффузионное сопротивление в фазе Фу. Если велики значения bу и m, то 1/bх >> 1/(mbу) и Kх » bх , то есть лимитирующей стадией в данном случае является диффузионное сопротивление в фазе Фх.
Линия равновесия – кривая, изображающая зависимость равновесной концентрации от любой концентрации этого вещества.
Массоотдача – перенос вещества внутри фазы: из фазы к границе раздела фаз или, наоборот, от границы раздела в фазу (по аналогии с процессом переноса теплоты внутри фазы – теплоотдачей).
Массопередача – процесс перехода вещества (или нескольких веществ) из одной фазы в другую в направлении достижения равновесия. В отличие от теплопередачи, которая происходит обычно через стенку, массопередача осуществляется, как правило, при непосредственном соприкосновении фаз (за исключением мембранных процессов).
Мембрана – полупроницаемая перегородка, пропускающая определенные компоненты жидких или газовых смесей.
Мембранные процессы – избирательное извлечение компонентов смеси или их концентрирование с помощью полупроницаемой перегородки – мембраны. Эти процессы представляют собой переход вещества (или веществ) из одной фазы в другую через разделяющую их мембрану. Применяется для разделения газовых и жидких смесей, очистки сточных вод и газовых выбросов.
Модель «идеального» фильтра – 1) каналы (поры) одинакового диаметра; 2) равномерно распределены по всей площади фильтровальной перегородки; 3) длина каналов равна высоте осадка.
Мокрая очистка газов – промывка газов водой или другой жидкостью.
Молекулярная диффузия – перенос распределяемого вещества, обусловленный беспорядочным тепловым движением молекул, атомов, ионов.
Монодисперсные системы – системы, состоящие из одинаковых по размеру частиц.
Направление массообменных процессов – определение, из какой фазы в какую будет переходить вещество. Причем направление перехода вещества определяется концентрациями вещества в фазах и условиями равновесия (в общем случае разностью химических потенциалов вещества в фазах): вещество переходит из той фазы, где его рабочая концентрация выше равновесной.
Насадки адсорберов – твердые тела различной формы; при наличии насадки увеличивается поверхность соприкосновения газа и жидкости.
Насадки барабанных сушилок: подъемно-лопастная насадка применяется для перемещения крупнокусковых и склонных к налипанию высушиваемых материалов. Распределительные насадки – полочная и крестообразная - применяются при сушке мелкокусковых и сыпучих материалов. При помощи таких насадок обеспечивается многократное пересыпание материала и его тесный контакт с сушильным агентом. Промежуточная, или секторная, насадка применяется для перемещения крупнозернистых высушиваемых материалов, обладающих малой сыпучестью. Ячейковая насадка применяется в процессах сушки тонкоизмельченных пылящих материалов. При пересыпании таких материалов в закрытых ячейках насадки достигается интенсивное перемешивание частиц.
Насыщенный раствор – раствор, находящийся в равновесии с твердой фазой при данной температуре.
Обратный осмос – это способ разделения растворов путем их фильтрования под давлением через полупроницаемые мембраны, пропускающие растворитель и задерживающие молекулы или ионы растворенных веществ.
Оптимальный расход поглотителя находят с помощью технико-экономического расчета, и он соответствует минимуму затрат Зmin.
Осаждение – разделение жидких или газовых неоднородных систем путем выделения из жидкой или газовой фазы твердых или жидких взвешенных частиц; такое выделение осуществляется под действием силы тяжести, центробежной силы, а также под действием сил электрического поля.
Острый водяной пар – пар, вводимый непосредственно в нагреваемую жидкость, при этом образующийся конденсат смешивается с нею.
Относительная влажность – отношение абсолютной влажности к максимально возможному количеству пара в 1 м3 воздуха, при той же температуре и данном барометрическом давлении, характеризует степень насыщения воздуха влагой.
Отрицательная растворимость – растворимость вещества, снижающаяся с повышением температуры.
Перегонка – разделение смеси жидкостей, основанное на различной температуре кипения отдельных веществ, входящих в состав смеси.
Пересыщенный раствор – раствор, в котором концентрация растворенного вещества больше его растворимости.
Периоды сушки. Первый – влага испаряется со всей поверхности влажного материала так же, как она испаряется с зеркала испарения некоторого объема жидкости. В этом периоде скорость сушки постоянна и определяется лишь скоростью внешней диффузии, т.е. диффузии паров влаги с поверхности материала в окружающую среду. Во втором периоде скорость сушки определяется внутренней диффузией – перемещением влаги изнутри материала к его поверхности.
Пермеат – прошедший через мембрану продукт.
Пленочная конденсация пара – образование сплошной пленки конденсата на смачиваемой поверхности.
Пленочное кипение – режим, при котором на поверхности нагрева образуется сплошная пленка пара, периодически прорывающегося в объем жидкости.
Плотность орошения – объем жидкости, проходящей через единицу площади поперечного сечения колонны за единицу времени.
Полезная разность температур – разность температур греющего пара, поступающего в первый корпус, и температуры насыщения вторичного пара из последнего корпуса за вычетом суммы температурных потерь по корпусам.
Полидисперсные системы – системы, состоящие из разных по размеру частиц одного и того же слоя.
Полная депрессия – депрессия, равная сумме температурной, гидростатической и гидравлической депрессий.
Положительная растворимость – растворимость вещества, увеличивающаяся с повышением температуры.
Полупроницаемая мембрана – мелкопористая мембрана, пропускающая через свои поры растворитель и задерживающая растворенное вещество.
Провальные тарелки. В провальных тарелках отсутствуют переливные трубы, вследствие этого газ и жидкость проходят через одни и те же отверстия.
Продолжительность сушки – сумма длительности сушки в период постоянной скорости и длительности ее в период падающей скорости при условии, что падение скорости сушки во втором периоде происходит прямолинейно.
Пролетный водяной пар – неполная конденсация пара, когда из аппарата отводится смесь конденсата и пара. При неполной конденсации пара расход его повышается.
Пузырьковое кипение (ядерное) – режим кипения, при котором паровые пузырьки, достигшие предельного (критического) размера, отрываются от поверхности нагрева, всплывают к свободной поверхности жидкости, возрастая в объеме за счет теплообмена с менее нагретой жидкостью.
Пыль – система, состоящая из газа и распределенных в нем твердых частиц с размерами от 5 до 50 мкм, она образуется преимущественно при дроблении и транспорте твердых материалов.
Рабочая линия процесса – уравнение прямой, выражающее зависимость между рабочими концентрациями: у = Ах + В, (у = f(х)).
Рабочие концентрации (у, х) – действительные концентрации распределяемого вещества, которые всегда отличаются от равновесных.
Равновесие – такое состояние системы, при котором перенос вещества отсутствует.
Равновесная линия – линия, которая либо является кривой, либо, в частном случае, прямой линией и выражается зависимостью у* = f(х) или x* = f(y), (у* = mx или х* = mу) – геометрическое место точек равновесных концентраций.
Равновесные концентрации (у*, х*) – предельные концентрации распределяемого вещества в фазах для данных температуры и давления, установившиеся при равновесии.
Растворимость – способность твердого вещества распределяться путем диффузии в жидкой среде.
Рафинат – жидкая смесь, обедненная извлекаемыми компонентами и обычно содержащая некоторое количество экстрагента.
Режим подвисания – режим, при котором в случае противотока газа и жидкости силы трения равны силе тяжести, действующей на жидкость.
Ретант – оставшаяся перед мембраной разделяемая смесь.
Свободный объем насадки – отношение объема воды к объему, занимаемому насадкой. Если жидкость задерживается в насадке, свободный объем насадки уменьшается, что приводит к увеличению скорости газа, пропорционально квадрату которой возрастает сопротивление насадки.
Сжимаемые и несжимаемые осадки – осадки, получаемые на фильтровальной перегородке при разделении суспензий. Под несжимаемыми понимают такие осадки, в которых порозность, то есть отношение объема пор к объему осадка, не уменьшается при увеличении разности давлений. Порозность сжимаемых осадков уменьшается, а гидравлическое сопротивление потоку жидкой фазы возрастает с увеличением разности давлений.
Ситчатые тарелки имеют отверстия диаметром от 2 до 5 мм; газ проходит через отверстия и барботирует через слой жидкости на тарелке.
Скорость массообменных процессов – количество вещества, переносимое в единицу времени через единицу поверхности контакта фаз.
Скорость начала псевдоожижения wпс - скорость, при которой нарушается неподвижность слоя и он начинает переходить в псевдоожиженное состояние. Начало псевдоожижения наступает при равенстве силы гидравлического сопротивления слоя весу всех его частиц.
Скорость осаждения wос – скорость равномерного движения частицы в среде.
Скорость свободного витания (скорость уноса) wсв – скорость, при которой слой разрушается и начинается массовый унос частиц потоком. Малейшее превышение скорости w0 над величиной wсв приводит к уносу частицы. Таким образом, условие витания частицы в восходящем потоке идентично условию равномерного осаждения частицы в неподвижной среде. Поэтому скорости wсв можно определять так же, как скорости осаждения wос.
Скорость свободного осаждения – скорость, при которой осаждающиеся частицы практически не оказывают влияния на движение друг друга.
Скорость стесненного осаждения - скорость, которая меньше, чем скорость свободного осаждения, вследствие трения и соударений между частицами, а также тормозящего влияния стенок аппарата.
Скорость сушки – количество влаги, испаряемой с единицы поверхности высушиваемого материала за единицу времени.
Скорость тепловых процессов – количество тепла, передаваемое в единицу времени через 1 м2 площади поверхности, нормальной к направлению теплопереноса (плотность теплового потока): q = Q/(Fτ), Вт/м2.
Скорость фильтрования – объем фильтрата, проходящий в единицу времени через 1 м2 фильтровальной перегородки:
 ,
,  .
.
Сплошная среда – среда, в которой не образуется пустот, не заполненных жидкостью. Вещества обладают субмикроскопической молекулярной структурой, причем молекулы разделены пустотами, а масса их сконцентрирована в основном, в ядрах атомов, составляющих молекулы, и, следовательно, распределена по объему вещества далеко не равномерно. Это касается и других свойств веществ. И потому, например, общее описание движения жидкости, понимаемой как материя с молекулярной структурой, заключалось бы в составлении уравнения движения всех молекул в отдельности, что при современном состоянии науки невозможно, да и не всегда необходимо для потребностей практики, где достаточно знать средние значения параметров. Осреднение можно выполнить таким образом, что жидкость (вещество) будет рассматриваться как сплошная среда (континиум).
Сплошная фаза (дисперсионная среда) – внешняя фаза, в которой распределены частицы дисперсной фазы в виде капель, пузырей, пленок.
Средняя разность температур - движущая сила тепловых процессов, в которых изменяется температура хотя бы одного теплоносителя.
Стадии кристаллизации – образование центров кристаллов и рост кристаллов.
Сушка – удаление влаги из твердых влажных материалов в основном путем ее испарения. Этот процесс представляет собой переход влаги из твердого влажного материала в газовую или паровую фазы. Применяют в технике для предварительного обезвоживания перерабатываемых веществ или обезвоживания готового продукта.
Температура мокрого термометра – температура, принимаемая жидкостью при испарении ее после достижения теплового равновесия.
Температура точки росы – температура, соответствующая полному насыщению воздуха водяными парами в процессе охлаждения.
Температурная депрессия – разность между температурами кипения раствора и чистого растворителя.
Теоретическая ступень изменения концентрации (теоретическая тарелка) соответствует некоторому гипотетическому участку аппарата, на котором жидкость полностью перемешивается, а концентрации удаляющихся фаз (например, жидкости и газа) являются равновесными. Методу теоретических ступеней (тарелок) присущи серьезные недостатки, и обоснованный переход от теоретических к действительным тарелкам затруднителен. В связи с этим разработаны более совершенные методы, позволяющие определить аналитически или графически непосредственно число действительных ступеней (тарелок) аппарата.
Теплоемкость удельная - количество теплоты, необходимое для нагревания единицы массы вещества на 1 К.
Теплоотдача – процесс теплообмена между твердым телом и соприкасающейся с ним жидкостью или газом.
Теплопередача – перенос теплоты от более нагретой среды к менее нагретой через разделяющую их стенку.
Теплопроводность (кондукция) – явление молекулярное, которое состоит в том, что перенос теплоты происходит путем непосредственного соприкосновения между микрочастицами.
Термическое сопротивление – величина, обратная тепловой проводимости: для теплоносителя rт=1/a; для стенки rст = S(di/l i.).
Туман – система, состоящая из газа и распределенных в нем капель жидкости с размерами от 0,3 до 3 мкм, образовавшихся в результате конденсации.
Турбулентная диффузия – конвективный перенос вещества, осуществляемый под действием турбулентных пульсаций.
Удельная поверхность а (м2/м3) – поверхность элементов или частиц материала, находящихся в единице объема, занятого слоем.
Удельная теплота фазовых превращений – количество тепла, которое выделяется или поглощается при фазовом превращении единицы массы вещества.
Удельное сопротивления осадка – разность давлений, необходимая для того, чтобы жидкая фаза с вязкостью 1 Па·с фильтровалась со скоростью 1 м/с сквозь слой осадка толщиной 1 м (rос=Dр/mhосW).
Удерживающая способность насадки – количество жидкости, задерживающееся в единице объема насадки.
Ультрафильтрация – это процесс разделения, фракционирования и концентрирования растворов с помощью полупроницаемых мембран. При этом жидкость непрерывно подается в пространство над мембраной под давлением от 0,1 до 1,0 МПа.
Фаза – однородная по химическому составу и физическим свойствам часть термодинамической системы.
Фазовое равновесие – состояние, при котором явного перехода вещества из одной фазы в другую происходить не будет.
Фактор формы
Ф = Fш / F,
где Fш – поверхность шара, имеющего тот же объем, что и рассматриваемое тело с поверхностью F. Например, для куба Ф = 0,806; для цилиндра, высотой в 10 раз превышающий его радиус, Ф = 0,69; для диска, высота которого в 10 раз меньше радиуса, Ф = 0,32. Значения Ф приводятся в справочниках.
Факторы кристаллизации – факторы, определяющие скорость кристаллизации, ими являются степень пересыщения раствора, температура, образование центров кристаллизации, интенсивность перемешивания, наличие примесей в растворе.
Фильтрование – процесс разделения с помощью пористой перегородки, способной пропускать жидкость или газ, но задерживать взвешенные в среде твердые частицы. Оно осуществляется под действием сил давления или центробежных сил и применяется для более тонкого разделения суспензий и пылей, осаждение.
Флегма – жидкость для орошения аппарата, получаемая путем конденсации части пара, имеющего состав, аналогичный составу дистиллята.
Флегмовое число – отношение количества флегмы к количеству дистиллята.
Флокуляция - слипание агрегативно неустойчивых твердых частиц.
Флотация – процесс разделения мелких твердых частиц (например, минералов), основанный на различии в их смачиваемости водой. Применяется, в частности, для обогащения полезных ископаемых.
Число единиц переноса – изменение рабочей концентрации распределяемого между фазами вещества, приходящееся на единицу движущей силы; обратно пропорционально средней движущей силе процесса массопередачи.
Число тарелок равно числу вертикальных отрезков ступенчатой линии между начальным и конечным составами газа.
Экстракция – извлечение растворенного в одной жидкости вещества другой жидкостью, практически не смешивающейся или частично смешивающейся с первой. Этот процесс представляет собой переход извлекаемого вещества из одной жидкой фазы в другую. Процесс применяют для извлечения растворенного вещества или группы веществ сравнительно невысоких концентраций.
Экстра-пар – вторичный пар, частично отводимый на сторону и используемый для предварительного нагрева раствора, поступающего на выпаривание, или для других технологических целей, не связанных с выпариванием.
Эмульсия – система, состоящая из жидкости и распределенных в ней капель другой жидкости, не растворяющейся в первой. Величина частиц дисперсной фазы в этом случае колеблется в довольно широких пределах.
Энтальпия – количество теплоты, необходимое для нагревания единицы массы вещества от 00С до данной температуры.
Эффективность перемешивания характеризует качество проведения процесса перемешивания и может быть выражена по-разному в зависимости от цели перемешивания. Эффективность перемешивания зависит не только от конструкции перемешивающего устройства и аппарата, но и от величины энергии, вводимой в перемешиваемую жидкость.
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
Общий
1. Дытнерский, Ю.И. Процессы и аппараты химической технологии: учебник для вузов / Ю.И. Дытнерский. – М.: Химия, 1995. – Ч.1, 2.
2. Касаткин, А.Г. Основные процессы и аппараты химической технологии / А.Г. Касаткин. – 9-е издание. – М.: Госхимиздат, 2005. – 754 с.
3. Плановский, А.Н. Процессы и аппараты химической и нефтехимической технологии / А.Н. Плановский, П.И. Николаев. – М.: Химия, 1987. – 540 с.
4. Плановский, А.Н. Процессы и аппараты химической технологии / А.Н. Плановский, В.Н. Рамм, С.З. Коган. – Л.: Химия, 1968. – 847 с.
5. Гельперин, Н.И. Основные процессы и аппараты химической технологии / Н.И. Гельперин, И.Н. Гельперин. – М.: Химия, 1981. – 812 с.
6. Айнштейн, В.Г. Общий курс процессов и аппаратов химической технологии: учебник для вузов / В.Г. Айнштейн, М.К. Захаров, Т.А. Носов. – М.: Химия, 1999. - Кн.1 – 888 с.
7. Павлов, К.Ф. Примеры и задачи по курсу процессов и аппаратов химической технологии / К.Ф. Павлов, П.Г. Романков, П.П. Носков. – Л.: Химия, 2004. – 576 с.
8. Руководство к практическим занятиям в лаборатории процессов и аппаратов химической технологии: учебное пособие / под ред. П.Г. Романкова. – 6-е изд., перераб. – Л.: Химия, 1990. – 256 с.
9. Коган, В.Б. Теоретические основы типовых процессов химической технологии / В.Б. Коган. – Л.: Химия, 1977. – 592 с.
К модулю № 5
10. Аэров, М.Э. Гидравлические и тепловые основы работы аппаратов со стационарным и кипящим зернистым слоем / М.Э. Аэров, О.М. Тодес. – Л.: Химия, 1968.
11. Протодьяконов, И.О. Гидромеханика псевдоожиженного слоя / И.О. Протодьяконов, Ю.Г. Чесноков. – Л.: Химия, 1982.
12. Протодьяконов, И.О. Гидромеханические основы процессов химической технологии / И.О. Протодьяконов, Ю.Г. Чесноков. – Л.: Химия, 1987.
13. Романков, П.Г. Гидромеханические процессы химической технологии / П.Г. Романков, М.Л. Курочкина. – Л.: Химия, 1974.
14. Балабеков, О.С. Очистка газов в химической промышленности: процессы и аппараты / О.С. Балабеков, Л.Ш. Балтабаев. – М.: Химия, 1991.
15. Стренк, Ф. Перемешивание и аппараты с мешалками / Ф. Стренк. – Л.: Химия, 1975.
16. Штербачек, З. Перемешивание в химической промышленности / З. Штербачек, П. Тауск. – Л.: Госхимиздат, 1963.
17. Буевич, Ю.А. Струйное псевдоожижение / Ю.А. Буевич, Г.А. Минаев. – М.: Химия, 1984.
18. Броунштейн, Б.И. Гидродинамика, массо- и теплообмен в коллоидных аппаратах / Б.И. Броунштейн, В.В. Щеголев. – Л.: Химия, 1988.
19. Броунштейн, Б.И. Гидродинамика, массо- и теплообмен в дисперсных системах / Б.И. Броунштейн, Г.А. Фишбейн – Л.: Химия, 1977.
К модулю № 6
20. Андреев, В.А. Теплообменные аппараты для вязких жидкостей. Основы расчета и проектирования / В.А. Андреев. – Л.: Госэнергоиздат, 1961.
21. Маньковский, О.Н. Теплообменная аппаратура химических производств (инженерные методы расчета) / О.Н. Маньковский. – Л.: Химия, 1976.
22. Промышленные тепломассообменные процессы и установки / под ред. А.М. Бакластова. – М.: Энергоатомиздат, 1986.
23. Пленочная тепло- и массообменная аппаратура / под ред. В.М. Олевского. – М.: Химия, 1988.
24. Теория тепломассообмена / под ред. А.И. Леонтьева. – М.: Высшая школа, 1979.
25. Теплообменники-конденсаторы в процессах химической технологии: моделирование, расчет, управление. – М.: Химия, 1991.
26. Таубман, Е.И. Выпаривание / Е.И Таубман. – М.: Химия, 1982.
27. Теория тепломассообмена / под ред. А.И. Леонтьева. – М.: Высшая школа, 1980.
28. Гидродинамические и тепломассообменные процессы в химической аппаратуре / под ред. В.В. Консетова, И.С. Павлушенко. – Л.: Машиностроение, 1964.
К модулю № 7
29. Заминян, А.П. Абсорберы с псевдоожиженной насадкой / А.П. Зиминян, В.М. Рамм. – М.: Химия, 1980.
30. Кальцев, Н.В. Основы адсорбционной техники / Н.В. Кальцев. – Л.: Химия, 1984.
31. Лукин, В.Д. Регенерация адсорбентов / В.Д. Лукин, И.С. Анцыпович. – Л.: Химия, 1983.
32. Путилов, А.Д. Адсорбционно-каталитические методы очистки газовых сред в химической технологии / А.Д. Путилов. – М.: Химия, 1989.
33. Рамм, В.М. Абсорбция газов / В.М. Рамм. – М.: Химия, 1976.
34. Серпионова, Е.Н. Промышленная адсорбция газов и паров / Е.Н. Серпинова. – М.: Высшая школа, 1969.
35. Лукин, В.Д. Регенерация адсорбентов / В.Д. Лукин, И.С. Анцыпович. – Л.: Химия, 1983.
36. Заминян, А.П. Абсорберы с псевдоожиженной насадкой / А.П. Заминян, В.М. Рамм. – М.: Химия, 1935.
37. Александров, И.А. Ректификационные и абсорбционные аппараты (методы расчета и основы проектирования) / И.А. Александров. – М.: Химия, 1978.
38. Багатуров, С.А. Основы теории и расчета перегонки и ректификации / С.А. Багатуров – М.: Химия, 1974.
39. Зельвенский, Я.Д. Ректификация разбавленных растворов / Я.Д. Зельвенский. – Л.: Химия, 1974.
40. Петлюк, Ф.Б. Многокомпонентная ректификация / Ф.Б. Петлюк, П.А. Серафимов. – М.: Химия, 1983.
41. Белоглазов, И.Н. Твердофазные экстракторы / И.Н. Белоглазов. – Л.: Химия, 1985.
42. Берестова, А.Н. Жидкостные экстракторы / А.Н. Берестова, И.Н. Белоглазов. – Л.: Химия, 1982.
43. Зюлковский, З. Жидкостная экстракция в химической промышленности / З. Зюлковский. – Л.: Госхимиздат, 1963.
К модулю № 8
44. Куц, П.С. Теплофизические и технологические основы сушки высоковольтной изоляции / П.С. Куц, И.Ф. Пикус. – Минск: Наука и техника, 1979.
45. Лыков, Н.В. Сушка в химической промышленности / Н.В. Лыков. – М.: Химия, 1970.
46. Муштаев, В.И. Сушка в условиях пневмотранспорта / В.И. Муштаев. – М.: Химия, 1984.
47. Муштаев, В.И. Сушка дисперсных материалов / В.И. Муштаев, В.М. Ульянов. – М.: Химия, 1988.
48. Романков, П.Г. Сушка во взвешенном состоянии. Теория, конструкции, расчет / П.Г. Романков, Н.Б. Рашковская. – Л.: Химия, 1968.
49. Романков, П.Г. Сушка в кипящем слое / П.Г. Романков, Н.Б. Рашковская. – Л.: Химия, 1964.
50. Рашковская, Н.Б. Сушка в химической промышленности / Н.Б. Рашковская. – Л.: Химия, 1977.
51. Романков, П.Г. Сушка перегретым паром / П.Г. Романков, Ю.Л. Михайлов. – М.: Химия, 1967.
52. Сажин, Б.С. Основы техники сушки / Б.С. Сажин. – М.: Химия, 1984.
53. Томас, Д. Мембранная фильтрация / Д. Томас. – М.: Мир, 1987.
54. Дытнерский, Ю.И. Мембранное разделение газов / Ю.И. Дытнерский. – М.: Химия, 1991.
55. Дытнерский, Ю.И. Мембранные процессы разделения жидких смесей / Ю.И. Дытнерский. – М.: Химия, 1975.
56. Николаев, Н.И. Диффузия в мембранах / Н.И. Николаев. – М.: Химия, 1980.
57. Дытнерский, Ю.И. Обратный осмос и ультрафильтрация / Ю.И. Дытнерский. – М.: Химия, 1978.
Учебное издание
Денисов Юрий Николаевич
Орлова Наталья Алексеевна
Пазников Евгений Александрович
Химической технологии
Часть 2
Типовые процессы и аппараты
Химической технологии
Редактор Идт Л.И.
Корректор Малыгина И.В.
Технический редактор Сазонова В.П.
Подписано в печать 29.09.10. Формат 60×84 1/16
Усл. п. л. – 9,07. Уч.-изд. л. – 9,75.
Печать – ризография, множительно-копировальный
аппарат «RISO EZ300»
Тираж 50 экз. Заказ 2010−144
Издательство Алтайского государственного
технического университета
656038, г. Барнаул, пр-т Ленина, 46
Оригинал-макет подготовлен ИИО БТИ АлтГТУ
Отпечатано в ИИО БТИ АлтГТУ
659305, г. Бийск, ул. Трофимова, 27
Бийский технологический институт (филиал)
государственного образовательного учреждения
высшего профессионального образования
«Алтайский государственный технический университет
им. И.И. Ползунова»
Ю.Н. Денисов, Н.А. Орлова, Е.А. Пазников
Последнее изменение этой страницы: 2019-04-10; Просмотров: 415; Нарушение авторского права страницы