
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Методы исследования при заболеваниях почекСтр 1 из 8Следующая ⇒
Методы исследования при заболеваниях почек
(Учебное пособие)
Алматы, 2010г.
УДК: 616.61-071 ББК: 56.9 Г: К 15
РЕЦЕНЗЕНТЫ:
Касенова Сауле Лаиковна - заведующая кафедрой внутренних болезней №4 КазНМУ им. С.Д. Асфендиярова, доктор медицинских наук, профессор
Рыскулова Алма Рахимовна - заведующая кафедрой профилактической медицины Казахстанского медицинского университета, кандидат медицинских наук, доцент
Г: К 15. д.м.н., профессор Канатбаева Асия Бакишевна с соавторами – Алматы, 2009. ______ страниц
ISBN __________________________________
В диагностике и лечении заболеваний почек огромное значение имеет целенаправленное применение методов исследования. Успешная работа специализированных отделений нефрологии и гемодиализа зависит от возможности обследования больных путем внедрения новых методов диагностики, основанных на доказательной медицине. За последние 20 лет диагностические методы в нефрологии подверглись существенному совершенствованию. Старые методы упрощены и стандартизированы. Внедряются новые технологии, многие из которых становятся доступными. Для успешного внедрения новых методов современный врач должен сам знать не только принципы и показания к их применению, но и уметь оценить результаты обследования. При выборе диагностического метода имеет значение информативность и безопасность метода. Также следует обращать внимание на стоимость. Учебное пособие предназначено для студентов ВУЗов, интернов, врачей нефрологов, урологов. Оно полезно для семейных врачей, терапевтов, педиатров, врачей смежных специальностей, к которым могут обратиться почечные больные.
ББК: 56.9
Одобрено и разрешено к печати членами ЦМС КазНМУ им. С.Д. Асфендиярова
Протокол № _____ от « _____ » _____________ 200 г.
Содержание
· Исследования мочи ………………………………………………..……………… 6 · Исследования крови ………………………………………………..…………….. 12
Для своевременной и точной диагностики почечных заболеваний важны как простые исследования мочи и крови, так и сложные исследования: специальные биохимические, иммунологические, морфологические, генетические методы. Отдельные исследования (ангиография, радионуклидные методы и др.) требуют специального оборудования. Точный диагноз требует не просто проведение серии обследования и констатации результатов, а создание диагностической концепции у конкретного больного. Важен учет таких факторов, как наибольшая информативность, современность, безопасность и стоимость предполагаемого метода исследования. В каждом конкретном случае поэтапное применение методов исследования с использованием алгоритмов облегчает диагностику того или другого заболевания. План обследования нефрологического больного основывается на синдромно-нозологическом принципе диагностики. При этом используется схема: · Выявление ведущего синдрома · Установление нозологической основы путем проведения дифференциального диагноза · Оценка функций почек (в начале и при динамическом наблюдении)
Лабораторные методы исследования
1. Исследования мочи. 2. Исследования крови. 3. Функциональные методы исследования. 4. Инструментальные методы исследования. 5. Биопсия почки и морфологические методы исследования биоптата. 6. Мониторинг лекарственных препаратов. 7. Методы молекулярной биологии. 8. Методы молекулярной генетики.
Исследования мочи
В моче исследуют рН, осмотическую концентрацию или относительную плотность, белки, глюкозу, осадок мочи и проводят микробиологические и биохимические исследования. Это – достаточно простые и информативные методы. Также следует знать современные дорогостоящие методы с высокими диагностическими возможностями, используемые в последние годы в развитых странах (протеомика мочи). Общий анализ мочи (ОАМ) – наиболее часто используемый метод. В настоящее время количественные (Аддиса-Каковского, Амбурже) и полуколичественные (Нечипоренко) пробы признаны неудобными и не имеют преимуществ перед ОАМ. Суточный сбор мочи показан только для оценки суточной протеинурии при невозможности определения протеин/креатининового коэффициента. Для проведения анализа необходимо исследование утренней свежевыпущенной мочи со средней порции без применения стабилизаторов с целью уменьшения вероятности ошибок, связанных с бактериальным разложением и другими факторами. Можно исследовать вторую и последующие порции мочи, полученные в течение дня. Экономичным и точным методом скринингового исследования мочи является применение тест-полосок (качественный анализ). В случае отсутствия гематурии/ гемоглобинурии или лейкоцитурии, протеинурии, глюкозурии, необходимость в микроскопическом исследовании мочи отпадает. При обнаружении хотя бы одной из вышеуказанных патологических находок необходимы дальнейшие количественные биохимические и микроскопические исследования. Глюкозурия обычно свидетельствует о гипергликемии, однако может носить и изолированный характер (почечная глюкозурия) или сочетаться с нарушениями других функций проксимальных почечных канальцев (синдром Фанкони). Глюкозурия иногда встречается при нефротическом синдроме и на фоне стероидной терапии.
Протеинурия – один из главных признаков заболевания почек, маркер локализации и тяжести почечного повреждения. Однако, следует помнить, что при таких состояниях, как лихорадка, значительная физическая нагрузка, хроническая сердечная недостаточность и инфекция мочевой системы, может иметь место транзиторное (преходящее) повышение альбумина в моче. В норме с мочой выделяются различные белки (альбумин, глобулин и др.), количество которых незначительно. Суточная протеинурия в норме не превышает 150мг/сут. Рутинные методы исследования (тест-полоски, проба с сульфосалициловой кислотой) не выявляют выделяющиеся в норме белки. При патологии уровень протеинурии растет. Поэтому диагностическое значение имеет определение суточного количества белка в моче, а также электрофоретическая дифференциация видов белка (альбумин, α 1, α 2 -микроглобулин, β 2-микроглобулин, белок Тамма-Хорсфаля и др.). При качественной пробе (тест-полоски) используется шкала: - отрицательный результат; - 1+ 0, 3 г/л; - 2++ 1 г/л; - 3+++ свыше 5 г/л Таким образом, диагностические полоски на протеинурию позволяют выявить содержание белка 300 мг/л и выше. При этом преимущественно определяется альбумин. При положительном результате (желательно повторить анализ) следует перейти на количественное определение белка. Для нивелирования различной концентрации веществ в моче используют определение суточной протеинурии. Для этого собирают суточную мочу и производят пересчет концентрации белка в моче (г/л) на суточный диурез (г/сут). Более удобен новый метод вычисления протеин/креатининового коэффициента, который позволяет определить суточную экскрецию белка без сбора 24-часовой мочи. Принцип основан на том, что креатинин выделяется путем клубочковой фильтрации и экскреция его постоянна в течение суток. С помощью вычисления отношения концентрации любого вещества (включая белок) в моче к уровню креатинина в моче, можно определить суточную экскрецию этих веществ (Na, K, Ca и др., табл.5). концентрация веществ и креатинина может выражаться в ммоль, мг или г/л. При расчете суточной протеинурии чаще белок определяют в мг или г, а креатинин в ммоль. Оба вещества могут определяться в г/л. В зависимости от этого протеин/креатининовый коэффициент в норме равен: у взрослых < 11 мг/ммоль или < 0, 2 (при расчете в г/л). Альбумин/креатининовый коэффициент у взрослых < 2, 3 мг/ммоль. Нормы протеинурии у детей представлены в табл.4. Таблица 4. Нормы протеинурии у детей
После вычисления коэффициента (К) «белок/креатинин» суточная протеинурия (СП) рассчитывается по следующей формуле:
СП=(150-возраст) х вес х 0, 0014 х К
В моче содержатся разнообразные белки. Клиническое значение имеет определение альбумина (гломерулярный белок) и тубулярных белков в моче у детей (рис.1). Суточная альбуминурия в норме не превышает 20 мг/сут. Незначительная альбуминурия в пределах 20-200 мг/сут (называемая микроальбуминурией - МАУ) имеет важное клиническое значение как ранний индикатор поражения почек при сахарном диабете и эссенциальной артериальной гипертонии. МАУ может определяться качественно (30-300 мг/л) специальными тест-полосками или количественно анализаторами. Тубулярные белки требуют специального оборудования для определения, тест-полоски их не определяют.
Рисунок 1. Дифференциация протеинурии (Схема)
В моче содержатся белки и неплазменного происхождения. 50% всех белков мочи образуется в мочевыводящем тракте, основным из которых является белок Тамма-Хорсфалля. Наиболее точными являются новые технологии электрофореза - нефелометрические методы определения белков-маркеров (альбумин, α 1-микроглобулин и др.). этот, пока малодоступный и дорогой метод, позволяет быстро дифференцировать гломерулярную и тубулярную дисфункции, отдельно выявляя альбумин и α -микроглобулин. С недавнего времени, используемый в развитых странах протеомный анализ мочи, предоставил возможность дальнейшего совершенствования неинвазивных методов диагностики заболеваний почек (рис.2).
Внедрение этого дорогостоящего метода в будущем позволит дифференцировать такие болезни, как Ig A нефропатия, фокально-сегментарный гломерулосклероз без биопсии почек. При заболеваниях почек, связанных с гематологическими, онкологическими болезнями, увеличивается экскреция парапротеинов с мочой. Парапротеины появляются в избыточном количестве при множественной миеломе, амилоидозе, макроглобулинемии Вальденстрема (протеинурия переполнения). Одним из них является белок Бенс-Джонса. Он не определяется обычными тест-полосками и требует специального исследования легких цепей иммуноглобулинов. Свойством белка Бенс-Джонса является осаждение при термической обработке сульфосалициловой кислотой.
Экскреция химических веществ в моче. Также определяется с использованием креатининового коэффициента (КК). Уровень экскреции химических веществ с мочой зависит от возраста детей и для правильной оценки рекомендуется руководствоваться нормативами (табл.5).
Таблица 5: Экскреция веществ с мочой по креатининовому коэффициенту в возрастном аспекте (95-й перцентиль) [по данным Matos V. с соавт., J. Pediatr. (1997)131: 252–257].
Большинство детей старше 2-х лет при нормальном питьевом режиме имеют уровень креатинина мочи 5±4 ммоль/л. Может быть ошибка «разведения мочи», когда креатинин мочи составляет около 2 ммоль/л или «концентрирования мочи» при концентрации около 12 ммоль/л. При концентрации альбумина в моче 1 г/л, то есть при 50-кратном его повышении, расчет КК не требуется. КК всех веществ у грудных детей выше, чем у старших детей. Это связано не с повышенной их экскрецией, а со сниженной экскрецией креатинина из-за малой мышечной массы. Норма КК у новорожденных детей в 4 раза выше, чем у старших детей. При определении КК необходимость в определении суточной экскреции веществ отпадает. Для правильной интерпретации экскреции электролитов (Na, K, Ca, Mg, Cl, P) с мочой важно знать их уровни в сыворотке крови и суточный прием. Учесть последний фактор удается редко, за исключением случаев парентерального введения электролитов. Например, при гипокалиемии 3.0 ммоль/л калийурия - 20 ммоль/л свидетельствует о почечной потере калия. При гиперкалиемии 6.5 ммоль/л калийурия - 20 ммоль/л – признак почечной недостаточности с задержкой калия, так как здоровые почки должны экскретировать калий в повышенных количествах – около 80 ммоль/л и выше. Особое внимание необходимо обращать на экскрецию кальция, так как ее повышение сопряжено с высоким риском нефрокальциноза и нефролитиаза. Определение экскреции органических кислот (цитраты, оксалаты, ураты) проводится при подозрении на гипероксалурию, гипо- или гиперцитратурию, гипоурикозурию. Это исследование выполняется в специальных лабораториях (дорогостоящий метод). Для определения рН и относительной плотности мочи используются рутинные методы. Точное определение рН (рН-метрия) имеет значение при нарушении экскреции водородных ионов (первичные и вторичные тубулопатии), процессах камнеобразования и инфекциях мочевых путей. Микроскопия мочи. Микроскопия мочи позволяет дифференцировать эритроцитурию от гемо, - миоглобинурии. Гематурия – частый симптом и может встречаться при многих заболеваниях: от тяжелых (гломерулонефрит) до доброкачественной гематурии у детей. В норме эритроциты в моче отсутствуют или могут быть не более 3-5 в поле зрения. Распространенность асимптоматической микрогематурии у детей школьного возраста составляет 0.5-2.0% случаев (у девочек выше, чем у мальчиков), макрогематурии – 0.13% [по данным Filler G, и Ehrich JHH., Kidney International (2005) 67: 2321-2324]. При микроскопии осадка мочи выявленные эритроциты нужно дифференцировать на ренальные или гломерулярные (дисморфные) и постренальные (не измененные), что возможно при использовании фазово-контрастной микроскопии. Опытный нефролог может распознать дисморфные эритроциты с помощью обычного светового микроскопа при увеличении в 400 раз. Дальнейшая дифференциация дисморфных эритроцитов на подгруппы проводится в редких случаях по показаниям из-за дороговизны (рис. 3, 4, 5). Выявление т.н. акантоцитов, клеток Шнуллера безусловно свидетельствует о гломерулярной патологии.
Рис.5. Электронная микроскопия различных эритроцитов. (Из: Haber M.H. Urine microscopy and clinical significance. Chocago: American Society of Clinical Pathologists. 1976.) Гломерулярная гематурия диагностируется при достаточном количестве дисморфных эритроцитов (напр. 200 эр/мл). Обнаружение эритроцитарных цилиндров в осадке мочи свидетельствует о гломерулярной патологии и исследуется только в неясных случаях. Количественный подсчет клеток в суточной моче по методу Аддиса не удобен, не информативен вследствие ошибок сбора мочи и спонтанного разрушения клеток. Главным показателем бактериальной инфекции мочевой системы (ИМС) является лейкоцитурия. Однако лейкоцитурия не всегда является следствием бактериальной ИМС. Например, стерильная лейкоцитурия может быть при тубулоинтерстициальном нефрите, нефролитиазе. При кандидозе или аденовирусной ИМС лейкоцитурия может отсутствовать. Проба Нечипоренко в данное время уже не используется, в виду того, что она не может считаться количественной, так как не учитывается время, за которое собрана моча и к тому же не имеет преимуществ перед общим анализом мочи. При микроскопическом исследовании мочи можно при необходимости дифференцировать лейкоциты по морфологии (напр. эозинофилы при интерстициальном нефрите). Выявление подоцитов и клеток париетального эпителия боуменовой капсулы в моче - дорогой метод диагностики почечного повреждения, требующий специально оборудованной лаборатории. При нефролитиазе рекомендуется определение суточной экскреции кальция, цистина и оксалатов в моче. Микроскопическая дифференциация кристаллов не информативна. При бактериурии микробиологическое исследование дает более точные данные о количестве и свойствах микроорганизмов. Степень бактериурии определяют методом Гоулда. Диагностическое значение имеет бактериурия 105 м.т. в 1 мл мочи и выше. Выявление в моче грибковой флоры является основанием для постановки диагноза кандидозной ИМС. Цилиндры. Гиалиновые цилиндры образуются в почечных канальцах из белка Тамма-Хорсфаля. Они быстро растворяются в щелочной среде и иногда встречаются в нормальной моче. Их количество возрастает при приеме диуретических средств, повышении температуры тела и физической нагрузке, но особенно значительно при почечной патологии. Наличие в моче зернистых и клеточных цилиндров свидетельствует о патологических изменениях в почечной паренхиме. Эритроцитарные цилиндры указывают на поражение клубочков (гломерулонефрит). Лейкоцитарные цилиндры – признак острого пиелонефрита. Количество гиалиновых цилиндров увеличивается при протеинурии. При СКВ характерен «телескопический» осадок с широким набором клеток и цилиндров. Жировые цилиндры встречаются при нефритическом синдроме, восковидные – признак ХПН (формируются при расширении канальцев почек).
2. Исследования крови
Общий анализ крови. Общий клинический анализ крови выявляет неспецифические симптомы, позволяющие заподозрить патологию почек. К примеру, лейкоцитоз с резким нейтрофилезом и повышение СОЭ у лихорадочных больных с симптомами интоксикации могут оказаться ведущими признаками острого пиелонефрита, что требует обязательного общего и бактериологического исследования мочи. Эти симптомы особенно характерны для детей младшего возраста. Уровень повышения СОЭ и определение С-реактивного белка помогает в определении активности воспалительного процесса при острых и хронических гломерулярных болезнях (первичный гломерулонефрит, люпус-нефрит, амилоидоз почек и др.). Выявление эозинофилии с эозинофилурией может помочь в диагностике интерстициального нефрита аллергической природы. Для больных с хроническим прогрессирующим заболеванием почек характерно постепенное развитие нормохромной анемии из-за нарушения синтеза эритропоэтина. Раннее развитие анемии характерно для детей с врожденными структурными поражениями почек (нефронофтиз Фанкони, дисплазия почек). Необходимо следить за уровнем гемоглобина (Нв) у больных с сахарным диабетом и поражением почек. В то же время у пациентов с поликистозом почек даже в терминальной стадии почечной недостаточности в клетках стенок кист продолжает синтезироваться эритропоэтин и не развивается анемия. Иммунологические методы У 1/3 больных с терминальной почечной недостаточностью причиной является иммунно-опосредованное заболевание почек или системное заболевание. Иммунологические методы исследования представлены в табл. 8.
Таблица 8. Иммунологические исследования крови при заболеваниях почек
Используется оценка состояния системы комплемента путем определения общей гемолитической активности (СН50) и концентрации С3 и С4 в сыворотке. Определение других компонентов показано лишь при низких значениях СН50 на фоне нормального уровня С3 и С4. Низкая концентрация С4 свидетельствует о развитии классического пути активации комплемента, тогда как снижение концентрации С3 указывает на альтернативный механизм активации системы комплемента. При остром постинфекционном гломерулонефрите (ГН) возможна активация обоих механизмов со снижением С3 и С4, но эти изменения носят преходящий характер. При длительной гипокомплементемии необходимы дополнительные исследования. При мембрано-пролиферативном ГН II типа («с плотными депозитами») характерно снижение концентрации С3 и наличие С3-нефритического фактора. Определение концентрации комплемента имеет значение при системной красной волчанке, нефрите на фоне бактериального эндокардита и инфекции предсердно-желудочкового шунта (табл. 9). Иммуноглобулины. У 50% больных с IgA нефропатией и ее системным вариантом (болезнь Шенлейн-Геноха) определяется повышение IgA в сыворотке крови. У некоторых больных при нефротическом синдроме с минимальными изменениями повышена концентрация общего IgЕ, что может указать на аллергическую природу заболевания. Парапротеинемия определяется при множественной миеломе, амилоидозе и смешанной криоглобулинемии. Количественное определение иммунных комплексов при заболеваниях почек не имеет большого диагностического значения. Таблица 9. Значение исследования комплемента (50-90 мг/дл) при заболеваниях почек
Криоглобулины – это иммунные комплексы, выпадающие в осадок при низкой температуре. Они имеют значение при системных заболеваниях с развитием криоглобулинемии (эссенциальный, вторичный). Аутоантитела. При системной красной волчанке (СКВ) обнаруживают большое количество разнообразных аутоантител. В нефрологической практике обычно определяют антинуклеарный фактор и антитела к двойной спирали ДНК (в 70%). При системных васкулитах обнаруживают анти-нейтрофильные цитоплазматические антитела. (АНЦА, которые в норме < 10 U/l). Есть 2 вида АНЦА (АNCA): p-ANCA – обнаруживают при микроскопическом полиангиите, синдроме Чарга-Стросса, васкулите Шенлейн-Геноха c-ANCA – при гранулематозе Вегенера. Антитела к гломерулярной базальной мембране (anti-GBM-antibody) имеют значение для диагностики одной из причин быстропрогрессирующего (экстракапиллярного) гломерулонефрита - синдрома Гудпасчера.
Биопсия почек Постановка диагноза многих гломерулярных и тубулоинтерстициальных болезней невозможна без чрескожной пункционной биопсии почки. Показаниями к биопсии являются: стероидрезистентный нефротический синдром (НС), острый нефритический синдром с почечной недостаточностью, подозрение на быстропрогрессирующий гломерулонефрит или тубулоинтерстициальный нефрит (исключение – постстрептококковый ГН), системные заболевания с вовлечением почек (СКВ, пурпура Шенлейн-Геноха и др. (см. табл.. 11)). Биопсия является золотым стандартом диагностики причин дисфункции почечного трансплантата. Открытая биопсия проводится в исключительных случаях, например, при подозрении на опухоль. Биопсия не показана при часто рецидивирующем стероидчувствительном НС, за исключением подозрения на нефротоксичность, обусловленную циклоспорином А. При длительной изолированной протеинурии биопсия показана не всегда (зависит от динамики и функций почек). Противопоказания для биопсии – единственная почка (относительное), эктопия почки, некурабельное нарушение свертывающей системы крови или неконтролируемая артериальная гипертензия (табл. 11).
Таблица 11. Показания и противопоказания к биопсии почек.
Примерный протокол биопсии почки, используемый в детской клинике Ганновера (Германия), а также в РДКБ «Аксай» (г. Алматы) приведен в приложении 4. Для биопсии почек используются различные биопсийные пистолеты: одноразовые (фирмы Galeni, Италия), автоматические со съемными одноразовыми иглами (фирмы Bard Magnum, США) и др. Биопсия почек проводится под контролем УЗИ опытным нефрологом либо хирургом в условиях стационара. Процедура относительно простая и занимает около 15-20 минут. Осложнения встречаются редко. Риск незначительного преходящего кровотечения составляет 5-10%. Чаще всего наблюдается гематома в околопочечную клетчатку (57-85%), которая рассасывается. Редкие осложнения – артерио-венозная фистула и/или профузное кровотечение (0, 1-0, 2%). Морфологические исследования Репрезентативный для морфологического диагноза почечный биоптат должен содержать минимум 10 клубочков и артерию. Морфологическое исследование почечного биоптата включает три исследования: световую (СМ), иммуногистохимическую (ИГХ) или иммунофлюоресцентную и электронную (ЭМ) микроскопии. Для СМ и ИГХ почечная ткань, фиксированная в 4% забуференном формалине (минимум 2 часа), заключается в гомогенизированный парафин с последующим получением серийных срезов толщиной не более 2-3 μ м на ротационном микротоме. Для ЭМ берется содержащий клубочки кусочек биоптата длиной около 1 мм, фиксированный в 2, 5% глютаральдегиде. Световая микроскопия Серийные срезы располагаются на 16 предметных стеклах, по 3 на каждом, для окраски методами: Гематоксилин-эозин, Шика (PAS), серебрение по Джонсу. Остальные неокрашенные стекла предназначены для дополнительных гисто- (Конго красный на амилоид) и иммуногистохимических исследований. Иммуногистохимия Определяются следующие показатели: IgG, IgM, IgA, C3, C1 q, C4d (при трансплантированной почке). Дополнительные показатели: каппа и лямбда легкие цепи (для выявления поражения почки при миеломной болезни и др.), SV40 (полиома-вирус в трансплантированной почке) и др. Электронная микроскопия Приготовление препаратов для ЭМ включает: заключение в эпоксидные смолы, получение полу- и ультратонких срезов, помещение их на медные сетки с контрастированием. Схема морфологии нормального клубочка приведена на рис. 11.Основные морфологические изменения, которые учитываются нефропатологом при постановке диагноза, а также типы гломерулонефритов перечислены в табл. 12 и 13.
Таблица 12. Основные морфологические изменения при заболеваниях почек
Таблица 13. Морфологические типы гломерулонефритов (ГН).
Рисунок 11. Морфология клубочка в норме. Примеры некоторых гломерулярных заболеваний представлены на рисунках 12-14. 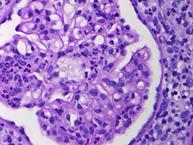 а. а.  б. б. 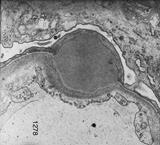 в. Рисунок. 12. Диффузный пролиферативный ГН (пост-инфекционный ГН). (Из: UpToDate. Version 17.2) а) СМ – увеличенный клубочек с окклюзией просветов некоторых капилляров из-за выраженной эндокапиллярной пролиферации, в основном за счет нейтрофилов (PAS). б) ИГХ – диффузное глобальное гранулярное отложение С3с в гломерулярной базальной мембране и мезангии.в) ЭМ – крупный субэпителиальный электронно-плотный депозит («горб»). в. Рисунок. 12. Диффузный пролиферативный ГН (пост-инфекционный ГН). (Из: UpToDate. Version 17.2) а) СМ – увеличенный клубочек с окклюзией просветов некоторых капилляров из-за выраженной эндокапиллярной пролиферации, в основном за счет нейтрофилов (PAS). б) ИГХ – диффузное глобальное гранулярное отложение С3с в гломерулярной базальной мембране и мезангии.в) ЭМ – крупный субэпителиальный электронно-плотный депозит («горб»). 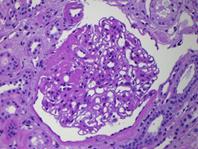 а. а. 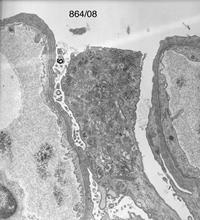 б. Рисунок. 13. Фокально-сегментарный гломерулосклероз. (Из: UpToDate. Version 17.2) а) СМ – увеличенный клубочек с сегментарным склерозом и гиалинозом, с небольшой мезангиальной пролиферацией и увеличением мезангиального матрикса (PAS). б) ЭМ – расплавление ножек подоцитов. б. Рисунок. 13. Фокально-сегментарный гломерулосклероз. (Из: UpToDate. Version 17.2) а) СМ – увеличенный клубочек с сегментарным склерозом и гиалинозом, с небольшой мезангиальной пролиферацией и увеличением мезангиального матрикса (PAS). б) ЭМ – расплавление ножек подоцитов. 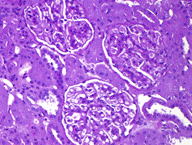 а. а. 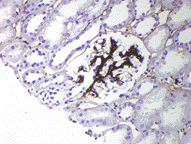 б. б. 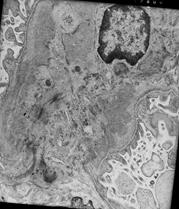 в. Рисунок. 14. IgA-нефропатия. (Из: UpToDate. Version 17.2)а) СМ – Диффузное умеренное расширение мезангиального матрикса и мезангиальная пролиферация (PAS). б) ИГХ – значительное отложение IgA в мезангии. в) ЭМ – электронноплотные депозиты в мезангии. Основными причинами дисфункции почечного трансплантата являются острое отторжение, нефротоксичность ингибиторов кальцинейрина, полиомавирусный тубулоинтерстициальный нефрит (рис. 15, 16, 17). в. Рисунок. 14. IgA-нефропатия. (Из: UpToDate. Version 17.2)а) СМ – Диффузное умеренное расширение мезангиального матрикса и мезангиальная пролиферация (PAS). б) ИГХ – значительное отложение IgA в мезангии. в) ЭМ – электронноплотные депозиты в мезангии. Основными причинами дисфункции почечного трансплантата являются острое отторжение, нефротоксичность ингибиторов кальцинейрина, полиомавирусный тубулоинтерстициальный нефрит (рис. 15, 16, 17). 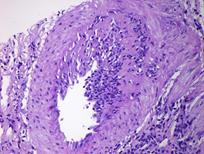 Рисунок. 15. Тяжелое острое сосудистое отторжение Banff III. Выраженный интимальный и трансмуральный артериит (PAS). (Из: UpToDate. Version 17.2) Рисунок. 15. Тяжелое острое сосудистое отторжение Banff III. Выраженный интимальный и трансмуральный артериит (PAS). (Из: UpToDate. Version 17.2) 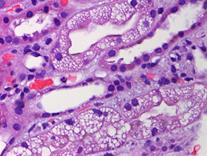 а. а. 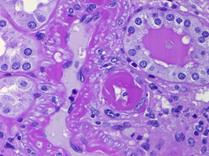 б. Рисунок. 16. Нефротоксичность ингибиторов кальцинейрина. (Из: UpToDate. Version 17.2)а) Острая: изометрическая вакуолизация тубулярного эпителия (Г-Э). б) Хроническая: нодулярный гиалиноз небольшой артерии (PAS). б. Рисунок. 16. Нефротоксичность ингибиторов кальцинейрина. (Из: UpToDate. Version 17.2)а) Острая: изометрическая вакуолизация тубулярного эпителия (Г-Э). б) Хроническая: нодулярный гиалиноз небольшой артерии (PAS). 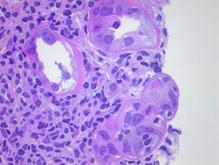 а. а.  б. Рисунок. 17. Полиомавирусный тубулоинтерстициальный нефрит. (Из: UpToDate. Version 17.2)а) СМ – увеличенные ядра клеток тубулярного эпителия с характерными тельцами включения, выраженная инфильтрация интерстиция мононуклеарами (PAS). б) ИГХ – выраженная позитивность на антиген полиомавируса (SV40). б. Рисунок. 17. Полиомавирусный тубулоинтерстициальный нефрит. (Из: UpToDate. Version 17.2)а) СМ – увеличенные ядра клеток тубулярного эпителия с характерными тельцами включения, выраженная инфильтрация интерстиция мононуклеарами (PAS). б) ИГХ – выраженная позитивность на антиген полиомавируса (SV40).
ПРИЛОЖЕНИЯ Приложение 1. Суточный мониторинг артериального давления у детей.
Мальчики
Девочки
Приложение 2. Основные биохимические показатели сыворотки крови, в норме Популярное:
|
Последнее изменение этой страницы: 2016-03-17; Просмотров: 2480; Нарушение авторского права страницы