
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Тема 3 - 9: МОЛЕКУЛЯРНЫЙ УРОВЕНЬ: ОБЩАЯ ХАРАКТЕРИСТИКА. ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ.Стр 1 из 8Следующая ⇒
Тема 3 - 9: МОЛЕКУЛЯРНЫЙ УРОВЕНЬ: ОБЩАЯ ХАРАКТЕРИСТИКА. ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ. Характеристика молекулярного уровня. С этого уровня начинаются процессы жизнедеятельности организма: обмен веществ и энергии, передача наследственной информации и др. Это уровень биологических макромолекул: белков, липидов, углеводов, нуклеиновых кислот. Из этих молекул строятся сложные химические соединения, различающиеся по строению и функциям. Из атомов строятся → молекулы → биополимеры (б.ж.у, нуклеиновые кислоты). Биополимеры – это органические соединения, входящие в состав клеток живых организмов, представляющие собой цепь, состоящую из многочисленных звеньев - мономеров. От греч. «р olys» - многочисленный Молекула полимера состоит из многих тысяч соединенных между собой мономеров, которые могут быть одинаковыми или разными. От числа и разнообразия мономеров, образующих полимер зависят свойства биополимеров. Для каждого вида биополимеров характерно определенное строение и функции. Мономеры – строительные блоки крупных органических молекул полимеров.
Биополимеры универсальны, так как построены по одному плану у всех живых организмов. Молекулы б.ж.у, нуклеиновых кислот рассматриваются как биополимеры только в клетке. Вне клетки биополимеры теряют биологическое значение и характеризуются только свойствами того класса соединений, к которым относятся. Разнообразные свойства биополимеров обусловлены различными сочетаниями всего лишь нескольких типов мономеров, образующих много вариантов длинных полимерных цепей. Этот принцип лежит в основе многообразия жизни на нашей планете.
Химический состав клетки. Самыми распространенными элементами земной коры, на долю которых приходится 90% ее атомарного состава, являются: О, Si, Al и Mg. Далее следуют Са, Fe, Na, P и другие элементы. В живых организмах обнаружено около 90 химических элементов. Биогенные элементы - химические элементы, выполняющие в клетке биологические функции. Таких элементов 27. МАКРОЭЛЕМЕНТЫ - 90 % массы клетки: Н2, О2, N2, C ( Органогенные (биофильные) элементы), а также Ca, K, Na, Mg, Fe, Cl, S, P ( их концентрация превышает 0, 001%). МИКРОЭЛЕМЕНТЫ - менее 0, 001% массы клетки: В, Cu, Zn, Mn, F, I , Мо, Со, Br. УЛЬТРАМИКРОЭЛЕМЕНТЫ – менее 0, 000001% или следовые количества: уран (U), радий (Ra), золото (Аu), ртуть (Hg), бериллий (Be), цезий (Cs), селен (Se). ВЫВОД: таким образом, элементарный состав живой и неживой природы одинаков, что свидетельствует об их материальном единстве. Провести четкую грань между живым и неживым на уровне атомов не представляется возможным. Молекулярный состав живого вещества Неорганические соединения – вода и минеральные вещества встречаются и в живой и в неживой природе. Органические вещества – углеводы, жиры, белки, нуклеиновые кислоты характерны только для живых организмов. Содержание неорганических и органических веществ в клетке
ВЫВОД: молекулярный состав живой и неживой природы различен, поэтому на молекулярном уровне можно провести между ними четкую границу. Вода и ее роль в клетке. Вода – одно из самых распространенных веществ на Земле, она покрывает большую часть земной поверхности и входит в состав всех живых организмов. Вода составляет почти 80% массы клетки (в головном мозге – 85%, в клетках развивающегося зародыша – 90%, в мышечных 76%, в жировой ткани 40%, в клетках эмали зубов воды 10%, как и в клетках покоящихся семян). Две трети (65%) массы человека составляет вода. Человек может прожить без воды несколько суток, верблюд 12 дней, медведь, сурок в спячке 2 месяца. Потеря организмом 20% воды может привести к смерти. В клетках молодого организма воды – около 80%, а в клетках старого – только 60%. ВЫВОД: чем больше воды в клетке, тем интенсивнее в ней идут обменные процессы. Для выращивания 1 кг растительной пищи (зерновые, овощи и т.д.) нужно 2 т. Н2О; 1 кг мяса – 20 т.; 1 человек в год потребляет 360 т. Н2О. В обычной воде 1: 6800 соотношение Н2О: Н3О (дейтерий - тяжелая вода). Снеговая Н2О содержит меньше Н3О, ее применение повышает в 2 раза яйценоскость, вес птицы, а при замочке семян урожайность повышается в 3 раза. Минеральные соли. Минеральные соли клетки в виде ионов или в твердом состоянии. Из катионов важны K +, Na +, C а2+, Mg 2+, NH 3 +. Из анионов H2 PO4-, H PO42 - Cl-, HCO3-, NO3-, PO43-, CO32 -. Концентрация ионов K+ внутри клетки выше, а Na+ низкая. В окружающей клетку среде (крови, морской воде) все наоборот. От концентрации солей зависит БУФЕРНОСТЬ – способность клетки сохранять определенную концентрацию водородных ионов (pH). В клетке поддерживается слабощелочная реакция (pH 7, 2). Буферными называют растворы, содержащие смесь слабой кислоты и ее растворимой соли. Внутри клетки буферность обеспечивают анионы – H2 PO4- , HPO42 - - это фосфатная буферная система . Вне клетки бикарбонатная система HCO3- , H2CO3. Нерастворимые в организме соли – фосфат кальция входит в состав межклеточного вещества костной ткани, в раковины моллюсков; панцири губок, диатомовых, красных водорослей - известковые или кремниевые. Исторические сведения. Вначале 18 в. итальянец Беккари получил первый очищенный белок – клейковину пшеницы. В 19в. француз Бракконо провел кислотный гидролиз белка и в полученном растворе обнаружил сладковатое вещество – аминокислоту глицин. В 20 в. установлено строение инсулина. Белки, их содержание в живом веществе и молекулярная масса.
Содержание белков в различных клетках колеблется от 50-80%. В животных клетках – 20%, в вегетативных органах культурных растений количество белков достигает 5—15% веса сухой ткани, в семенах злаков – 10—20%, в семенах бобовых и масличных культур – 25—35%. Синтезируются в гранулярной ЭДС на рибосомах. Уровни организации белков. (молекулы белков принимают разные пространственные формы – конформации, которые являются 4-я уровнями организации белка)
Тема: ФЕРМЕНТЫ. Катализатор - это вещество, которое ускоряет реакцию, не расходуясь. ФЕРМЕНТЫ (от лат. fermentum – брожение, закваска), или энзимы – биологические катализаторы белковой природы. Некоторые молекулы РНК имеют свойства ферментов. Сегодня известно 2 тыс. ферментов. Первый фермент – уреаза был выделен в 1926 г. американским биохимиком Дж. Самнером. Она катализирует расщепление мочевины. Без уреазы она протекала бы 3 млн. лет. (NH2)2CO+H2O уреаза→ CO2↑ +2NH3 В одной клетке 100 разных ферментов, работающих при t =5 - 40º С (предпочитают t = 4-37 º c), при 60 º С денатурируют. Название фермента от названия субстрата + окончание –«аза». Субстрат – в-во на которое действует фермент. Например,
Примеры работы ферментов
СВОЙСТВА ФЕРМЕНТОВ: 1. Ферменты – глобулярные белки; 2. Увеличивают скорость реакции, но сами не расходуются; 3. Не влияют на свойства конечного продукта; 4. Малое количество фермента превращает большое количество субстрата; 5. Активность фермента зависит от t, рН, концентрации субстрата и фермента. Например, пепсин активен при рН < 7; при рН > 7 трипсин, липаза, каталаза; рН = 7 амилаза слюны; 6. Катализируемая реакция обратима; 7. Фермент специфичен, т.е. каждый фермент действует на определенный субстрат: формула «один фермент – один субстрат». ГИПОТЕЗА «КЛЮЧА И ЗАМКА» Выдвинута 1890 г. Э.Фишером: субстрат подходит к ферменту, как ключ к замку. Субстрат сравнивается с «ключом», который подходит к «замку» – ферменту.
ФЕРМЕНТЫ
КОФАКТОРЫ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| · Неорганические ионы (например, для активации фермента амилазы слюны, необходимы ионы хлора (Сl–); · Простетические группы (ФАД, гем), прочно связанные с ферментом. · Коферменты (НАД, НАДФ, кофермент А), непрочно связанные с ферментом. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Голофермент – комплекс фермента с кофактором.
Апофермент – ферментная часть голофермента.
Тема: УГЛЕВОДЫ.
Углеводы (Сахариды) - это органические вещества с общей формулой Сх(Н2О)у, где х и у могут иметь разное значение.
Название «углевод» отражает тот факт, что водород и кислород присутствуют в молекуле в тех же соотношениях, что и в молекуле воды.
В животных клетках 2 - 5% углеводов (печень, мышцы).
В растительных клетках 90% углеводов от сухой массы.
Синтезируются в хлоропластах, эгранулярной ЭДС.
Полисахариды
ПОЛИСАХАРИДЫ 1-го порядка (олигосахариды ) – ди, - три, тетрасахара.
Дисахариды – углеводы, образованные остатками двух моносахаридов. Например, сахароза, лактоза, мальтоза.
 Сахароза С12Н22О11 – тростниковый (свекловичный сахар). Состоит из глюкзы+фруктозы. Содержится в семенах, ягодах, корнях, клубнях, плодах.
Сахароза С12Н22О11 – тростниковый (свекловичный сахар). Состоит из глюкзы+фруктозы. Содержится в семенах, ягодах, корнях, клубнях, плодах.
Растения, из которых получают сахар в промышленности:
а — сахарная свекла; б — сахарный тростник
ПОЛИСАХАРИДЫ 2 -го порядка- сахара, состоящие из большого числа моноз, соединенных ковалентными связями.

Растительные продукты – поставщики крахмала и целлюлозы:
а — картофель; б — кукуруза; в — зерно; г — хлопчатник; д — древесина
Функции углеводов.
В суточном рационе человека и животных преобладают углеводы. Травоядные получают крахмал, клетчатку, сахарозу. Хищники получают гликоген с мясом.
Тема: ЛИПИДЫ.
ЛИПИДЫ (от греч. lí pos — жир) (жиры и жироподобные вещества) – это гидрофобные органические вещества, которые можно извлечь из клеток органическими растворителями – эфиром, хлороформом и бензолом. В клетке липиды составляют 5 - 15% от сухой массы; в жировой ткани – 90%.
Синтезируются в агранулярной ЭДС.
Классические липиды – это сложные эфиры жирных кислот и трехатомного спирта глицерина. Их называют триглицериды.

Связь между жирной кислотой и трехатомным спиртом глицерином называют сложноэфирной связью.
Где R1, R2, R3 – радикалы жирных кислот. Они неполярные, гидрофобные. Остаток глицерина гидрофилен.
ЖИРНЫЕ КИСЛОТЫ – небольшие органические молекулы, содержащие углеводородную цепь (гидрофобная) и карбоксильную группу (гидрофильная).
Формула жирной кислоты R-СООН, где R атом водорода или алкильный радикал СН3 и т.д.
ПРИМЕРЫ ЖИРНЫХ КИСЛОТ
| Название жирной кислоты | Формула |
| ПАЛЬМИТИНОВАЯ | СН3-(СН2)15-СООН |
| СТЕАРИНОВАЯ | СН3-(СН2)16-СООН |
| ОЛЕИНОВАЯ | СН3-(СН2)7-СН=СН-(СН2)7-СООН |
Жирные кислоты делят на 2 группы:
1. Насыщенные (предельные) т.е. не содержат двойных связей. Например, стеариновая, пальмитиновая.
2. Ненасыщенные (непредельные) т.е. содержат двойные связи. Например, олеиновая.
Триглицериды принято делить на жиры и масла в зависимости от того, остаются ли они твердыми при 20 C (жиры) или имеют при этой температуре жидкую консистенцию (масла).
Растительные жиры или масла богаты непредельными жирными кислотами. Они легкоплавки и жидки при комнатной температуре. Например, в оливковом масле глицерин связан с остатками олеиновой жирной кислоты.

Классификация липидов.

ДНК. Репликация ДНК.
Хранитель наследственной информации растений и животных – молекула ДНК.
Молекула ДНК – 2-е спирально правосторонне закрученные, одна вокруг другой, антипараллельные цепи. (модель 1953г. Уотсона и Крика).

Полный оборот спирали (шаг спирали) приходится на 3, 4 нм, т.е. на 10 пар нуклеотидов, под углом 36º друг к другу (винтовая лестница); диаметр ДНК =2нм, длина молекулы=100.000нм; m=6 * 10-12гр.
Характеристика ДНК:
1. Мономерами ДНК являются дезоксирибонуклеотиды.
Нуклеотидный состав проанализирован американским биохимиком Чаргаффом. Он обнаружил, что в ДНК количество пуриновых оснований = количеству пиримидиновых (А=Т, Г=Ц) – это правило Чаргаффа.
2. Каждый нуклеотид состоит из сахара – дезоксирибозы, азотистого основания и Н3РО4. Нуклеотид с азотистым основанием А - адениловый, Т-тимидиловый, Г-гуаниловый, Ц-цитидиловый

3. Каждая нить ДНК – это полинуклеотид. Длинная цепь, в которой в строго определенном порядке расположены нуклеотиды. Они соединены между собой через углевод одного нуклеотида и Н3РО4 соседнего с помощью ковалентных фосфоэфирных связей, образуя сахарофосфатный остов.
4. Вторая цепь ДНК достраивается по принципу комплементарности.
Комплементарность (от lat. сomplementum – дополнение) – это принцип дополнения при котором пары нуклеотидов строго соответствуют друг другу, имеют одинаковый размер, в результате диаметр ДНК по всей ее длине одинаков. А=Т, Г≡ Ц
5. Между нуклеотидами первой и второй цепи образуются водородные связи.
Цепи антипараллельны: 3′ конец одной цепи напротив 5′ конца другой.

6. ДНК находится в хромосомах, митохондриях, хлоропластах.
РЕПЛИКАЦИЯ ДНК.
Репликация ДНК - удвоение ДНК. Доказана в 1958г. Мезелсоном и Сталем.
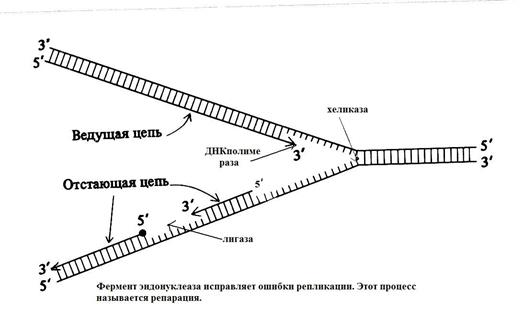
1. Двойная спираль временно раскручивается под действием фермента хеликазы одновременно в нескольких местах.
Репликон (единица репликации ) – участок между двумя точками репликации.
Репликативная вилка – расплетенный участок ДНК, в котором начинается репликация.

2. Разрываются водородные связи, но сохраняются фосфоэфирные.
3. Фермент ДНК- полимераза, в присутствии АТФ, непрерывно присоединяет нуклеотиды по принципу комплементарности от 5′ → 3′ концу. Так синтезируется ВЕДУЩАЯ ЦЕПЬ, а от 3′ → 5′ дочерняя часть молекулы синтезируется фрагментами Оказаки. Фрагменты Оказаки сшиваются вместе ДНК - лигазой. Так синтезируется ОТСТАЮЩАЯ ЦЕПЬ молекулы ДНК.
В результате репликация идет по полуконсервативному механизму: синтезируются 2-е молекулы ДНК, у каждой из которых одна половина молекулы - материнская, а другая вновь синтезированная - дочерняя.
РНК.
1. РНК – нуклеиновая кислота, обеспечивающая процесс синтеза белка.
2. РНК - одноцепочечная молекула.
3. РНК – это полимер, состоящий из мономеров – рибонуклеотидов.
4. Каждый нуклеотид состоит из сахара – рибозы, азотистого основания и Н3РО4. Нуклеотид с азотистым основанием А - адениловый, Г-гуаниловый, Ц-цитидиловый, У – уридиловый(урацил вмасто тимина)

5. Каждая нить РНК – это полинуклеотид. Длинная цепь, в которой в строго определенном порядке расположены нуклеотиды. Они соединены между собой через углевод одного нуклеотида и Н3РО4 соседнего с помощью ковалентных связей.
6. РНК находится в ядрышке, рибосомах, цитоплазме, митохондриях, пластидах.
7. Существует 3 типа РНК:
· Матричная (мРНК) или информационная (иРНК);
· Рибосомальная (рРНК);
· Транспортная (тРНК).
Матричная (мРНК) или информационная (иРНК) (5% от всех видов РНК)
Синтезируется на ДНК и содержит информацию о структуре белка. Созревание мРНК происходит путем вырезания незначащих участков – интронов.
Рибосомальная (рРНК)(85% от всех видов РНК)
Синтезируется в ядрышке, образует активный центр рибосомы, где идет биосинтез.
Транспортная (тРНК)(10% от всех видов РНК)
Образуется в ядре на ДНК и переходит в цитоплазму. Они самые мелкие (70-100 нуклеотидов) имеет форму листа клевера с двумя активными участками:
1. триплет – АНТИКОДОН комплементарен триплету на иРНК;
2. АКЦЕПТОРНЫЙ УЧАСТОК - посадочный участок для аминокислоты.
АНТИКОДОН – последовательность оснований, строго соответствующая той аминокислоте, которую переносит данная тРНК.

1. универсальная петля, 2. дополнительная петля
АТФ.
АТФ - это нуклеотид, содержащий:
· азотистое основание АДЕНИН;
· сахар – рибозу;
· три фосфатные группы.
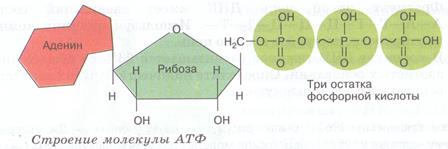
АТФ – универсальный переносчик энергии в биологических системах. Находится в цитоплазме. При отщеплении двух ее концевых фосфатных групп выход энергии на каждую из них составляет по 40кДж. Эти фосфатные группы соединены между собой высокоэнергетическими – МАКРОЭРГИЧЕСКИМИ связями.
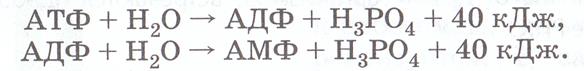
Отщепление третьей фосфатной группы АТФ дает 13, 8 кДж.
АТФ – аденозинтрифосфат.
АДФ - аденозиндифосфат.
АМФ - аденозинмонофосфат.
Фосфорилирование – это процесс образования АТФ.
АТФ синтезируется в процессе клеточного дыхания в митохондриях и в процессе фотосинтеза в хлоропластах.
Тема 3 - 9: МОЛЕКУЛЯРНЫЙ УРОВЕНЬ: ОБЩАЯ ХАРАКТЕРИСТИКА. ХИМИЧЕСКИЙ СОСТАВ КЛЕТКИ.
Последнее изменение этой страницы: 2019-06-19; Просмотров: 108; Нарушение авторского права страницы