Занятие № 9 Тема: «Коллоидные растворы: получение, очистка и свойства. Коагуляция коллоидных растворов. Коллоидная защита».
1. Вопросы для обсуждения:
1. Классификация дисперсных систем.
2. Методы получения и очистки коллоидных растворов. Гемодиализ, применение в медицине.
3. Строение мицеллы гидрофобного коллоидного раствора. Виды потенциалов: термодинамический (j) и электрокинетический (z).
4. Свойства коллоидных растворов:
а) оптические свойства (светорассеяние, поглощение света). Эффект Тиндаля;
б) молекулярно-кинетические свойства (броуновское движение, диффузия, осмос, седиментация);
в) электрокинетические свойства (электрофорез, электроосмос, потенциалы течения и оседания).
5. Виды устойчивости и факторы устойчивости коллоидных растворов. Коагуляция. Правило Шульце-Гарди.
6. Применение коллоидных растворов в медицине. Коллоидная защита.
7. Высокомолекулярные соединения. Биополимеры. Классификация и особенности строения и свойств ВМС.
8. Грубо- и коллоиднодисперсные системы. Эмульсии. Полуколлоиды. Мыла. Порошки. Суспензии. Гели, их структура, свойства.
2. Ситуационные задачи:
1. К 250 мл 0, 001 М раствора BaCl2 добавили 50 мл 0, 1 М Na2SO4 раствора.
а) Написать мицеллярную формулу;
б) Определить, какой из перечисленных электролитов вызовет коагуляцию этого золя с наименьшим порогом коагуляции: KCl, NаBr, LiNO3?
Решение:
а) BaCl2 + Na2SO4 → BaSO4¯ + 2NaCl
Определяем, какой из растворов находится в избытке:
n (BaCl2) = C´ Vр-ра = 0, 001´ 0, 25 = 2, 5´ 10-4 моль
n (Na2SO4) = C´ Vр-ра = 0, 1´ 0, 05 = 5´ 10-3 моль Þ В избытке Na2SO4.
Мицеллярная формула гидрофобного золя:
BaCl2 + Na2SO4 ( изб.) → BaSO4¯ + 2NaCl
мицелла
 | |
| |
потенциалопределяющие
ионы
 | |
| |
{[BaSO4] m ∙ n SO42-∙ 2(n-x) Na+}2x- 2x Na+
| | | | | |
агрегат адсорбционный диффузионный слой
| | слойпротивоионов противоионов
ядро
| |
гранула
б) Т.к. гранула имеет отрицательный заряд, то по правилу Шульце-Гарди коагуляцию этого золя будут вызывать катионы сильных электролитов. Поэтому наибольшим коагулирующим действием обладает KCl, т.к. при одинаковом заряде +1, имеет наибольший радиус в ряду Li – Na – K.
2. Пороги коагуляции некоторого золя электролитами KNO3, MgCl2, NaBr равны соответственно 50, 0; 0, 8; 49, 0 ммоль/л. Рассчитать коагулирующую способность электролитов. Как относятся между собой величины коагулирующих способностей этих веществ? Указать коагулирующие ионы. Определить заряд коллоидной частицы?
Решение: Коагулирующее действие (g) - величина, обратная порогу коагуляции.



MgCl2 обладает наибольшим коагулирующим действием. Согласно правилу Шульце-Гарди: коагуляцию коллоидных растворов вызывают ионы, знак заряда которых противоположен знаку заряда гранулы. Коагулирующее действие тем сильнее, чем выше заряд иона-коагулянта (g = f(z6) – коагулирующее действие иона-коагулянта пропорционально его заряду в шестой степени):
g (Na+) ׃ g (Na+) ׃ g (Mg2+) = 0, 0204 ׃ 0, 02 ׃ 1, 25 = 1 ׃ 1 ׃ 62, 5
Так как анионы во всех данных электролитах однозарядны, то ионами-коагулянтами являются катионы, а следовательно, заряд коллоидной частицы – отрицательный.
3. К 4 л золя гидроксида железа (III) добавили 0, 92 мл 10%-ного раствора сульфата магния (плотность 1, 1 г/мл), при этом произошло помутнение раствора. Рассчитать порог коагуляции золя сульфат ионами.
Решение: Определяем массу MgSO4, вызвавшего коагуляцию, и его количество: 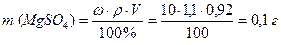
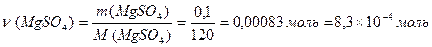
ν (SO42-) = ν (MgSO4) = 8, 3´ 10-4 моль.
Определяем порог коагуляции по формуле:


3. Выполнить тестовые задания (письменно):
|
|
| Золь серы получен при смешивании спиртового раствора серы с избытком воды. Какой метод получения коллоидного раствора был использован?
|
|
| А
| Химическая конденсация
|
|
| Б
| Пептизация
|
|
| В
| Метод замены растворителя
|
|
| Г
| Механическое диспергирование
|
|
|
|
|
|
|
| Согласно правила Панетта-Фаянса, на поверхности кристаллического твердого адсорбента из раствора адсорбируется тот ион, который:
|
|
| А
| Входит в состав кристаллической решетки адсорбента
|
|
| Б
| Не входит в состав кристаллической решетки адсорбента
|
|
| В
| Образует с одним из ионов решетки труднорастворимое соединение
|
|
| Г
| Образует с одним из ионов решетки хорошо растворимое соединение
|
|
|
|
|
|
|
| Указать ион, формирующий потенциалопределяющий слой мицеллы гидрофобного золя: CuCl2 + K2S (избыток) →
|
|
| А
| S2-
|
|
| Б
| K+
|
|
| В
| Cu2+
|
|
| Г
| Cl-
|
|
|
|
|
|
|
| Указать ядро мицеллы гидрофобного золя: CaCl2(избыток) + Na2CO3 →
|
|
| А
| [(CaCO3)m, nCl-]
|
|
| Б
| [(Na2CO3)m, nCl-]
|
|
| В
| [(CaCO3)m, nCa2+]
|
|
| Г
| [(CaCl2)m, nCa2+]
|
|
|
|
|
|
|
| Указать наиболее эффективный метод очистки водного коллоидного раствора крахмала от примесей BaSO4.
|
|
| А
| Диализ
|
|
| Б
| Электродиализ
|
|
| В
| Ультрафильтрация
|
|
| Г
| Фильтрация
|
|
|
|
|
|
|
| Указать наиболее эффективный метод очистки коллоидного раствора белка от примесей глюкозы.
|
|
| А
| Диализ
|
|
| Б
| Электродиализ
|
|
| В
| Ультрафильтрация
|
|
| Г
| Фильтрация
|
|
|
|
|
|
|
| Указать наиболее эффективный метод очистки коллоидного раствора белка от примеси (NH4)2SO4.
|
|
| А
| Диализ;
|
|
| Б
| Электродиализ;
|
|
| В
| Ультрафильтрация
|
|
| Г
| Фильтрация
|
|
|
|
|
|
|
| Метод очистки крови от токсичных низкомолекулярных веществ:
|
|
| А
| Фильтрация
|
|
| Б
| Центрифугирование
|
|
| В
| Гемодиализ
|
|
| Г
| Электродиализ
|
|
|
|
|
|
|
| Образование светящегося конуса при прохождении света через коллоидный раствор (эффект Тиндаля) является результатом
|
|
| А
| Поглощения света коллоидными частицами
|
|
| Б
| Рассеяния света молекулами дисперсионной среды
|
|
| В
| Рассеяния света коллоидными частицами
|
|
| Г
| Поглощения света молекулами дисперсионной среды
|
|
|
|
|
|
|
| Какое из свойств коллоидных растворов не относится к молекулярно-кинетическим:
|
|
| А
| Броуновское движение
|
|
| Б
| Коагуляция
|
|
| В
| Осмотическое давление
|
|
| Г
| Седиментация
|
|
|
|
|
|
|
| Электрокинетический потенциал – это потенциал возникающий на:
|
|
| А
| Границе мицеллы и воды
|
|
| Б
| Границе между диффузным и адсорбционным слоем
|
|
| В
| Границе между ядром и потенциалопределяющими ионами
|
|
| Г
| Поверхности электродов, опущенных в раствор коллоида
|
|
|
|
|
|
|
| Электрофорез – это:
|
|
| А
| Движение гранул через полупроницаемую мембрану
|
|
| Б
| Движение дисперсионной среды относительно неподвижной дисперсной фазы
|
|
| В
| Движение частиц дисперсной фазы в электрическом поле
|
|
| Г
| Движение мицелл под действием электрического тока
|
|
|
|
|
|
|
| Электроосмос – это:
|
|
| А
| Движение частиц дисперсной фазы в электрическом поле
|
|
| Б
| Движение мицелл под действием электрического тока
|
|
| В
| Движение гранул через полупроницаемую мембрану
|
|
| Г
| Движение дисперсионной среды относительно неподвижной дисперсной фазы
|
|
|
| Седиментационная устойчивость коллоидных растворов – это
|
|
| А
| Способность коллоидных частиц сохранять дисперсность
|
|
| Б
| Свойство коллоидных частиц не оседать под действием силы тяжести
|
|
| В
| Устойчивость коллоидных растворов при добавлении ВМС
|
|
| Г
| Необратимая агрегация дисперсной фазы
|
|
|
|
|
|
|
| Агрегативная устойчивость коллоидных растворов – это
|
|
| А
| Необратимая агрегация дисперсной фазы
|
|
| Б
| Способность коллоидных частиц сохранять дисперсность
|
|
| В
| Устойчивость коллоидных растворов при добавлении ВМС
|
|
| Г
| Свойство коллоидных частиц не оседать под действием силы тяжести
|
|
|
|
|
|
|
| Коагуляция коллоидных частиц - это
|
|
| А
| Свойство коллоидных частиц не оседать под действием силы тяжести
|
|
| Б
| Механическое диспергирование дисперсной фазы
|
|
| В
| Необратимая агрегация дисперсной фазы
|
|
| Г
| Способность коллоидных частиц сохранять дисперсность
|
|
|
|
|
|
|
| Минимальная концентрация электролита, при которой начинается коагуляция, называется:
|
|
| А
| Коагулирующей способностью
|
|
| Б
| Потенциалом течения
|
|
| В
| Коллоидной защитой
|
|
| Г
| Порогом коагуляции
|
|
|
|
|
|
|
| Какой ион обладает большим коагулирующим действием на коллоидный раствор с отрицательно заряженной гранулой:
|
|
| А
| Вa2+
|
|
| Б
| SO42-
|
|
| В
| PO43-
|
|
| Г
| Ca2+
|
|
|
|
|
|
|
| Какой ион обладает большим коагулирующим действием на коллоидный раствор с положительно заряженной гранулой:
|
|
| А
| Na+
|
|
| Б
| SO42-
|
|
| В
| PO43-
|
|
| Г
| Ca2+
|
|
|
|
|
|
|
| Коллоидной защитой называется повышение агрегативной устойчивости золя:
|
|
| А
| При введении неиндифферентного электролита
|
|
| Б
| Увеличением степени дисперсности коллоидных частиц
|
|
| В
| При введении индифферентного электролита
|
|
| Г
| При введении высокомолекулярного соединения (ВМС)
|
4. Задания для самостоятельного решения (выполнить письменно):
1. Построить мицеллу гидрофобного золя, записать мицелярную формулу согласно уравнения и обозначить составные структурные компоненты мицеллы:
CuSO4 + Na2S →
Избыток
2. К 100 мл 0, 03%-ного раствора NaCl (плотность 1 г/мл) добавили 250 мл 0, 001 М раствора AgNO3. Построить мицеллу и написать мицеллярную формулу. Какой из перечисленных электролитов вызовет коагуляцию этого золя с наименьшим порогом коагуляции: KCl, Ba(NO3)2, K2CrO4, MgSO4, AlCl3?
3. К 1, 5 л золя сульфида золота добавили 570 мл раствора хлорида натрия с концентрацией 0, 2 моль/л, при этом произошло помутнение раствора. Рассчитать порог коагуляции золя ионами натрия.
5. Тематика рефератов по учебно-исследовательской работе студентов (УИРС).
Популярное:
- Адсорбционные методы выделения кофеина из водных растворов.
- Банковская система: структура, функции, роль.
- Загрязнение и очистка воздуха на предприятиях мясной промышленности
- Занятие № 1. Тема: Правила работы со световым микроскопом. Особенности строения растительной клетки.
- Занятие № 11 Тема: «Биогенные s– , p– и d– элементы: биологическая роль, применение в медицине. Рубежная контрольная №1».
- Занятие № 14. Тема: Империя заднежгутиковые: царство настоящие грибы: отделы хитридиомицеты и зигомицеты.
- Занятие № 5. Тема: строение побега. Метаморфозы побега.
- Занятие № 6. Тема: порядок астроцветные, или сростнопыльниковые: семейство сложноцветные, или астровые.
- Занятие № 9. Тема: порядок чешуецветные, или мятликоцветные: семейство злаки, или мятликовые.
- Занятие №12 Тема: «Классификация, номенклатура, изомерия органических соединений. Взаимное влияние атомов. Сопряжение. Ароматичность. Реакционная способность углеводородов».
- Занятие №14 Тема: «Углеводы. Строение и химические свойства моно-, ди- и полисахаридов».

