
|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |

|
Архитектура Аудит Военная наука Иностранные языки Медицина Металлургия Метрология Образование Политология Производство Психология Стандартизация Технологии |
Микросомальное окисление веществ
В микросомах находятся ферментные цепи окисления веществ. Они представлены двумя короткими цепями переноса электронов и протонов, вмонтированными в мембраны эндоплазматической цепи или микросом. Когда говорят о микросомальном окислении, имеют в виду эти цепи.
 Одна из них монооксигеназная цепь окисления, в которой источником электронов и протонов является НАДФН∙ Н+. Она является основной в процессе микросомального окисления. Последовательность переноса электронов и протонов представлена на рисунке: Одна из них монооксигеназная цепь окисления, в которой источником электронов и протонов является НАДФН∙ Н+. Она является основной в процессе микросомального окисления. Последовательность переноса электронов и протонов представлена на рисунке:
Н2О
Рис. 7. Схема монооксигеназной цепи микросомального окисления.
Источником НАДФН∙ Н+ для монооксигеназной цепи является пентозофосфатный цикл (ПФЦ). НАДФН∙ Н+ – зависимая монооксигеназная цепь микросом состоит из флавопротеина (ФП2), коферментом которого служит ФАД, и цитохрома Р450. Флавопротеин обладает НАДФН∙ Н+ – дегидрогеназной активностью, причем ФАД акцептирует 2Н+ и 2e-. С флавопротеинов электроны транспортируются на цитохром Р450, а протоны в окружающую среду. Цитохром Р450 последнее самоокисляющееся звено этой цепи. Как и все цитохромы он относится к гемопротеинам. Белковая часть цитохрома Р450 представлена одной полипептидной цепью. Молекулярная масса цитохрома Р450 около 50000 Д. Он способен образовывать комплексы с оксидом углерода (II). Такой комплекс имеет максимум поглощения при 450 нм, отсюда и название данного цитохрома. Цитохром Р450 выполняет двойную функцию: он активирует кислород посредством переноса на него электронов и использует активированный кислород для окисления вещества (R) и образования воды. В результате один атом кислорода включается в окисляемое вещество (RO), а другой, связывая два Н+ из среды, входит в состав воды. В целом процессы, происходящие при работе монооксигеназной цепи можно представить следующим образом:
 RH + O2 + НАДФН∙ Н+ ROH + H2O + НАДФ+ RH + O2 + НАДФН∙ Н+ ROH + H2O + НАДФ+
 R - CH = CH - R R - CH - CH - R R - CH = CH - R R - CH - CH - R

Другая – редуктазная цепь окисления, в которой источником электронов и протонов служит НАДН∙ Н+, источником которого, в свою очередь, является гликолиз. Редуктазная цепь микросомального окисления несет вспомогательную для монооксигеназной цепи функцию, обеспечивая дополнительный приток туда водорода и электронов, что имеет очень большое значение, поскольку восстановленный НАДФ является относительно дефицитным продуктом. НАДН∙ Н+ – зависимая редуктазная цепь окисления содержится не только в мембранах микросом, она имеется также в наружной мембране митохондрий, ядерной мембране, клеточной мембране эритроцитов. Редуктазная цепь относится к самым быстрым реакциям биологического окисления. Взаимодействие монооксигеназной и редуктазной цепей представлено на схеме:
Рис. 8. Схема взаимосвязи редуктазной и монооксигеназной цепи микросомального окисления.
Иногда ошибочно считают, что монооксигеназная цепь микросом предназначена только для окисления ксенобиотиков. На самом деле она служит универсальной биологической системой окисления неполярных соединений любого происхождения, поскольку цитохром Р450, непосредственно участвующий в окислении, находится в липидном слое мембран. Субстрат, окисляемый цитохромом Р450 должен отвечать одному требованию – быть неполярным (относительная субстратная специфичность). II фаза – Конъюгация – может быть двух типов: I тип реакций – когда предварительно активируется конъюгирующее вещество. Наиболее частый вид конъюгации. Примером реакций данного типа могут служить глюкуронидная и сульфатная конъюгации. 1. Глюкуронидная. Молекула глюкуроновой кислоты находится в виде УДФ-глюкуроновой кислоты (УДФГК). Фермент, который переносит глюкуроновую кислоту на молекулу конъюгируемого вещества, называется УДФ-глюкуронилтрасфераза (рис. 9).
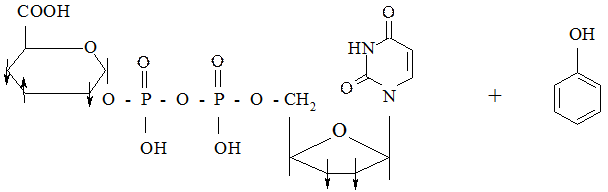

Рис. 9. Глюкуронидная конъюгация (на примере молекулы фенола).
3. Сульфатная. Молекула серной кислоты находится в виде 3-фосфоаденозил-5-фосфосульфата (ФАФС). Фермент, который переносит остаток серной кислоты на молекулу конъюгируемого вещества, называется арилсульфотрансфераза (рис. 10).

Рис. 10. Сульфатная конъюгация (на примере молекулы фенола).
Примером сульфатной конъюгации является также обезвреживание продуктов превращения триптофана в результате процессов гниения в кишечнике:



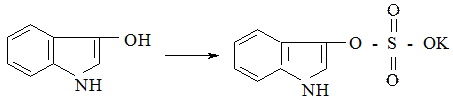
Рис. 11. Схема обезвреживания продуктов гниения триптофана. II тип реакций. Сначала активируется ксенобиотик, который затем переносится на конъюгирующую биомолекулу с образованием конъюгата. Относительно редкий вид конъюгации. Примером реакций конъюгации данного типа является глициновая конъюгация бензойной кислоты, которая протекает в два этапа: 1.

2.
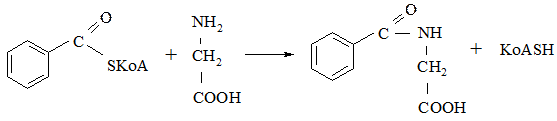
Рис. 12. Схема обезвреживания бензойной кислоты.
Гиппуровая кислота выделяется с мочой. В клинике для оценки обезвреживающей функции печени используют пробу Квика-Пытеля: больному дают нагрузку бензойной кислотой и по скорости прироста количества гиппуровой кислоты в моче судят об обезвреживающей функции печени. Химический канцерогенез О химическом канцерогенезе говорят, когда в ходе биотрансформации изначально безвредных молекул образуются канцерогенные вещества. Как говорилось ранее, в ходе биотрансформации, как правило, более токсичные вещества, переходят в менее токсичные. Однако такая закономерность наблюдается не всегда. Примером может служить биотрансформация компонента табачного дыма – бензпирена (содержится в больших количествах в копченостях и пиве). Изначально бензпирен является безвредным для организма веществом. Однако, являясь ксенобиотиком, подвергается биотрансформации с участием микросомальной системы окисления с образованием сильнейших канцерогенов – 3-гидроксибензпирена и 3, 6 – бензпиренхинона (рис. 13).
   
Рис. 13. Биотрансформация бензпирена.
Контрольные вопросы 1. Дайте определение ксенобиотикам. Какие вещества к ним относятся? 2. Назовите этапы обезвреживания ксенобиотиков в организме, их значение. 3. Напишите схему монооксигеназной цепи микросомального окисления, охарактеризуйте ее элементы. 4. Охарактеризуйте редуктазную цепь микросомального окисления, покажите ее взаимосвязь с монооксигеназной цепью. 5. Какие вы знаете виды конъюгации в печени? Приведите примеры конъюгаций I и II типа. 6. Что такое химический канцерогенез? Приведите пример. ТЕСТОВЫЕ ЗАДАНИЯ Выберите один правильный ответ на каждый вопрос. 8. ИСТОЧНИКОМ ВОДОРОДА В МОНООКСИГЕНАЗНОЙ ЦЕПИ МИКРОСОМАЛЬНОГО ОКИСЛЕНИЯ ЯВЛЯЕТСЯ: 1) НАДН∙ Н+; 2) НАДФН∙ Н+ ; 3) восстановленная форма убихинона; 4) ФАДН2; 5) вода. 9. ИСТОЧНИКОМ ВОДОРОДА В РЕДУКТАЗНОЙ ЦЕПИ МИКРОСОМАЛЬНОГО ОКИСЛЕНИЯ ЯВЛЯЕТСЯ: 1) НАДН∙ Н+; 2) НАДФН∙ Н+; 3) восстановленная форма убихинона; 4) ФАДН2; 5) вода. 10. СУБСТРАТ, ОКИСЛЯЮЩИЙСЯ ЦИТОХРОМОМ Р450 ДОЛЖЕН ОТВЕЧАТЬ СЛЕДУЮЩЕМУ ГЛАВНОМУ ТРЕБОВАНИЮ: 1) быть полярным; 2) быть неполярным; 3) иметь в составе двойную связь; 4) иметь в составе аминогруппу; 5) относится к классу ароматических веществ. 11. В ПРОЦЕССЕ КОНЪЮГАЦИИ БЕНЗОЙНОЙ КИСЛОТЫ ОНА ВСТУПАЕТ В РЕАКЦИЮ С АМИНОКИСЛОТОЙ: 1) метионином; 2) глутамином; 3) триптофаном; 4) глицином; 5) пролином. 12. ПРИ ПРОВЕДЕНИИ ПРОБЫ КВИКА-ПЫТЕЛЯ В МОЧЕ ОБСЛЕДУЕМОГО ОПРЕДЕЛЯЮТ СОДЕРЖАНИЕ: 1) мочевой кислоты; 2) бензойной кислоты; 3) креатинина; 4) гиппуровой кислоты; 5) мочевины. СИТУАЦИОННЫЕ ЗАДАЧИ Задача №1. Из практики известно, что пациенту в состоянии алкогольного опьянения не желательно назначение лекарственных препаратов и средств для наркоза. Дайте обоснованный ответ, с чем это связано? Задача №2. При обследовании двух пациентов, у одного из них в моче обнаружено повышенное содержание животного индикана, а в моче другого, помимо повышенного содержания животного индикана, обнаружен индол. Какие нарушения у пациентов можно предположить по результатам анализа? Популярное:
|
Последнее изменение этой страницы: 2017-03-11; Просмотров: 3472; Нарушение авторского права страницы